
【题目】甲、乙、丙、丁、戊是中学常见的物质,其中甲、乙为单质,它们的转化关系如下图所示(某些条件和部分产物已略去)。下列说法不正确的是( )
![]()
A. 若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序一定为甲<丙<戊
B. 若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙可能为Na2O2
C. 若丙、丁混合产生白烟,且丙分子为18电子分子,丁分子为10电子分子,则乙的水溶液可能具有漂白性
D. 若甲既能与盐酸反应又能与NaOH溶液反应,则戊可能属于两性氢氧化物
【答案】A
【解析】A.若甲、丙、戊含有同一种元素,当甲为S,乙为氧气,丙为二氧化硫,丁为HClO等具有强氧化性的物质,戊为硫酸,则含S元素的化合价由低到高的顺序为甲<丙<戊,若甲为氯气,乙为氢气,丙为HCl,戊可以为氯化物,化合价不符合题意,故A错误;B.甲为短周期中原子半径最大的主族元素的单质,则甲为Na,乙为氧气,二者反应生成的丙可能为Na2O2或Na2O,故B正确;C.丙、丁混合产生白烟,且丙为18电子分子,丁为10电子分子,则丙为HCl,丁为NH3,若乙为氯气,其水溶液中含有HClO,具有漂白作用,故C正确;D.甲为单质,既能与盐酸反应又能与NaOH溶液反应,则甲为Al,乙为硫,二者反应生成丙为硫化铝,戊为氢氧化铝,戊属于两性氢氧化物,故D正确;故选A。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】下列所得溶液的物质的量浓度等于0.1molL-1的是
A. 将16gCuSO4·5H2O充分溶解,配成1L溶液中
B. 将25gCuSO4·5H2O充分溶解,配成1L溶液
C. 将16gCuSO4充分溶解在1L水中
D. 将25gCuSO4·5H2O充分溶解在1L水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于0.1 mol/L Na2SO3溶液,下列叙述正确的是
A. c(Na+) : c(SO32―) < 2 : 1
B. c(Na+) = 2 c (SO32―) + c(HSO3―) + c(H2SO3)
C. c(Na+) + c(H+) = 2 c (SO32―) + 2 c(HSO3―) + c(OH―)
D. 加入少量NaOH固体,c(SO32―) 与c(Na+) 均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中某区域的一些元素多用于制造半导体材料,它们是
A. 左下方区域的金属元素 B. 右上方区域的非金属元素
C. 金属元素和非金属元素分界线附近的元素 D. 稀有气体元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氢化物有多种,在科学技术和生产中有重要的应用。根据题意完成下列计算:
(1)某氮的氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,确定该氢化物的分子式为____________。该氢化物受撞击则完全分解为氮气和氢气。4.30 g该氢化物受撞击后产生的气体在标准状况下的体积为____________L。
(2)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为
6NO+4NH3=5N2+6H2O① 6NO2+ 8NH3=7N2+12H2O②
反应①中氧化剂是__________,还原剂与还原产物物质的量之比_______________;如NO与NO2混合气体87g被过量氨水(质量分数0.300)完全吸收,产生50.4L氮气(标准状况下测定),则计算混合气体中NO与NO2的体积比为多少____________?(要求写计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物甲与![]() 发生酯反应的产物A是一种食用香料。11.6g甲完全燃烧可产生0.6mo1 CO2和0.6mo1 H2O。相同条件下,甲蒸气对氧气的相对密度为1.8125,甲分子为链状结构且不含甲基。回答下列问题:
发生酯反应的产物A是一种食用香料。11.6g甲完全燃烧可产生0.6mo1 CO2和0.6mo1 H2O。相同条件下,甲蒸气对氧气的相对密度为1.8125,甲分子为链状结构且不含甲基。回答下列问题:
(1)甲中的结构简式为_________________________。
(2)甲中含有的官能团名称为___________________。
(3)![]() 有多种同分异构体,其中属于酯类,能使FeCl3溶液显紫色,且苯环上的一氯代物有两种的同分异构体的结构简式为_______________________(任写两种)。
有多种同分异构体,其中属于酯类,能使FeCl3溶液显紫色,且苯环上的一氯代物有两种的同分异构体的结构简式为_______________________(任写两种)。
(4)已知:![]() (
(![]() )A的合成路线如下:
)A的合成路线如下:
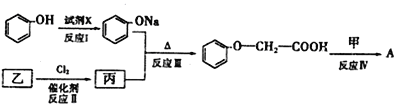
①试剂x不可选用________(填序号)
A.NaOH溶液 B.Na2 CO3溶液 C.NaHCO3溶液 D.Na
②乙的结构简式为___________________,反应Ⅲ的反应类型为______________。
③反应Ⅳ的化学方程式为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
84消毒液
有效成分 NaClO
规格 1 000 ml
质量分数 25%
密度 1.19 g·cm-3
(1)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=____mol·L-1。
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL该消毒液。下列说法正确的是________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
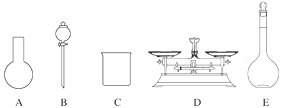
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(3)配制溶液的过程如下,该同学的错误步骤有(____)
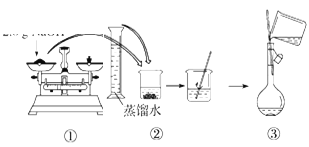
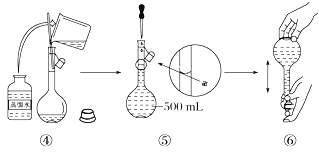
A.1处 B.2处 C.3处 D.4处
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。需用浓硫酸的体积为____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A. ![]() =1×10-13 mol·L-1的溶液中:NH
=1×10-13 mol·L-1的溶液中:NH![]() 、Ca2+、Cl-、NO
、Ca2+、Cl-、NO![]()
B. 使酚酞变红色的溶液中:Na+、Al3+、SO![]() 、Cl-
、Cl-
C. 与Al反应能放出H2的溶液中:Fe2+、K+、NO![]() 、SO
、SO![]()
D. 水电离的c(H+)=1×10-13 mol·L-1的溶液中:K+、Na+、AlO![]() 、CO
、CO![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com