
【题目】以2-甲基丙烯为原料,合成有机玻璃F的合成路线如下:
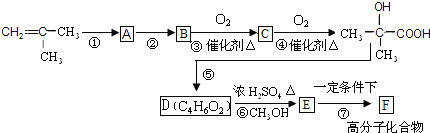
(1)填写反应类型:反应⑦是____________________,反应⑤是____________。
(2)写出结构简式:B_________________ F__________________。
(3)写出物质D中所含官能团的名称:___________________________。
(4)写出反应③的化学方程式_____________________________________。
(5)已知:化合物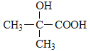 同类别的同分异构体G,在一定条件下能形成八元环状化合物。则G可能的结构简式为:_____________________________________________________。
同类别的同分异构体G,在一定条件下能形成八元环状化合物。则G可能的结构简式为:_____________________________________________________。
(6)完成反应:_________________________________________
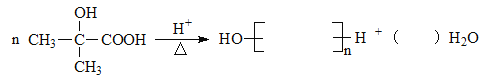
【答案】加聚反应 消去反应 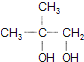
 碳碳双键、羧基
碳碳双键、羧基  +O2
+O2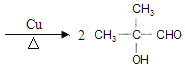 +H2O HOOCCH(CH3)CH2OH或HOOCCH2CH(CH3)OH
+H2O HOOCCH(CH3)CH2OH或HOOCCH2CH(CH3)OH 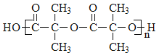 ;n-1
;n-1
【解析】
由反应历程可知2-甲基丙烯先与溴发生加成反应,然后水解生成二元醇,氧化分别生成醛、酸,经消去后生成2-甲基丙烯酸,与甲醇发生酯化反应生成2-甲基丙烯酸酯,经聚合反应可生成有机物玻璃,即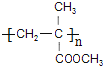 ,则A为CH3CBr(CH3)CH2Br,B为
,则A为CH3CBr(CH3)CH2Br,B为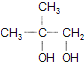 ,C为CH3COH(CH3)CHO,D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH3,结合有机物的结构和性质以及题目要求和解答该题。
,C为CH3COH(CH3)CHO,D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH3,结合有机物的结构和性质以及题目要求和解答该题。
由反应历程可知2-甲基丙烯先与溴发生加成反应,然后水解生成二元醇,氧化分别生成醛、酸,经消去后生成2-甲基丙烯酸,与甲醇发生酯化反应生成2-甲基丙烯酸酯,经聚合反应可生成有机物玻璃,即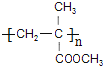 ,则A为CH3CBr(CH3)CH2Br,B为
,则A为CH3CBr(CH3)CH2Br,B为 ,C为CH3COH(CH3)CHO,D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH3,
,C为CH3COH(CH3)CHO,D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH3,
(1)由官能团的变化可知反应⑦为CH2=C(CH3)COOCH3生成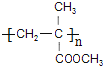 的反应,应为加聚反应,反应⑤为
的反应,应为加聚反应,反应⑤为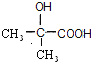 生成的CH2=C(CH3)COOH反应,应为消去反应;
生成的CH2=C(CH3)COOH反应,应为消去反应;
(2)由以上分析可知B为 ,F为
,F为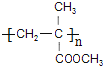 ;
;
(3)D为CH2=C(CH3)COOH,含有碳碳双键、羧基;
(4)反应③为 在Cu作催化剂条件下发生催化氧化的反应,反应的方程式为
在Cu作催化剂条件下发生催化氧化的反应,反应的方程式为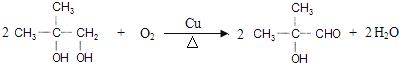 ;
;
(5)已知:化合物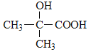 同类别的同分异构体G,在一定条件下能形成八元环状化合物。则两分子G反应可生成八元环状酯类化合物,所以G中的羧基和羟基连在相邻两个C原子上,则G可能的结构简式为:HOOCCH(CH3)CH2OH或HOOCCH2CH(CH3)OH;
同类别的同分异构体G,在一定条件下能形成八元环状化合物。则两分子G反应可生成八元环状酯类化合物,所以G中的羧基和羟基连在相邻两个C原子上,则G可能的结构简式为:HOOCCH(CH3)CH2OH或HOOCCH2CH(CH3)OH;
(6)反应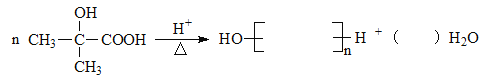 为
为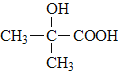 在一定条件下发生缩聚反应生成
在一定条件下发生缩聚反应生成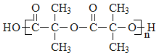 和水,故
和水,故![]() 应为
应为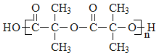 ,H2O前面的计量数为n-1。
,H2O前面的计量数为n-1。


科目:高中化学 来源: 题型:
【题目】环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如下图。下列对该物质的叙述中,正确的是
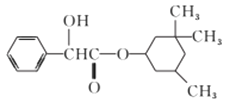
A. 该有机物苯环上的二氯代物共有8种
B. 该有机物分子中至少有7个碳原子共平面
C. 该有机物可以与Br2的CCl4溶液发生加成反应使之褪色
D. 1mol该有机物最多可与2molNaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究氯、溴、硫的非金属性强弱,设计如下实验装置(加热及夹持装置已略)。
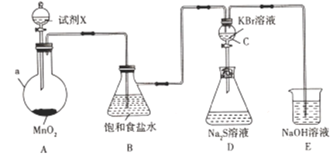
(1)仪器a的名称是______。试剂X是_____________。
(2)写出装置A中发生反应的化学方程式:__________________________________
(3)装置E中NaOH溶液的作用是____________________________________________
(4)反应一段时间后,观察到装置C中溶液变为橙黄色,说明非金属性:Cl___Br( 填“>"或"<")。
(5)打开装置C中的活塞,将装置C中的溶液逐渐滴人装置D中,振荡。观察到的现象是______________,写出可能发生反应的离子方程式:_____________________________________写一个即可),根据此现象不一定能说明溴的非金属性比硫强,原因是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态O原子的电子排布图为_______,基态O原子电子占据最高能级的电子云轮廓图为____形,O原子最外层电子的运动状态有_____种。
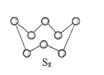
(2)下图为S8的结构,该分子中S原子的杂化轨道类型为______________。其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为_____________。
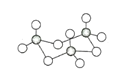
(3)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形;固体三氧化硫中存在如下图所示的三聚分子,该分子中S原子的价层电子数___________。
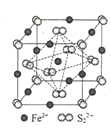
(4)FeS2晶体的晶胞如图所示。晶胞中有Fe2+_____个,有S22-_____个,晶胞中Fe2+位于S22-所形成的____(填空隙名称)的体心。晶胞边长为a nm、FeS2相对分子质量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________gcm﹣3。
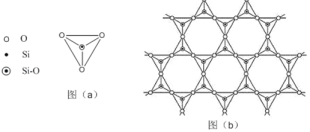
(5)在硅酸盐中,SiO44﹣四面体(如下图(a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长层状结构的多硅酸根;其中Si原子的杂化形式为____。该多硅酸根的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应或离子反应方程式正确的是
A. 苯与溴水反应:2![]() +Br2
+Br2![]()
B. 1一氯丙烷中加入氢氧化钠溶液并加热:CH3CH2CH2Cl+NaOH= CH3CH=CH2↑+NaCl+H2O
C. 苯酚钠溶液中通入少量CO2:C6H5O-+H2O+CO2→C6H5OH+HCO3-
D. 实验室制取乙炔的反应:CaC2+H2O → CaO + CH≡CH↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行以下实验,能得到相应实验结论的是
① | ② | ③ | 实验结论 |
| |
A | 浓氨水 | NaOH | 酚酞 | NaOH的碱性比 NH3H2O的强 | |
B | 浓盐酸 | MnO2 | 淀粉溶液 | 非金属性:氯元素大于碘元素 | |
C | 浓硝酸 | Na2CO3 | Na2SiO3 | 酸性:HNO3 > H2CO3 > H2SiO3 | |
D | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在短周期元素中:
①元素周期表IA族中金属性最强的元素(符号)是____,与水反应最剧烈的VIIA族中的非金属元素的(符号)是___;
②原子核外电子总数是其最外层电子数2倍的元素名称是__,最外层电子数为电子层2倍的元素名称有____。
(2)已知某主族元素的原子结构示意图如图,Y在周期表的位置为___。

(3)A2-原子核内有x个中子,其质量数为m,则ngA2-所含电子的物质的量为__。
(4)X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示。
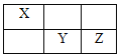
已知X、Y、Z三元素的原子序数之和为40,回答下列问题:
①Z元素的原子结构示意图为___。
②与Y同主族的下一周期元素的原子序数是___。
③X的气态氢化物与Y的最高价氧化物对应水化物发生的化学反应方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图中的实验装置进行相应的实验,不能达到实验目的的是( )
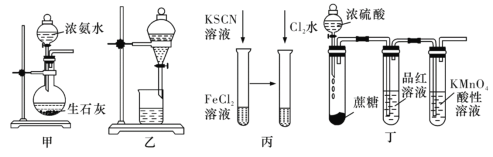
A.用图甲装置,可快速制取氨气
B.用图乙装置,分离饱和食盐水溶液中的食盐和水
C.用图丙装置操作方法,可检验Fe2+
D.用图丁装置,可说明浓H2SO4具有脱水性和强氧化性.,SO2具有漂白性和还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com