
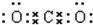 ,
,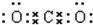 ;
; 

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
| A | B | C | D | ||||
 |  |  |  | ||||
| 闪电时会发生反应: N2+O2
| 利用丁达尔效应证明烧杯中的分散系是胶体 | 蔗糖中加入浓硫酸搅拌后变黑,因为浓硫酸有吸水性 | 加热时熔化的铝不滴落,证明Al2O3的熔点比Al高 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性:Y(OH)2>WOH |
| B、阴离子的还原性:X->Z- |
| C、原子半径:W>Y>Z>X |
| D、气态氢化物的稳定性:HX>HZ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验 | 操作 |
| A | 钠与水反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 证明某溶液中含Fe2+ | 取少量该溶液先加入氯水,再滴加KSCN溶液 |
| D | 取出分液漏斗中的上层液体 | 下层液体从分液漏斗下端管口放出,及时关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、取同量的溶液于两支试管中,各滴入酚酞试液,红色较深的是Na2CO3 |
| B、取同量的溶液于两支试管中,加热,有气泡产生的是NaHCO3 |
| C、取同量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO3 |
| D、取同量的溶液于两支试管中,滴加Ba(OH)2溶液,生成白色沉淀的是Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验目的 | 仪器 |
| A | 出去氢氧化铁胶体中的泥沙 | 漏斗(带滤纸)、烧杯、玻璃棒 |
| B | 从食盐水中获得NaCl晶体 | 玻璃棒、酒精灯、泥三角 |
| C | 分离含有碘的四氯化碳和水的混合物 | 分液漏斗、烧杯 |
| D | 用普通酒精制备无水酒精 | 酒精灯、石棉网、蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
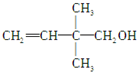 在下列反应中,如图有机物能发生的是( )
在下列反应中,如图有机物能发生的是( )| A、①②③⑤ | B、①②③④ |
| C、①②④⑤ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中C、H个数比为1:2 |
| B、分子中的C、H的个数比为2:1 |
| C、该有机物的相对分子质量为14 |
| D、该烃常温下是气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com