
| 选项 | 实验目的 | 仪器 |
| A | 出去氢氧化铁胶体中的泥沙 | 漏斗(带滤纸)、烧杯、玻璃棒 |
| B | 从食盐水中获得NaCl晶体 | 玻璃棒、酒精灯、泥三角 |
| C | 分离含有碘的四氯化碳和水的混合物 | 分液漏斗、烧杯 |
| D | 用普通酒精制备无水酒精 | 酒精灯、石棉网、蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
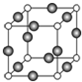 已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大.元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同.
已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大.元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x=y | B、x=2y |
| C、x=3y | D、以上均不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定不能喝含有食盐的水,因为那样会越喝越渴 |
| B、最好喝纯净水,因为纯净水不含任何化学物质 |
| C、最好喝含有氯化钠的水,这样可以补充必需的盐分 |
| D、最好不喝自来水,因为自来水都是用氯气、漂白粉或二氧化氯消毒过,这些物质在水中会损害身体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④ | B、①③ | C、②④ | D、③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com