
【题目】氯化物在工业生产、日常生活中应用都非常广泛.某学习小组为探究一些实用性很强的氯化物,进行了一系列的资料查询与具体实验.
(1)用于制造电池的原材料二氯亚砜(SOCl2),是一种液态化合物,沸点为77℃.在盛10mL水的锥形瓶中小心滴加8~10滴SOCl2可观察到剧烈反应,液面上形成白雾,并逸出刺激性气味的气体,该气体可使沾有品红试液的滤纸褪色.轻轻振荡锥形瓶,待白雾消失后往溶液中滴加AgNO3溶液,有不溶于稀HNO3的白色沉淀析出.室温下,小组某同学取2.38g SOCl2与水发生上述反应,测得放出热量为17.88kJ.根据以上实验,写出SOCl2与水反应的热化学方程式 .
(2)低温蒸干AlCl3溶液得到固体的主要成分是;小组某同学想制取无水AlCl3固体,他提出可以用AlCl36H2O与SOCl2混合后共热来制取无水AlCl3固体,你认为可行吗?请说明原因 .
(3)TiO2是一种非常好的催化剂.某同学通过查阅资料显示:TiCl4水解程度很大,可以用于TiO2的制备,制备时加入大量的水,同时加热,促进水解趋于完全,所得TiO2xH2O经焙烧得TiO2 . 请写出TiCl4水解的化学方程式
(4)某同学利用NaCl溶液设计实验验证Fe在原电池反应中的生成物,使用Cu电极、Fe电极、经过酸化的3%NaCl溶液,组成原电池装置,实验结束后,该同学往Fe电极区滴入2滴黄色铁氰化钾溶液,现象是: .
【答案】
(1)SOCl2(l)+H2O(l)═SO2(g)+2HCl(g)△H=﹣894kJ/mol
(2)Al(OH)3;AlCl3溶液易发生水解,AlCl3?6H2O与SOCl2混合后共热,SOCl2与AlCl3?6H2O中的结晶水作用,生成无水AlCl3及SO2和HCl气体
(3)TiCl4+(2+x)H2O?TiO2?xH2O↓+4HCl
(4)生成带有特征蓝色的铁氰化亚铁沉淀
【解析】解:(1)SOCl2是一种液态化合物,与水发生剧烈的非氧化还原反应,生成两种有刺激性气味的气体,该两种气体应该为氯化氢和二氧化硫,反应的方程式为SOCl2+H2O=2HCl↑+SO2↑,2.38g SOCl2与水发生上述反应,物质的量= ![]() =0.02mol,测得放出热量为17.88kJ,1molSOCl2与水发生上述反应放热894KJ,反应的热化学方程式为:SOCl2(l)+H2O(l)═SO2(g)+2HCl(g)△H=﹣894 kJ/mol.
=0.02mol,测得放出热量为17.88kJ,1molSOCl2与水发生上述反应放热894KJ,反应的热化学方程式为:SOCl2(l)+H2O(l)═SO2(g)+2HCl(g)△H=﹣894 kJ/mol.
所以答案是:+H2O(l)═SO2(g)+2HCl(g)△H=﹣894 kJ/mol;
(2.)低温蒸干AlCl3溶液,氯化铝水解生成氢氧化铝和盐酸,AlCl3+3H2OAl(OH)3+3HCl,蒸发过程中HCl挥发,促进水解正向进行得到固体的主要成分是水解产物氢氧化铝,低温蒸干AlCl3溶液得到固体的主要成分,SOCl2与水反应生成的氯化氢会对氯化铝水解起到抑制作用;反应的化学方程式为:SOCl2+H2O=2HCl↑+SO2↑,蒸干AlCl3溶液不能得到无水AlCl3 , 使SOCl2与AlCl36H20混合并加热,可得到无水AlCl3 , SOCl2与水反应生成的氯化氢会对氯化铝水解起到抑制作用,
所以答案是:Al(OH)3 , AlCl3溶液易发生水解,AlCl36H2O与SOCl2混合后共热,SOCl2与AlCl36H2O中的结晶水作用,生成无水AlCl3及SO2和HCl气体;
(3.)在加热的条件下,TiCl4水解得TiO2xH2O和HCl,反应方程式为:TiCl4+(x+2)H2O ![]() TiO2xH2O↓+4HCl↑,所以答案是:TiCl4+(x+2)H2O
TiO2xH2O↓+4HCl↑,所以答案是:TiCl4+(x+2)H2O ![]() TiO2xH2O↓+4HCl↑;
TiO2xH2O↓+4HCl↑;
(4.)使用Cu电极、Fe电极、经过酸化的3%NaCl溶液,组成原电池装置,金属铁是负极,发生电极反应:Fe﹣2e﹣=Fe2+;滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液时,发生反应:3Fe2++2[Fe(CN)6]3﹣=Fe3[Fe(CN)6]2↓,产生蓝色沉淀,所以答案是:生成带有特征蓝色的铁氰化亚铁沉淀;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】高铁轨道焊接常用到铝热反应,某学习小组进行铝热反应实验,装置如图所示。
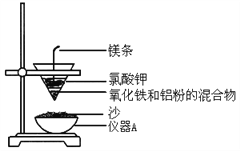
(1)仪器 A 的名称为_______。
(2)写出工业上制取金属镁的化学方程式______。
(3)点燃镁条引发反应,在反应过程中没有涉及到的化学反应类型是_______。
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
(4)写出该铝热反应的化学方程式,并用单线桥表示电子转移的方向和数目_______。
(5)铝热反应中放出大量的热,有黑色熔融物落入沙中。学习小组推测黑色熔融物中除了含有铁和氧化铝,还含有铝和氧化铁,实验验证如下:
Ⅰ. 向冷却后的黑色固体中加入 NaOH 溶液,观察到有气体产生。实验结论:黑色固体中含有铝。写出该反应的离子方程式:________。
Ⅱ. 取少量黑色固体于试管中,加入稀盐酸,固体溶解,有气泡产生。向所得溶液中滴入几滴 0.01 mol·L- 1 KSCN 溶液,溶液不变色。实验结论:黑色固体中不含氧化铁。
你认为实验结论是否合理?____(填“合理”或“不合理”)。理由是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图中的物质均为中学化学常见物质。已知A、B、C均为有刺激性气味的气体,A、B分别通入品红溶液中,红色均褪去;B、C分别通入紫色石蕊试液中,B使溶液先变红后褪色,C使溶液显蓝色;H为无色气体,I为红棕色气体。反应①需要有水参加,反应②有大量白烟生成。
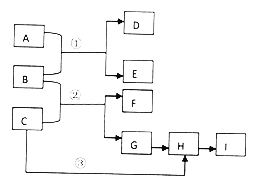
请回答下列问题:
(1)写出下列反应的化学方程式:
反应①_____________________________________;
反应②_______________________________________;
反应③____________________________________________;
(2)用Na2CO3溶液吸收I生成CO2,若9.2gI和Na2CO3溶液完全反应时转移0.1mol电子,则反应的离子方程式为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是甲醇(CH3OH)燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.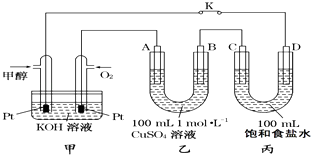
(1)甲中负极的电极反应式为 .
(2)乙中A极电极反应式为 , A极析出的气体在标准状况下的体积为 .
(3)丙装置溶液中C极的质量变化为 . 若在丙装置溶液中滴入酚酞溶液进行上述实验,D极附近能观察到的实验现象: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.10 mol·L-1盐酸逐滴滴入20.00 mL 0.10 mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH= -lg c(OH-)。

下列说法正确的是
A. M点所示溶液c(NH4+)+c(NH3·H2O)= c(Cl-)
B. N点所示溶液中:c(NH4+)>c(Cl-)
C. Q点所示消耗盐酸的体积等于氨水的体积
D. M点和N点所示溶液中水的离子积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T℃下,分别在三个容积为10L的恒容绝热密闭容器中,发生反应:2CO(g)+SO2(g)![]() S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
容器 | 起始时物质的量/mol | 平衡时CO2(g)的物质的量/mol | |||
CO(g) | SO2(g) | S(g) | CO2(g) | ||
甲 | 1 | 0.5 | 0.5 | 0 | a |
乙 | 1 | 0.5 | 0 | 0 | 0.8 |
丙 | 2 | 1 | 0 | 0 | b |
下列说法正确的是
A. 其他条件不变,容器乙达到平衡后,再充入体系中四种气体各1mol,平衡逆向移动
B. b=1.6
C. 平衡常数:K甲>K乙
D. 其他条件不变,向容器甲再充入1mol CO,平衡常数(K)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置就用于实验室制取NH3 , 并用AlCl3溶液吸收多余氨气制氢氧化铝,最后回收氯化铵的实验,能达到实验目的是( )
A.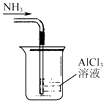
吸收NH3制取Al(OH)3
B.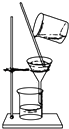
在不断搅拌下分离Al(OH)3和NH4Cl溶液
C.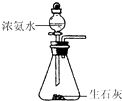
制取NH3
D.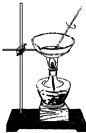
蒸干NH4Cl溶液并灼烧制NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com