
【题目】实验室需用480 mL 0.1 mol·L-1的硫酸铜溶液,现选取500 mL容量瓶进行配制,以下操作能配制成功的是( )
A.称取7.68 g CuSO4粉末,加入500 mL水
B.称取12.5 g CuSO4·5H2O晶体,加水配成500 mL溶液
C.称取8.0 g CuSO4粉末,加入500 mL水
D.称取8.0 g CuSO4·5H2O晶体,加水配成500 mL溶液
科目:高中化学 来源: 题型:
【题目】在Na+浓度为0.5mol·L-1的某澄清溶液中,还可能含有下表中的若干种离子。
阳离子 | K+ Ag+ Mg2+ Ba2+ |
阴离子 | NO3- CO32- Cl- SO42- |
现取该溶液100mL进行如下实验(气体体积均在标准状况下测定)。
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀硝酸 | 放出标准状况下0.56L无色气体 |
Ⅱ | 向Ⅰ的反应混合液中加入过量的硝酸钡,产生白色沉淀,对沉淀洗涤、干燥,称量所得固体质量 | 固体质量为9.32克 |
Ⅲ | 向Ⅱ的滤液中滴加硝酸银溶液 | 无明显现象 |
请回答下列问题。
(1)实验Ⅰ能确定一定不存在的离子是___。
(2)实验Ⅰ中生成气体的离子方程式为___。
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)。___
阴离子 | NO3- | CO32- | Cl- | SO42- |
c/mol·L-1 |
(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组同学设计如图实验装置(部分夹持仪器未画出)探究氨气的还原性并检验部分产物。
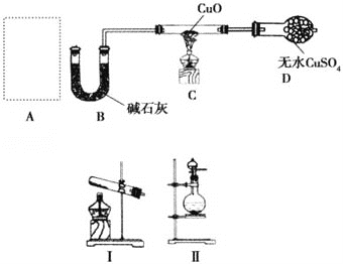
(1)若A中使用装置Ⅰ制取氨气,则化学方程式为__,发生装置试管口略向下倾斜的原因_____;若A中使用装置Ⅱ制取氨气,则分液漏斗中的试剂为__,圆底烧瓶中的固体可以为__。
(2)B中碱石灰的作用是__。
(3)氨气还原炽热氧化铜的化学方程式为__,装置C中的实验现象为__,装置D中的实验现象为__。
(4)①该装置存在明显的缺陷是__。
②请画出改进后需要增加连接的实验装置图________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA 表示阿伏加德罗常数的值,下列说法正确的是
A.100 mL 0.1 mol·L-1的稀硫酸中含有SO42-个数为0.1NA
B.含1 mol HCl的盐酸与足量Fe反应,Fe所失去的电子总数为2 NA
C.4℃ 时,5.4 mL水中所含的水分子数是0.3 NA
D.标准状况下,22.4L氢气所含的质子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)含0.3 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是___________。
(2)___________g H2O2所含原子数与0.2 mo lH3PO4所含原子数相等。
(3)质量相同的H2、NH3、SO2、O3四种气体中,含有原子数目最少的是_____(填写化学式)。
(4)如果规定,1mol粒子集合体所含的粒子数与0.024 kg 12C中所含的碳原子数相同。那么将36.5 g HCl溶于水中配成溶液500mL,则溶液的浓度为_________mol/L。
(5)同温同压下,某容器充满氧气重116g,若充满二氧化碳重122g,现充满某气体重114g,则该气体的摩尔质量为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学好化学知识的重要基础,下列有关化学用语表示正确的有( )
①用电子式表示HCl的形成过程:![]()
②MgCl2的电子式:![]() ③质量数为133、中子数为78的铯原子:
③质量数为133、中子数为78的铯原子:![]() Cs
Cs
④乙烯、乙醇结构简式依次为:CH2=CH2、C2H6O ⑤S2﹣的结构示意图:![]()
⑥次氯酸分子的结构式:H-O-Cl ⑦CO2的分子模型示意图:![]()
A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁(PFS)是水处理中重要的絮凝剂,如图是以回收废铁屑为原料制备PFS的一种工艺流程.
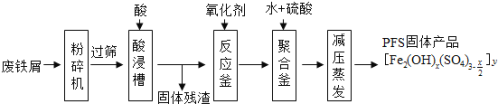
回答下列问题
(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为_______。粉碎过筛的目的是________。
(2)酸浸时最合适的酸是______,写出铁锈与酸反应的离子方程式_________。
(3)反应釜中加入氧化剂,下列氧化剂中最合适的是______(填标号).
A.KMnO4 B.Cl2C.H2O2D.HNO3
(4)相对于常压蒸发,减压蒸发的优点是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质用途的叙述中不正确的是
A.过氧化钠可用于呼吸面具或潜水艇中作为氧气的来源
B.在常温下可用铝制容器贮藏运输浓硫酸
C.Al(OH)3可作治疗胃酸过多的一种药剂
D.Al2O3 和MgO是较好的耐火材料,两者均易与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图.下列说法正确的是 ( )

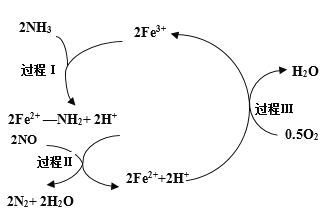
A.NH3催化还原NO为吸热反应
B.过程Ⅰ中NH3断裂非极性键
C.过程Ⅱ中NO为氧化剂,Fe2+为还原剂
D.脱硝的总反应为: 4NH3(g)+4NO(g)+ O2(g) ![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com