
����Ŀ����֪��H2(g)�� F2(g)===2HF(g)�������仯��ͼ��ʾ�������й���������ȷ����(����)

A. ����������ֽ����������ͷ����ķ�Ӧ�Ƿ��ȷ�Ӧ
B. 1 mol H2��1 mol F2��Ӧ����2 molҺ̬HF�ų�������С��270 kJ
C. ����ͬ��������1 mol H2��1 mol F2�������ܺʹ���2 mol HF���������
D. ����1 mol H��H����1 mol F��F�����յ����������γ�2 mol H��F���ų�������
���𰸡�C
��������A����ͼ���֪��2molHF(g)������С��1molH2(g)��1molF2(g)���������ʷ���������ֽ����������ͷ����ķ�Ӧ�����ȷ�Ӧ����A����B��2molҺ̬HF������С��2molHF(g)�����������ڷ��ȷ�Ӧ������Ӧ����ͬʱ�����������Խ�ͣ���Ӧ�ų�������Խ�࣬�ʷų�����������270KJ����B����C��1molH2(g)��1molF2(g)����2molHF(g)���ȣ���1molH2(g)��1molF2(g)������������������2molHF(g)�����е���������C��ȷ��D������1molH2(g)��1molF2(g)����2molHF(g)���ȣ�����Ӧ����H=�ϼ����յ�����-�ɼ��ų���������0���ʶ���1molH-H����1molF-F���ų�������С���γ�2molH-F���ų�����������D����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. CO2��NO2��SO2���ᵼ��������γ� B. ľ�Ľ���ˮ�����������õķ�������
C. ʯӢ������ˮ�ࡢ�մɶ��ǹ����β�Ʒ D. ����й©����Ӧ��������ʹ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥCO2�е�HCl��������ǽ��������ͨ��������
A������NaOH��Һ B������NaHCO3��Һ
C������Na2CO3��Һ D��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ���γɵĴ�����A��B��C��D��E����������֮���ת����ϵ��ͼ��ʾ������A������B֮��ķ�Ӧ������Һ�н���(E������A��B���������е�һ����ͬ)��

��ش��������⣺
��1����C�����ӻ����D��һ��ǿ���C�Ļ�ѧʽ________������дһ��C����Ҫ��; ��
��2����E��ˮ��Һ�������ԣ�D�Ǽ�������ǿ�ᡢ��������ǿ��Ļ����
���õ��뷽��ʽ����D��������ǿ�ᡢ��������ǿ���ԭ��(��д�����뷽��ʽ����)�� ________________________��
���õ���غ�ĵ�ʽ��ʾE��NaOH��Һ��Ӧ�������ε���Һ���������ӵ�Ũ��֮��Ĺ�ϵ��________________________________��
��3����C��һ�����壬D��һ��ǿ�ᣬ��
��C��ˮ��Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
����֪����������A������B��Ӧ����1 mol����C�Ħ�H=��57 kJ��mol��1��1 mol����C��H2O��Ӧ���ɻ�����D������E�Ħ�H=��46 kJ��mol��1��д������A������B��ˮ��Ӧ���ɻ�����D���Ȼ�ѧ����ʽΪ__________________________________________��
��������Ϊ��ŨH2SO4���Ը�������C����ijͬѧΪ����֤�ù۵��Ƿ���ȷ������ͼ��ʾװ�ý���ʵ�顣
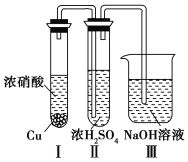
ʵ������У���ŨH2SO4��δ�����������ݳ�����ó��Ľ�����____________________________��
���ò����缫���H2SO4����Һ���������ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������,��ȷ����
A. �ڱ�״����,1mol�κ����ʵ����Ϊ22.4L
B. �������ʵ��������ʵ������������,H+�����ʵ���Ҳ���
C. 1 mol H2��1mol He��,�����ķ�������ͬ��ԭ������ͬ
D. ���Ϊ6L��O2,����������Ϊ8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[2016���¿α�II��]ij��ͬѧ������ʵ��̽��Fe2+��Fe3+�����ʡ��ش��������⣺
��1���ֱ�ȡһ�����Ȼ������Ȼ��������壬�����Ƴ�0.1 mol/L����Һ����FeCl2��Һ�������������м����Ŀ����__________________________��
��2������ͬѧȡ2 mL FeCl2��Һ�����뼸����ˮ���ټ���1��KSCN��Һ����Һ��죬˵��Cl2�ɽ�Fe2+������FeCl2��Һ����ˮ��Ӧ�����ӷ���ʽΪ_______________________________��
��3������ͬѧ��Ϊ�����ʵ�鲻���Ͻ�������ͬѧ��2 mL FeCl2��Һ���ȼ���0.5 mLú�ͣ�����Һ�������μ��뼸����ˮ��l��KSCN��Һ����Һ��죬ú�͵�������______��
��4������ͬѧȡ10 mL 0.1 mol/L KI��Һ������6 mL 0.1 mol/L FeCl3��Һ��ϡ��ֱ�ȡ2 mL����Һ��3 ֧�Թ��н�������ʵ�飺
����һ֧�Թ��м���1 mL CCl4��������ã�CCl4�����ɫ��
���ڶ�֧�Թ��м���1��K3[Fe(CN)6] ��Һ��������ɫ������
������֧�Թ��м���1��KSCN��Һ����Һ��졣
ʵ���������������__________�������ӷ��ţ���ʵ��������˵������I ����������£���Һ���Ժ���___________�������ӷ��ţ����ɴ˿���֤����������ԭ��ӦΪ_____________________��
��5������ͬѧ��ʢ��H2O2��Һ���Թ��м��뼸���ữ��FeCl2��Һ����Һ����ػ�ɫ��������Ӧ�����ӷ���ʽΪ_______________________________��һ��ʱ�����Һ�������ݳ��֣������ȣ�����к��ɫ�������ɡ��������ݵ�ԭ����____________________________________________�����ɳ�����ԭ����___________________________________����ƽ���ƶ�ԭ�����ͣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ʹ��pH���������ⶨNa2CO3��NaHCO3�������NaHCO3�ĺ�������ȡ1.59 g��Ʒ������ˮ���250.00 mL��Һ��ȡ������Һ25.00 mL��0.1 mol��L��1������еζ����õ��������ߡ�����˵���������ȷ����( )
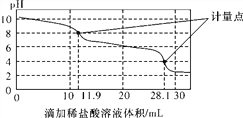
A. ��һ��������ǰ������Ӧ�����ӷ���ʽΪHCO(��H��===H2O��CO2��
B. ��һ����������Һ�д��ڴ�������������Cl����HCO(
C. ����Ʒn(NaHCO3)��(28.1��2��11.9)��10��4 mol
D. ʹ�ø÷����ⶨNa2CO3��NaOH�����Һ�е��������ƺ���������õ�1��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ѧ��Ѱ�Ҹ�Ч������ͨ�����·�Ӧʵ�ִ�����Ⱦ��ת����
2CO(g) +2NO(g) ![]() N2(g)+2CO2(g) ��H1
N2(g)+2CO2(g) ��H1
��֪��CO��ȼ���ȡ�H2=-283kJ/moL
N2(g) +O2(g) =2NO(g)���ֻ�ѧ���ļ����������£�
��ѧ�� | N��N�� | O=O�� | NO�е���� |
����(kJ/mol) | 945 | 498 | 630 |
���H1__________________��
��2��NH3��Ϊһ����Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863�ƻ����ں��º���װ���г���һ������NH3��O2����ij�����������½���������ӦI����ò�ͬʱ���NH3��O2��Ũ�����±���
ʱ�䣨min�� | 0 | 5 | 10 | 15 | 20 | 25 |
C(NH3)/mol��L-1 | 1.00 | 0.36 | 0.12 | 0.08 | 0. 0072 | 0.0072 |
C(O2)/mol��L-1 | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
�������й���������ȷ����______________
A.ʹ�ô���ʱ���ɽ��÷�Ӧ�Ļ�ܣ��ӿ��䷴Ӧ����
B. �����������4v��(NH3)=6v��(H2O)ʱ��˵����Ӧ�Ѵ�ƽ��
C.��������![]() =1ʱ��˵����Ӧ�Ѵ�ƽ��
=1ʱ��˵����Ӧ�Ѵ�ƽ��
D.ǰ10�����ڵ�ƽ������v��NO��=0.088mol��L-1��min-1
<>��3����������ʱ�ᷢ����������������ӦI��II�����������н�ǿ��ѡ���ԣ���רһ�ԡ���֪����ӦI 4NH3(g)+5O2(g)![]() 4NO(g) +6H2O(g)
4NO(g) +6H2O(g)
��Ӧ II��4NH3(g)+3O2(g) ![]() 2N2(g) +6H2O(g)
2N2(g) +6H2O(g)
Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���1L�ܱ������г���1 mol NH3��2mol O2������й����ʵ�����ϵ��ͼ��

�ٸô����ڸ���ʱѡ��Ӧ____________ (� I ���� II������
�� 520��ʱ��4NH3(g)+3O2![]() 4N2(g) +6H2O(g)��ƽ�ⳣ��K=________________ (��Ҫ��ó���������ֻ���г����ּ���ʽ����
4N2(g) +6H2O(g)��ƽ�ⳣ��K=________________ (��Ҫ��ó���������ֻ���г����ּ���ʽ����
����ͼ����жϣ���ӦI����Ӧ��H_______________ 0���>������<������=����
��C���B����������NO�����ʵ����ٵ���Ҫԭ��_________________________��
��4���ǰ���NH2OH���ĵ���ʽ_____________���ǰ���һ�ֻ�ԭ�����������������ԭ�廯�����������ʺ͵������÷�Ӧ�Ļ�ѧ����ʽΪ______________________________��
����25.00mL0.049mol/L���ǰ���������Һ����������������Һ����������·�Ӧ�����ɵ�Fe2+ǡ����24.50mL 0.020mol/L��KMnO4������Һ��ȫ���ã�����������Ӧ�У��ǰ�������������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[2016�����]�����Ƿ�չ�е�����Դ���������ð�������Ʊ��������Ӧ���������ڡ��ش��������⣺
��1����������ȣ�������Ϊȼ�ϵ��ŵ��� (���ٴ������)����������ֱ��ȼ�յ�����ת����Զ����ȼ�ϵ�أ�д����������ȼ�ϵ�صĸ�����Ӧʽ�� ��
��2�������������Ʊ�H2O2����֪��
H2(g)+A(l) ![]() B(l) ��H1
B(l) ��H1
O2(g)+B(l) ![]() A(l)+H2O2(l) ��H2
A(l)+H2O2(l) ��H2
����A��BΪ�л������Ӧ��Ϊ�Է���Ӧ����H2(g)+O2(g) ![]() H2O2(l)�Ħ�H 0(�>������<����=��)��
H2O2(l)�Ħ�H 0(�>������<����=��)��
��3���ں��º��ݵ��ܱ������У�ij���ⷴӦ��MHx(s)+yH2(g)![]() MHx+2y(s) ��H<0�ﵽ��ѧƽ�⡣�����й�������ȷ���� ��
MHx+2y(s) ��H<0�ﵽ��ѧƽ�⡣�����й�������ȷ���� ��
a������������ѹǿ���ֲ���
b������y mol H2ֻ��1 mol MHx
c�������£��÷�Ӧ��ƽ�ⳣ������
d������������ͨ��������������v(����)>v(����)
��4������̫����ֱ�ӷֽ�ˮ���⣬�����������������;����������ת����ʽΪ ��
��5�����������ĸ�����Ҳ����������Դ����ⷨ��ȡ�й㷺��;��Na2FeO4��ͬʱ���������Fe+2H2O+2OH![]()
![]() +3H2��������ԭ����ͼ1��ʾ��װ��ͨ������缫���������Ϻ�ɫ
+3H2��������ԭ����ͼ1��ʾ��װ��ͨ������缫���������Ϻ�ɫ![]() �����缫�����ݲ�����������������ҺŨ�ȹ��ߣ����缫����������ɫ���ʡ���֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ��
�����缫�����ݲ�����������������ҺŨ�ȹ��ߣ����缫����������ɫ���ʡ���֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ��

�����һ��ʱ���c(OH)���͵������� (������ҡ��������ҡ�)��
���������У��뽫�������������弰ʱ�ų�����ԭ��Ϊ ��
��c(Na2FeO4)���ʼc(NaOH)�ı仯��ͼ2����ѡM��N�����е�һ�㣬����c(Na2FeO4)�������ֵ��ԭ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com