
【题目】导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质A可以是__(填序号)。
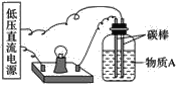
①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是__(填字母)。
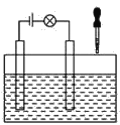
A.盐酸中逐滴加入食盐溶液 B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸 D.硫酸中逐滴加入氢氧化钡溶液
(3)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。若在(2)题图中,电解质溶液为Ca(OH)2溶液,向溶液中逐渐通入CO2。则:下列四个图中,__(填字母)能比较准确地反映出溶液的导电能力和通入CO2气体量的关系(x轴表示CO2通入的量,y轴表示导电能力)。
A.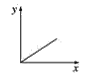 B.
B.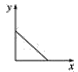 C.
C.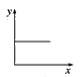 D.
D.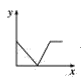
【答案】⑤⑥⑦⑧ D D
【解析】
(1)电解质溶液导电性与离子浓度成正比、与离子电荷成正比,若灯泡亮,说明广口瓶中电解质溶液中含有大量自由移动离子;
(2)溶液导电性强弱由离子浓度大小及所带电荷数多少等因素决定,实验时灯泡能出现由亮-暗-熄灭-亮,说明在滴加溶液过程中导致离子浓度减小,最终为0,再继续滴加溶液,离子浓度逐渐增大;
(3)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水,若在Ca(OH)2溶液中逐渐通入CO2,溶液中离子浓度先减小到几乎为零,后又逐渐增大,据此分解答。
(1)若灯泡亮,则广口瓶内的物质A含有大量自由移动的离子,氯化钠、氢氧化钠晶体虽由离子构成,但离子不能自由移动,所以不导电,两者溶于水后,在水分子的作用下,离解成自由移动的阴、阳离子(实为水合离子),所以二者的水溶液能导电;蔗糖晶体和酒精均由分子构成,不能导电,其水溶液也不导电;稀盐酸、硫酸铜溶液中均含有大量自由移动的离子,可以导电;综上所述,⑤⑥⑦⑧可以导电;故答案为:⑤⑥⑦⑧;
(2)溶液能否导电,取决于溶液中是否有自由移动的离子存在;导电性强弱则由离子浓度大小及所带电荷数多少等因素决定,
A. 盐酸中逐滴加入食盐溶液,不发生反应,混合后仍为强电解质溶液,溶液存在大量自由移动的离子,可导电,不会熄灭,故A不符合;
B. 硫酸中逐滴加入氢氧化钠溶液生成硫酸钠,仍为强电解质溶液,溶液存在大量自由移动的离子,可导电,不会熄灭,故B不符合;
C. 石灰乳中滴加稀盐酸,石灰乳中Ca(OH)2溶解度小,加稀盐酸生成了可溶性的CaCl2,导电能力增强,灯泡变亮,故C不符合;
D. 发生反应H2SO4+Ba(OH)2===BaSO4↓+2H2O,溶液中离子浓度减小,恰好完全反应时,溶液中几乎没有离子,灯泡熄灭,继续滴加Ba(OH)2溶液,Ba(OH)2过量,溶液中Ba2+、OH-数目增多,灯泡逐渐变亮,故D符合;故答案为:D;
(3)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水,若在Ca(OH)2溶液中逐渐通入CO2,先发生反应CO2+Ca(OH)2=CaCO3↓+H2O,溶液中自由移动的离子的浓度逐渐减小,所以一开始导电能力逐渐下降,当开始发生反应CaCO3+CO2+H2O=Ca(HCO3)2,随着反应的进行,离子浓度又逐渐增大,导电能力又逐渐增大,故D符合;故答案为:D。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150 mL 4 mol·L-1的稀硝酸恰好使混合物完全溶解,放出2.24 L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为( )
A. 0.21 mol B. 0.25 mol C. 0.3 mol D. 0.35 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol白磷(P4,s)和4mol红磷(P,s)与氧气反应过程中的能量变化如图(E表示能量)。下列说法正确的是( )
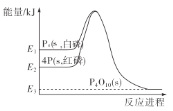
A. P4(s,白磷)=4P(s,红磷) ΔH>0
B. 以上变化中,白磷和红磷所需活化能相等
C. 白磷比红磷稳定
D. 红磷燃烧的热化学方程式是4P(s,红磷)+5O2(g)=P4O10(s) ΔH=-(E2-E3)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素B是第三周期的主族元素,B在周期表中与邻近的元素A、C、D、E的位置如图所示,已知该五种元素的核电荷数之和为85,回答下列问题:
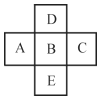
(1)B元素的原子序数是_____,原子结构示意图是_____。
(2)A、B、C三种元素的非金属性由强到弱的顺序是_____,它们的最高价氧化物的水化物的酸性由弱到强的顺序是_____。(用化学式表示)
(3)B、D、E三种元素的非金属性由强到弱的顺序是_____,它们的氢化物的还原性由弱到强的顺序是_____(用化学式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 3 个体积均为 2.0 L 的恒容密闭容器中,反应H2O(g) + C(s)![]() CO(g) + H2(g) ΔH > 0分别在一定温度下达到化学平衡状态。下列说法正确的是
CO(g) + H2(g) ΔH > 0分别在一定温度下达到化学平衡状态。下列说法正确的是
容器 | 温度 (T1>T2) | 起始时物质的量/mol | 平衡时物质的量/mol | |||
n(H2O) | n(C) | n(CO) | n(H2) | n(CO) | ||
I | T1 | 0.5 | 1 | 0 | 0 | 0.25 |
II | T1 | 1 | 1 | 0 | 0 | x |
III | T2 | 0 | 0 | 0.5 | 0.5 | y |
A.当温度为 T1时,该反应的化学平衡常数值为 0.25
B.若 5min 后容器 I 中达到平衡,则 5min 内的平均反应速率:v(H2) = 0.05mol·L-1·min-1
C.达到平衡时,容器 II 中H2O的转化率比容器 I 中的小
D.达到平衡时,容器 III 中的 CO 的转化率小于 50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2(g)+3H2(g)![]() 2NH3 (g) △H<0,在某一时间段中反应速率与反应过程的曲线关系如图,t1、t3、t4时刻外界条件有所改变。下列说法正确的是( )
2NH3 (g) △H<0,在某一时间段中反应速率与反应过程的曲线关系如图,t1、t3、t4时刻外界条件有所改变。下列说法正确的是( )

A. t5~t6时氨气的体积分数最大 B. t3时升高了温度
C. t1时加入催化剂 D. t4时减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸被认为是理想的氢能载体,我国科技工作者运用DFT计算研究单分子HCOOH在催化剂表面分解产生H2的反应历程如图所示,其中吸附在催化剂表面的物种用*标注
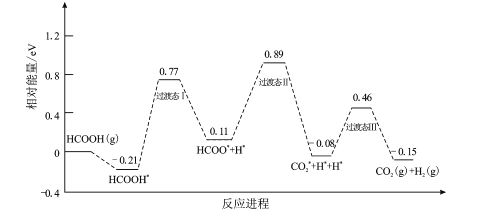
回答下列问题:
(1)该历程中决速步骤的能垒(活化能)E正=__________eV,该步骤的反应方程式为__________
(2)甲酸分解制氢气的热化学方程式为__________
(3)在温度为383K压强为p0时,将一定量的HCOOH气体充入一个盛有催化剂的刚性容器中,达到平衡时,H2的分压为0.55p0,则该反应α(HCOOH)=______________,该温度下的压强平衡常数Kp=__________ (计算结果保留2位有效数字)
(4)HCOOH的分解存在副反应HCOOH(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
已知H2的选择性=![]() 能够增大H2选择性的可能方法是____
能够增大H2选择性的可能方法是____
(5)甲酸作为直接燃料电池的燃料具有能量密度高的优点若电解质溶液显酸性,甲酸直接燃料电池的负极反应式为__________,该电池的理论输出电压为1.48V,能量密度E=________kW·h/kg(能量密度=电池输出电能/燃料质量,1kW·h=3.6×106J)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断中,正确的是( )
A.泡沫灭火器的灭火原理:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
B.将CH3COONa溶液从20℃升温至30℃,溶液中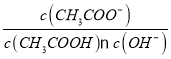 增大
增大
C.某物质的溶液中由水电离出的c(H+)= 1×10-a mol/L,若a>7时,则该溶液的pH一定为14-a
D.已知25℃时NH4CN显碱性,则25℃时的电离常数K(NH3·H2O)>K(HCN)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com