
����Ŀ��I��ij��ѧ��ȤС����ʵ����������װ���Ʊ�������

��ش�
��1��д��Aװ������ȡ�����Ļ�ѧ����ʽ____________________��
��2����Ҫ�Ʊ����������������������A��B֮�����Ӿ���װ��D��E�����е������ӵ�˳����____________________ (��д���ֱ��)��
II��ij��ѧʵ���Ҳ����ķ�Һ�к���Fe3+��Cu2+��Ag+���ֽ������ӣ�ʵ��������˷����Է�Һ�����������������������ս�����

��ش�
��1���������еõ��ij������еĽ���������__________��
��2���������ǽ�Fe2+ת��ΪFe3+��������ѡ�õ��Լ���_____��
A��Fe�� B��NaOH��Һ C��������ˮ D��ϡ����
��3���������м��백ˮ���ɺ��ɫ���������ӷ���ʽΪ___________________��
���𰸡�MnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O �ۢܢڢ� Ag��Cu��Fe C Fe3+��3NH3��H2O��Fe(OH)3����3NH4+
MnCl2��Cl2����2H2O �ۢܢڢ� Ag��Cu��Fe C Fe3+��3NH3��H2O��Fe(OH)3����3NH4+
��������
����������ʵ�����Ʒ��������仯��������ʽ��
I��(1)װ��A��MnO2��ŨHCl������ȡ�����Ļ�ѧ����ʽMnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O��
MnCl2��Cl2����2H2O��
(2)���������к�HCl��H2O(g)���ʣ��Ʊ��������������������A��B֮�����ñ���ʳ��ˮ��ȥHCl������Ũ������װ��D��E�ĵ�������˳�����ۢܢڢ١�
II��(1)�����������û���Ӧ����Ag��Cu�������۹�������Feʣ����
(2)��������Fe2+ת��ΪFe3+��Ӧʹ����������ֻ��������ˮ������
(3)����������İ�ˮ����Fe3+ת��Ϊ���ɫFe(OH)3���������ӷ���ʽFe3+��3NH3��H2O��Fe(OH)3����3NH4+��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС�����ʵ�飺�������ữ�Ĺ���������Һ�м���⻯�ء����ۺ���������ƵĻ����Һ��һ��ʱ�����Һ��������������֪��ϵ�д���������Ҫ��Ӧ��
��Ӧi��H2O2(aq) + 2I��(aq) + 2H+(aq) I2(aq) + 2H2O(l) ��H1 = -247.5 kJ/mol
��Ӧii��I2(aq) + 2S2O32-(aq) 2I��(aq) + S4O62-(aq) ��H2 = -1021.6 kJ/mol
��1��H2O2��S2O32-��Ӧ���Ȼ�ѧ����ʽΪ______��
��2������ʵ�鷽����֤ʵ������Ӧ���̡���ʵ�鷽�����������������Լ�Ũ�Ⱦ�Ϊ0.01 mol/L����
a�����ữ��H2O2��Һ�м���________��Һ����Һ������Ϊ��ɫ��
b��_________����Һ������ɫ��
��3��̽��c(H+)�Է�Ӧ���ʵ�Ӱ�죬ʵ�鷽�����±���ʾ���������Լ���H2O���⣬Ũ�Ⱦ�Ϊ0.01 mol/L��
ʵ����� | a | b | |
�� �� | H2O2/mL | 5 | ______ |
H2SO4/mL | 4 | 2 | |
Na2S2O3/mL | 8 | _____ | |
KI�������ۣ�/mL | 3 | _____ | |
H2O | 0 | ______ | |
��������ҺѸ�ٻ�� �۲����� | ��Һ��������ʱ�� Ϊt1�� | ��Һ��������ʱ�� Ϊt2�� | |
�� ��ʵ��b����������
�� �Ա�ʵ��a��ʵ��b��t1_____t2������>������<������
�� ��ϣ�2�������������Һ��Ϻ�һ��ʱ��ű�����ԭ��________��
�� ����ʵ��a�����ݣ�����t1ʱ����H2O2��S2O32-��Ӧ��ƽ����Ӧ���ʣ���H2O2Ũ�ȵı仯��ʾ��________mol/(L��s)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С����ϳɳ��ݼ������ɺ�Ⱦ���м���X��
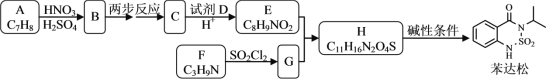
��֪��Ϣ����![]() ��RCOOR��
��RCOOR��![]()
![]()
��RCH2COOR����R���COOR����![]()
![]()
(1)����˵����ȷ����________��
A��������B��C��ת���漰��ȡ����Ӧ
B��������C��������
C���Լ�D�����Ǽ״�
D�������ɵķ���ʽ��C10H10N2O3S
(2)������F�Ľṹ��ʽ��________��
(3)д��E��G��H�Ļ�ѧ����ʽ________��
(4)д��C6H13NO2ͬʱ��������������ͬ���칹��Ľṹ��ʽ________��
�ٷ�������һ����Ԫ�����ҳɻ�ԭ������ຬ2����̼ԭ�ӣ�
��1HNMR��IR��������������4�ֻ�ѧ������ͬ����ԭ�ӡ���N��O����û�й�����(��O��O��)��
(5)�����CH3CH2OH�� ԭ���Ʊ�X(
ԭ���Ʊ�X( )�ĺϳ�·��(���Լ���ѡ���ϳ������õ������٢�������֪��Ϣ��������ͼ��ʾ)________��
)�ĺϳ�·��(���Լ���ѡ���ϳ������õ������٢�������֪��Ϣ��������ͼ��ʾ)________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ǿ�������������Ƕ��ѧ�ڻ������������Ͽ�ѧ�������о�����Ҫ���⡣��ͼΪ����HCl���������253 K�������������ܽ���̵�ʾ��ͼ�����������������

A. �������һ���У�HCl�Է�����ʽ����
B. ������ڶ����У�H+Ũ��Ϊ5��103 mol��L1��������ܶ�Ϊ0.9 g��cm3��
C. ������������У������������ṹ���ֲ���
D. ���������֮�䣬�����ڿ��淴ӦHCl![]() H++Cl
H++Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��е��١�������Ԫ�أ���д���пհף�

��1������ЩԪ���У���λ��Ԫ�����ڱ��ĵ�______�������������γɵĵ���ɫ�Ĺ�������������ӵĸ�����Ϊ_______��
��2���õ���ʽ��ʾԪ���������Ļ�������γɹ���__________________________
��3��Ԫ�����ļ��⻯�ﳣ���º�Ԫ�����ĵ��ʷ�Ӧ�����ӷ���ʽΪ__________________��
��4���ܢݢޢ��ļ����Ӱ뾶��С����Ϊ___________________������Ԫ�ط��ű�ʾ��
��5��Ԫ������Ԫ������ȣ���֤��������Ԫ�طǽ�����ǿ������ʵ��_______����ѡ����ţ���
A�����������ĵ��ʺ����ĵ���״̬��ͬ
B�����ļ��⻯������ļ��⻯���ȶ�
C�����ļ��⻯��ķе�����ļ��⻯��ķе��
D�����ĵ����������ļ��⻯�ﷴӦ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A������ʯ�͵���Ҫ�л�����ԭ�ϣ������ʿ�����������һ������ʯ�ͻ�����չˮƽ��E�Ǿ��й���ζ���л��F��һ�ָ߾�����Ƴɶ��ְ�װ���ϡ�

��1��F�Ľṹ��ʽΪ__________��C������Ϊ__________��
��2��ʹ1molA������������ȫ�ӳɷ�Ӧ��Ȼ��ʹ�üӳɷ�Ӧ�IJ����������ڹ��յ������·�����ȫȡ����Ӧ�����������������ĵ��������ܵ����ʵ�����_______mol��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��
��__________________________________________________________��
��__________________________________________________________��
��__________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�������к͵ζ�ʵ���˵����ȷ����

A. ��ͼB�ĵζ��ܿ�ȷ��ȡ25.00 mL������KMnO4��Һ
B. �ζ������У��۾�Ҫʱ��ע�ӵζ�����Һ��ı仯
C. �ζ���װ��Һ��ǰ�����ô�װҺ��ϴ
D. �ζ�ǰƽ�ӣ��ζ����������Ӷ�������ʹ�ⶨ���ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ�����й��������ἰ�����ε�˵������ȷ����
A. Na2SO3��Һ�� NaHSO3��Һ�к��е�����������ȫ��ͬ
B. pH=3�� NaHSO3��Һϡ�ͺ���Һ�и�����Ũ�Ⱦ���С
C. H2SO3��Һ��c(H��)��c(SO32��)/c(H2SO3)��С�����ܵĴ�ʩ�Ǽ���NaHSO4����
D. ��0.1 mol/L NaHSO3��Һ��pH=2����0.1 mol/L H2SO3��Һ��c(H+)һ��С��0.11 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ�У�ʵ�ʲμӷ�Ӧ���������뻹ԭ�������ʵ���֮����ȷ����(����)
��KClO3��6HCl(Ũ)=KCl��3Cl2����3H2O��1��6
��3Cu��8HNO3(ϡ)=3Cu(NO3)2��2NO����4H2O��2��3
��SiO2��3C![]() SiC��2CO����1��2
SiC��2CO����1��2
��3NO2��H2O=2HNO3��NO��2��1
A.�٢�B.�ڢ�
C.�ڢ�D.�٢�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com