
【题目】2000年诺贝尔化学奖授予两位美国化学家和一位日本化学家,以表彰他们在导电塑料领域的贡献,他们首先把聚乙炔树脂制成导电塑料。下列关于聚乙炔叙述错误的是( )
A. 聚乙炔是以乙炔为单体发生加聚反应形成的高聚物
B. 聚乙炔的化学式为![]() ,分子中所有碳原子在同一直线上
,分子中所有碳原子在同一直线上
C. 聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质
D. 聚乙炔树脂自身不导电
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】用现有三组溶液:①汽油和氯化钠溶液②汽油和柴油的混合物③从氯化钠和单质碘的水溶液中分离出碘,分离以上物质正确方法依次是( )
A.分液、蒸馏、萃取B.萃取、蒸发、分液
C.分液、萃取、蒸馏D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A~J在周期表中的位置,用元素符号或化学式回答下列问题:

(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的元素是________。(填元素符号)
(2)最高价氧化物的水化物中酸性最强的是________,呈两性的是________。
(3)在B、C、E、F中,原子半径最大的是________。
(4)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:________。
(5)与C元素同族的第5周期元素X的价电子排布式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r溶液为强电解质溶液,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )

A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。已知:硫酰氯通常条件下为无色液体,熔点54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =97.3 kJ·mol1,实验装置如图所示(部分夹持装置未画出)。
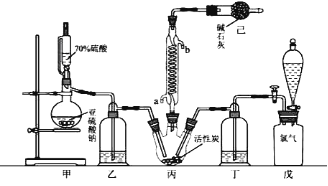
回答下列问题:
(1)装置己的作用是_________________________________________________;如何控制两种反应物体积相等:__________________________________________________。
(2)装置戊上方分液漏斗中最好选用下列试剂:_____(选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 molL1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫会发生副反应,化学方程式是________________________________________________________;同时生成的SO2Cl2也会水解而“发烟”,该反应的化学方程式为______________________________________
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有(填序号)______。
①控制气流速率,宜慢不宜快 ②持续加热丙装置
③若丙装置发烫,可适当降温 ④先通冷凝水,再通气
(5)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H![]() SO2Cl2 + H2SO4,分离两种产物的方法是__________(选填字母)。
SO2Cl2 + H2SO4,分离两种产物的方法是__________(选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
请设计实验方案检验产物中存在硫酸(可选试剂:稀盐酸、稀硝酸、氯化钡溶液、蒸馏水、石蕊试液)_______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 (2﹣羟基﹣4﹣苯基丁酸乙酯)是某药物的中闻体,常温下是一种无色透明的油状液体,沸点为212℃.某同学设计实验制备该物质:原料:
(2﹣羟基﹣4﹣苯基丁酸乙酯)是某药物的中闻体,常温下是一种无色透明的油状液体,沸点为212℃.某同学设计实验制备该物质:原料:  (2﹣羟基﹣4﹣苯基丁酸)和乙醇 实验装置:
(2﹣羟基﹣4﹣苯基丁酸)和乙醇 实验装置:
实验步骤:
①按如图1装置连接仪器.
②20mL 2﹣羟基﹣4﹣苯基丁酸于三颈瓶中,加入适量浓硫酸和20mL无水乙醇,加入几块沸石.
③加热至70℃左右保持恒温半小时.
④分离、提纯三颈瓶中粗产品,得到有机产品.
⑤精制产品.
请回答下列问题:
(1)加入原料时,能否最先加入浓硫酸?(填“能”或“否”).油水分离器的作用是 .
(2)本实验的加热方式宜用(填“直接加热”或“水浴加热”).如果温度过高,或浓硫酸的量过多,制备产率会(填“增大”、“减小”或“不变”).
(3)写出制备反应的化学方程式: .
(4)分离提纯产品:取三颈瓶中混合物加入足量的饱和碳酸钠溶液,分液得到有机层.饱和碳酸钠溶液的作用是 . ①吸收过量的乙醇 ②除去过量的有机酸 ③促进产品水解 ④降低产品在水中溶解度
(5)产品精制:精制产品的实验装置如图2所示,试分析装置是否合理,若不合理将如何改进: . (若装置合理,此空不作答).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下面的短文,回答问题。
聚碳酸酯(PC)是一类碳酸的聚酯,是一种强韧的热塑性树脂,耐弱酸,耐弱碱,耐中性油,不耐强碱,有阻燃性。其光学性能接近有机玻璃(  ),在透明建筑板材、电子电器、光盘媒介、汽车工业等领域有广泛应用。碳酸本身并不稳定,但其衍生物,如碳酸二苯酚酯、光气等有一定稳定性。工业上以碳酸的衍生物和双酚A为原料合成聚碳酸酯(PC),反应如下:
),在透明建筑板材、电子电器、光盘媒介、汽车工业等领域有广泛应用。碳酸本身并不稳定,但其衍生物,如碳酸二苯酚酯、光气等有一定稳定性。工业上以碳酸的衍生物和双酚A为原料合成聚碳酸酯(PC),反应如下:
(1)下列说法正确的是(填序号)。
a.光气比碳酸稳定
b.聚碳酸酯能和强碱发生反应
c.聚碳酸酯易燃
d.聚碳酸酯是一种强韧的热塑性树脂
(2)双酚A和光气(  )也可发生类似的缩聚反应,生成一种聚碳酸酯。该反应的化学方程式是。
)也可发生类似的缩聚反应,生成一种聚碳酸酯。该反应的化学方程式是。
(3)有机玻璃的单体的结构简式是。在一定条件下,有机玻璃和NaOH溶液能发生反应,该反应的化学方程式是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com