
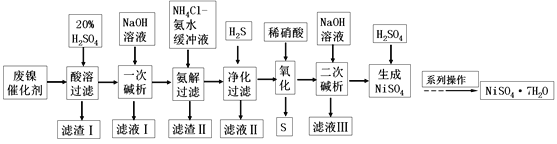
【题目】硫酸镍是一种重要的化工中间体,是镍行业研究的热点。一种以石油化工中废镍催化剂(主要成分为NiCO3和SiO2,含少量Fe2O3、Cr2O3)为原料制备硫酸镍的工业流程如图:
已知:①NiS、Ni(OH)2、Cr(OH)3均难溶于水,Cr(OH)3是两性氢氧化物。
②Fe(OH)3不溶于NH4Cl-氨水的混合液,Ni(OH)2溶于NH4Cl-氨水的混合液生成[Ni(NH3)6]2+。
请回答下列问题:
(1)“酸溶”时为了提高浸取率,可采取的措施有________(任写出一条)。
(2)“滤渣I”的主要成分是_________。
(3)“一次碱析”时,加入的NaOH溶液需过量,则含铬微粒发生反应的离子方程式为__________。
(4)“氨解”的目的为___,“净化”时加入的H2S的目的是将镍元素转化为____沉淀。
(5)“氧化”时发生反应的离子方程为________。
(6)“二次碱析”时,若使溶液中的Ni2+沉淀完全(离子浓度≤10-5mol·L-1时,离子沉淀完全),则需维持c(OH-)不低于_______(已知Ni(OH)2的Ksp=2×10-15,![]() ≈1.4)。
≈1.4)。
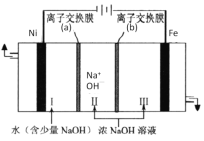
(7)以Fe、Ni为电极制取Na2FeO4的原理如图所示。通电后,在铁电极附近生成紫红色的FeO42-。电解时阳极的电极反应式为________,离子交换膜(b)为__________(填“阴”或“阳”)离子交换膜。
【答案】升高温度、将废镍催化剂粉碎、搅拌等 SiO2 Cr3++4OH-=CrO2-+2H2O 除去Fe3+ NiS 3NiS+8H++2NO3-=3Ni2++2NO↑+3S↓+4H2O 1.4×10-5mol/L Fe-6e-+8OH-=FeO42-+4H2O 阴
【解析】
废镍催化剂(主要成分为NiCO3和SiO2,含少量Fe2O3、Cr2O3)为原料制备硫酸镍,加入20%的硫酸酸溶,NiCO3、Fe2O3、Cr2O3反应进入溶液中,SiO2不能反应,过滤,滤渣Ⅰ为SiO2,滤液加入NaOH溶液进行一次碱析,滤液Ⅰ含有CrO2-,沉淀加入氯化铵、氨水缓冲液,由信息②可知滤渣Ⅱ为Fe(OH)3,过滤得到的滤液含有[Ni(NH3)6]2+,“净化”时通入的H2S,可以将镍元素转化为NiS沉淀,加入硝酸氧化,可生成S和Ni2+,加入氢氧化钠生成Ni(OH)2,过滤后加入硫酸可得到硫酸镍,经蒸发浓缩、冷却结晶得到硫酸镍晶体,以此解答该题。
(1)“酸溶”时为了提高浸取率,可以先将废镍催化剂粉碎,以增大固体表面积,或进行搅拌,并在加热条件下使废镍催化剂与20%硫酸充分反应等;
(2)“滤渣Ⅰ”主要成分为二氧化硅;
(3)Cr(OH)3难溶于水,Cr(OH)3是两性氢氧化物,可以与过量的NaOH溶液发生反应产生CrO2-,则含铬微粒发生反应的离子方程式为Cr3++4OH-=CrO2-+2H2O;
(4)加入氯化铵和氨水的缓冲液,可生成Fe(OH)3沉淀,同时生成[Ni(NH3)6]2+,达到除去Fe3+的目的;“净化”时通入的H2S的目的是将镍元素转化为NiS沉淀,对应的离子方程式为[Ni[Ni(NH3)6]2++H2S=NiS↓+2NH4++4NH3↑;
(5)“氧化”时HNO3将NiS氧化为S单质,HNO3被还原为NO,发生反应的离子方程式为3NiS+8H++2NO3-=3Ni2++2NO↑+3S↓+4H2O,从而可除去硫,生成镍离子;
(6)离子浓度≤1×10-5mol/L时,离子沉淀完全,已知Ni(OH)2的Ksp=2×10-15,则c(OH-)=![]() mol/L=1.4×10-5mol/L;
mol/L=1.4×10-5mol/L;
(7)电解池中阳极发生氧化反应,依据题意可知铁在阳极失去电子,碱性环境下生成高铁酸根离子FeO42-,阳极的电极反应式为:Fe-6e-+8OH-=FeO42-+4H2O,离子交换膜(b)为阴离子交换膜,可使氢氧根离子进入阳极区。


科目:高中化学 来源: 题型:
【题目】中华优秀传统文化涉及到很多的化学知识,下列有关说法错误的是
A.“日照澄洲江雾开”中伴有丁达尔效应
B.古剑“沈卢”以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
C.“粉身碎骨浑不怕,要留清白在人间”指的是物质发生了物理变化
D.“煤饼烧蛎房成灰![]() 蛎房即牡蛎壳
蛎房即牡蛎壳![]() ”中灰的主要成分为碳酸钙
”中灰的主要成分为碳酸钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化对人类文明贡献巨大,古代文献中记载了古代化学研究成果。下列叙述不正确的是
A.![]() 本草纲目
本草纲目![]() 中有“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”的记载,“浣衣”过程中涉及水解反应
中有“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”的记载,“浣衣”过程中涉及水解反应
B.![]() 本草衍义
本草衍义![]() 中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是干馏
中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是干馏
C.![]() 梦溪笔谈
梦溪笔谈![]() 中对宝剑的记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折”,“剂钢”指的是铁合金,硬度比纯铁大
中对宝剑的记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折”,“剂钢”指的是铁合金,硬度比纯铁大
D.![]() 淮南万毕术
淮南万毕术![]() 对湿法冶金术的记载:“曾青得铁则化为铜”,文中涉及置换反应
对湿法冶金术的记载:“曾青得铁则化为铜”,文中涉及置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)石油和煤是重要的能源物质,下列说法错误的是___。
a.石油和煤是不可再生能源
b.煤为混合物,含有苯、甲苯、二甲苯等有机物
c.煤的干馏和石油的分馏都是物理变化
d.煤燃烧及汽车尾气是造成空气污染的重要原因
e.以煤、石油为原料可生产塑料、合成橡胶、合成纤维等合成材料
(2)以煤为原料经过一系列反应可生产乙酸乙酯,其合成路线如下:
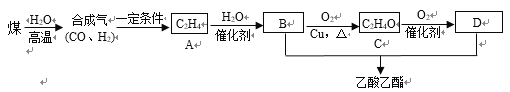
①C的名称是______;A→B的反应类型是_______。
②决定化合物B性质的基团名称是_________。
③B→C的化学方程式为_______________________________。
B+D→乙酸乙酯的化学方程式为________________________________。
(3)某化学实验小组的同学,采用如图装置制取乙酸乙酯。

①仪器B的名称是_______;仪器A中冷却水的进口是_____(填“a”或“b”)。
②观察仪器A的内层结构,与长直导管相比较,该反应装置的优点是_______。
③将乙醇和乙酸按照物质的量3∶2混合得到258g混合液,在浓硫酸作用下发生反应,乙酸乙酯的产率为50%,则生成的乙酸乙酯的质量是_______g。(相对分子质量:乙醇—46,乙酸—60,乙酸乙酯—88)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾溶液中存在如下平衡:(1)Cr2O72-+H2O![]() 2H++2CrO42-,向2mL0.1mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,发生反应:Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O。下列分析正确的是
2H++2CrO42-,向2mL0.1mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,发生反应:Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O。下列分析正确的是
A. 向K2Cr2O7溶液加入几滴浓NaOH溶液,溶液由黄色变成橙黄
B. 氧化性:Cr2O72->Fe3+
C. CrO42-和Fe2+在酸性溶液中能大量共存
D. 向K2Cr2O7溶液中加水稀释,反应(1)平衡向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以某含镍废料(主要成分为NiO,还含有少量FeO、Fe2O3、CoO、SiO2)为原料制备NixOy和碳酸钴的工艺流程如下:
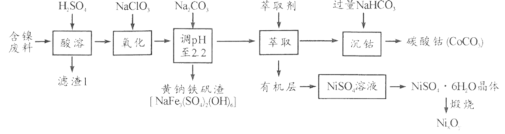
(1)“酸溶”时需将含镍废料粉碎,目的是_________________________________;“滤渣Ⅰ”主要成分为____________________(填化学式)。
(2)“氧化”中添加NaClO3的作用是_______________________,为证明添加NaClO3已足量,可用_______________(写化学式)溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,其离子方程式为__________________。
(4)“沉钴”过程的离子方程式________________________。若“沉钴”开始时c(Co2+)=0.10 mol/L,则控制pH≤_____________时不会产生Co(OH)2沉淀。(已知Ksp[Co(OH)2]=4.0×10-15,lg2=0.3)
(5)从NiSO4溶液获得NiSO4·6H2O晶体的操作依次是:加热浓缩溶液至有晶膜出现,______________,过滤,洗涤,干燥。“煅烧”时剩余固体质量与温度变化曲线如图,该曲线中B段所表示氧化物的化学式为__________________。
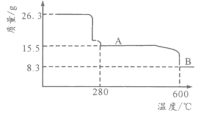
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂用闪锌矿制备锌及颜料 A(红棕色固体)的工艺流程如下图所示。(闪锌矿的主要成分为 ZnS,同时含有 10%的 FeS 及少量 CuS)
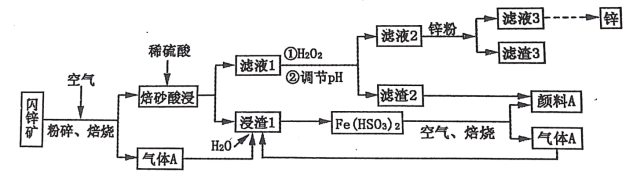
已知:①闪锌矿在焙烧时会生成副产物 ZnFeO4,ZnFeO4 不溶于水及硫酸。Fe(HSO3)2 难溶于水。②Ksp[Fe(OH)3]=1×10-39。
完成下列问题
(1)闪锌矿粉碎的目的是_______________________________________________________。
(2)“滤液 1”中选用足量的 H2O2,理由是_____________________。假设“②调节 pH"前,滤液 1 中 c(Fe3+)=1molL-1 ,则 Fe3+ 完全沉淀时的 pH 至少为____________________。(离子浓度≤ 10-6mol·L-1 规为完全除去)。
(3)“滤渣 3”的成分为__________________________________ (写化学式)。
(4)设计一种检验“颜料 A”中是否含有 Fe2+的实验方案_______________________________________________________。
(5)“气体 A”与“浸渣 1”反应的化学方程式为_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以煤为主要原料可以制备乙二醇,相关工艺流程如下:
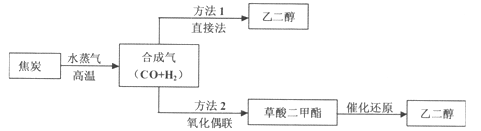
(1)写出方法l在催化剂的条件下直接制取乙二醇的化学方程式_______
(2)合成气在不同催化剂作用下,可以合成不同的物质。下列物质仅用合成气为原料就能得到且原子利用率为100%的是_____填字母)。
A.草酸( HOOC-COOH) B.甲醇(CH3OH) C.尿素[CO(NH2)2]
(3)工业上还可以利用天然气(主要成份为CH4)与C02反应制备合成气。已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ/mol
2H2(g)+ O2(g)= 2H2O(l) △H=-571.6kJ/mol
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
则CH4与CO2生成合成气的热化学方程式为____________________。
(4)方法2:在恒容密闭容器中投入草酸二甲酯和H2发生如下反应:
CH3OOC—COOCH3(g)+ 4H2(g)![]() HOCH2CH2OH(g)+2CH3OH(g)△H=-34kJ/mol
HOCH2CH2OH(g)+2CH3OH(g)△H=-34kJ/mol
为提高乙二醇的产量和速率,宜采用的措施是___________(填字母)。
A.升高温度 B.增大压强 C.增大氢气浓度
(5)草酸二甲酯水解生成草酸:CH3OOC—COOCH3+ 2H2O![]() HOOC—COOH+2CH3OH
HOOC—COOH+2CH3OH
①草酸是二元弱酸,可以制备![]() (草酸氢钾),
(草酸氢钾),![]() 溶液呈酸性,用化学平衡原理解释:__________________。
溶液呈酸性,用化学平衡原理解释:__________________。
②在一定的![]() 溶液中滴加NaOH溶液至中性。下列关系一定不正确的是_______(填字母)。
溶液中滴加NaOH溶液至中性。下列关系一定不正确的是_______(填字母)。
A.![]()
B.![]()
C.![]()
(6)乙二醇、空气在KOH溶液中构成燃料电池,加入乙二醇的电极为电源的_____填“正”或“负”)极,负极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。
请回答以下问题:
⑴ 该结晶水合物中含有的两种阳离子是________和________,阴离子是_________。
⑵ 试通过计算确定该结晶水合物的化学式。________
⑶ 假设过程中向该溶液中加入的NaOH溶液的物质的量浓度为5mol·L-1,请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系________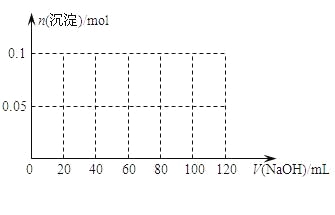
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com