
【题目】氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料。
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2![]() 2NH3。该可逆反应达到平衡的标志是________________。
2NH3。该可逆反应达到平衡的标志是________________。
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时消耗3m mol H2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间变化
E.a molN≡N键断裂的同时,有6amolN—H键断裂
F.N2、H2、NH3的分子数之比为1∶3∶2
(2)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入1molN2和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则从反应开始到25min时,以N2表示的平均反应速率= ;该温度下平衡常数K= ;
(3) 利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H=-99kJ·mol-1
CH3OH(g) △H=-99kJ·mol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-58 kJ·mol-1
CH3OH(g)+H2O(g) △H=-58 kJ·mol-1
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H
CO(g)+H2O(g) △H
图1中能正确反映平衡常数K随温度变化关系的曲线是 ;反应③的△H= kJ·mol-1。
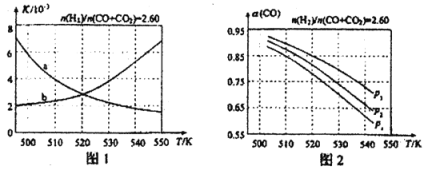
(4)合成气的组成n(2)/n(CO+CO2)=2.60时体系中的CO平衡转化率α(CO)与温度和压强的关系如图2所示。图中的压强p1、p2、p3由大到小的顺序为 ;α(CO)随温度升高而减小,其原因是 。
【答案】(1)BCE (2)0.01 mol/(L.min) 2.37( mol/L)-2
(3)a(2分) +41 (2分)
(4)p3>p2>p1(2分)反应①为放热反应,升高温度,平衡左移,α(CO)减小;反应③为吸热反应,升高温度,平衡右移,α(CO)也减小(2分)
【解析】
试题分析:(1)A.2v(H2)正=3v(NH3)逆时,该反应达到平衡状态,所以3v(H2)正=2v(NH3)逆时该反应没有达到平衡状态,错误;B.单位时间生成m mol N2的同时消耗3m mol H2,正逆反应速率相等,所以该反应达到平衡状态,正确;C.容器内的总压强不再随时间而变化,反应体系中各物质的浓度不变,所以达到平衡状态,正确;D.无论该反应是否达到平衡状态,混合气体的密度不随时间变化,所以密度不能作为判断依据,错误;E.a molN≡N键断裂的同时,有6amolN-H键断裂,正逆反应速率相等,所以该反应达到平衡状态,正确;F.N2、H2、NH3的分子数之比为1:3:2时该反应不一定达到平衡状态,与反应物的初始浓度及转化率有关,错误;答案选BCE;
(2)同一温度下,容器中气体压强与总的物质的量成正比,设平衡状态时混合气体的物质的量为x,
16.80:12.60=(1+3)mol:x,x=(4mol×12.60)/16.80=3,所以平衡时混合气体的物质的量为3mol,设参加反应的氮气的物质的量为y,则
N2(g)+3H2(g)![]() 2NH3(g) 物质的量减少
2NH3(g) 物质的量减少
1mol 2mol
y (4-3)mol
1mol:2mol=y:(4-3)mol
解得y=0.5mol
则从反应开始到25min时,以N2表示的平均反应速率=![]() =0.01mol/(L·min)
=0.01mol/(L·min)
平衡时,c(N2)=0.5mol÷2L=0.25mol/L、c(H2)=(3mol3×0.5mol)÷2L=0.75mol/L、c(NH3)=(0.5mol×2)÷2L=0.5mol/L,化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,则化学平衡常数K=![]() =2.37。
=2.37。
(3)由于正方应是放热反应,升高温度平衡向逆反应方向移动,平衡常数减小,因此a正确。已知①CO(g)+2H2(g)![]() CH3OH(g) △H=-99kJ·mol-1
CH3OH(g) △H=-99kJ·mol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-58 kJ·mol-1
CH3OH(g)+H2O(g) △H=-58 kJ·mol-1
则根据盖斯定律可知②—①即得到反应③CO2(g)+H2(g)![]() CO(g)+H2O(g)的△H=+41kJ/mol。
CO(g)+H2O(g)的△H=+41kJ/mol。
(4)相同温度下,由于反应①为气体分子数减小的反应,加压有利于提升CO的转化率;而反应③为气体分子数不变的反应,产生CO的量不受压强影响,故增大压强时,有利于CO的转化率升高,所以图2中的压强由大到小为P3>P2>P1;反应①为放热反应,升高温度时,平衡向左移动,使得体系中CO的量增大;反应③为吸热反应,平衡向右移动,又产生CO的量增大;因此最终结果是随温度升高,使CO的转化率降低。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某溶液中可能含有SO42-、 CO32-、Cl-、SO32-。为了检验其中是否含有SO42-,除BaCl2溶液外,还需要的溶液是( )。
A. H2SO4 B. HCl C. NaOH D. HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据π键的成键特征,判断C=C键的键能和C—C键的键能的关系是
A.双键的键能等于单键的键能的2倍B.双键的键能大于单键的键能的2倍
C.双键的键能小于单键的键能的2倍D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两种短周期元素组成的化合物,其中两种元素的原子个数比为1:3,若两种元素的原子序数分别为a和b,则a和b的关系可能是( )
①a=b+4;②a+b=8;③a+b=30;④a=b+8
A. ①②③④ B. ①③④ C. ②④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的气化在煤化工业中占有重要地位,至今仍然是化学工业的重要组成部分。
(1)已知H2(g)、CO(g)和CH3OH(l)的标准燃烧热分别为-285.8 kJ·mol-1、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请写出CH3OH(l)完全燃烧生成二氧化碳和液态水的热化学方程式:________________________________________________________________。
(2)工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)
CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)
温度/℃ | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断ΔH________(填“>”、“=”或“<”)0。
②某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应后,4 min达到平衡时测得c(CO)=0.2 mol·L-1,此时的温度为_____,则反应速率v(H2)=__________。
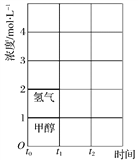
(3)T ℃时,在t0时刻,合成甲醇反应CO(g)+2H2(g)![]() CH3OH(g)达到平衡,若在t1时刻将容器的体积缩小为原来的
CH3OH(g)达到平衡,若在t1时刻将容器的体积缩小为原来的![]() ,在t2时刻又达到新的平衡,请在图中用曲线表示t1~t2时间段氢气、甲醇物质的量浓度随时间变化的趋势示意图(其他条件不变,曲线上必须标明氢气、甲醇)。__________
,在t2时刻又达到新的平衡,请在图中用曲线表示t1~t2时间段氢气、甲醇物质的量浓度随时间变化的趋势示意图(其他条件不变,曲线上必须标明氢气、甲醇)。__________
(4)如果用CH3OH和空气作燃料电池,用KOH作电解质溶液,请写出该燃料电池的负极的电极反应式:_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物转化关系是化学学习的重要内容之一。下列各组物质的转化关系中不全部是通过一步反应完成的是( )。
A. Na→NaOH→Na2CO3→NaCl B. Fe→Fe(NO3)3→Fe(OH)3→Fe2O3
C. Mg→MgCl2→Mg(OH)2→MgSO4 D. Al→Al2O3→Al(OH)3→AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物CH3CH==CH—C≡CH中标有“·”的碳原子的杂化方式依次为
A.sp、sp2、sp3B.sp3、sp、sp2C.sp2、sp、sp3D.sp3、sp2、sp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业是我国化工生产支柱产业。主要生产工艺流程如下:

接触室中的反应为2SO2(g)+O2(g)![]() 2SO3(g) H=197 kJ·mol1。
2SO3(g) H=197 kJ·mol1。
请回答以下几个问题:
(1)图中炉气要净化的原因是_____________________________________。
(2)吸收塔排出的尾气先用足量的氨水吸收,反应的离子方程式为_______________,再用浓硫酸处理,得到较高浓度的SO2和铵盐。所得的SO2可用于工业制溴过程中吸收潮湿空气中的Br2,吸收Br2的过程中主要反应的化学方程式是____________________________________。所得铵盐溶液中各离子物质的量浓度由大到小的顺序为________________________。
(3)为什么从接触室出来的SO3气体不用水直接吸收,而是用98.3%的浓硫酸吸收:____________________。
![]() (4)燃烧1 t含二硫化亚铁90%的黄铁矿,在理论上能生产________t 98%的硫酸(设有1.5%的硫留在炉渣里,精确至0.01),从提高SO3的产率同时适当降低生产成本的角度出发,以下措施可取的是___________(填字母)。
(4)燃烧1 t含二硫化亚铁90%的黄铁矿,在理论上能生产________t 98%的硫酸(设有1.5%的硫留在炉渣里,精确至0.01),从提高SO3的产率同时适当降低生产成本的角度出发,以下措施可取的是___________(填字母)。
A.通入过量的空气 B.使用优质催化剂
C.调整适宜的温度 D.采用高压
(5)科研工作者开发了制备SO2,再用电化学原理生产硫酸的方法,装置如图。为了稳定技术生产,硫酸的浓度应维持不变,则通入的SO2和水的质量比为__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 某有机物由C、H、O三种元素组成,球棍模型如图所示:

(1)该有机物的分子式是_____________;
(2)该有机物可以发生加聚反应,其产物的结构简式是_____________;
(3)下列有关该有机物的描述中,正确的是____(填序号)。
a. 能与NaHCO3溶液反应
b. 能发生水解反应
c. 不能与溴的CCl4溶液反应
d. 能与酸性高锰酸钾溶液反应
II. (1)写出下列化合物的名称或结构简式:
①![]() _______________________________,
_______________________________,
②2,5-二甲基-2,4-己二烯的结构简式:_______________________。
(2)麻黄素又称黄碱,是我国特定的中药材麻黄中所含有的一种生物碱,经我国科学家研究发现其结构如图:

麻黄素中含氧官能团的名称是_________________,属于____________类(填“醇”或“酚”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com