
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��е��١�������Ԫ�أ���д���пհף�
�� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� |
��1������ЩԪ���У���ѧ��������õ���______����Ԫ�ط��ţ�����λ��Ԫ�����ڱ��ĵ�____���С�
��2����ЩԪ�ص�����������ˮ�����У�������ǿ�Ļ�����ĵ���ʽ��___________��
��3�����ĵ��ʱ����ĵ����۵�_______�����������������������ܢݢޢ��ļ����Ӱ뾶��С�����˳��Ϊ___________________������ű�ʾ����
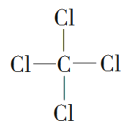
��4���������γɵ�ij�ֻ����ᆳ��������ȡ������ṹʽΪ________���û���������________������������������������������������γɵĵ���ɫ�Ĺ�������������ӵĸ�����Ϊ_______��
��5��Ԫ������Ԫ������ȣ���֤��������Ԫ�طǽ�����ǿ������ʵ��_______����ѡ����ţ���
A�����������ĵ��ʺ����ĵ���״̬��ͬ B�����ļ��⻯������ļ��⻯���ȶ�
C�����⻯��ķе�����>�� D�����ĵ����������ļ��⻯�ﷴӦ���ɢĵ���
���𰸡� Ar 15 ![]() �� ��<��<��<��
�� ��<��<��<��  ���� 1��2 BD
���� 1��2 BD
������������Ԫ�������ڱ��е����λ�������жϳ�Ԫ�����ƣ�Ȼ����Ԫ���������Լ��й����ʵĽṹ�����ʷ������
�ɱ�����Ϣ��֪���٢ڢۢܢݢޢߢ��ֱ����C��N��O��Na��Al��S��Cl��Ar��K��Ԫ�ء���
��1������ЩԪ���У���ѧ��������õ���ϡ������Ԫ��Ar�����ǵ�Ԫ�أ�λ��Ԫ�����ڱ��ĵ�15���С�
��2��������������ˮ�����У�������ǿ�Ļ�������KOH���������Ӽ��ͼ��Լ��������ʽ��![]() ��
��
��3���ƺͼ���ͬһ����Ľ�������۵�������ͬ�������Ӱ뾶��С�����ԣ��ƵĽ�����ǿ�ڼأ����Ƶ��۵�ȼظߣ��ܢݢޢߵļ����ӷֱ���Na+��Al3+��S2-��Cl-��ǰ���ߺ�����2�����Ӳ㣬�����ߺ�����3�����Ӳ㣬���Ӳ�ṹ��ͬ�����ӣ��˵����Խ��İ뾶ԽС�����ԣ��뾶��С����Ϊ�ݣ��ܣ��ߣ��ޡ�
��4��������γɵ�ij�ֻ����ᆳ��������ȡ����Ӧ�������Ȼ�̼������ṹʽΪ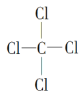 ���û�����ֻ�й��ۼ������ڹ��ۻ����������γɵĵ���ɫ�Ĺ����ǹ������ƣ������������ӷֱ��ǹ��������Ӻ������ӣ������������ӵĸ�����Ϊ1:2��
���û�����ֻ�й��ۼ������ڹ��ۻ����������γɵĵ���ɫ�Ĺ����ǹ������ƣ������������ӷֱ��ǹ��������Ӻ������ӣ������������ӵĸ�����Ϊ1:2��
��5����Ԫ������Ԫ����ȣ���֤��������Ԫ�طǽ�����ǿ������ʵ�У����ļ��⻯�����ļ��⻯���ȶ������ĵ���������ļ��⻯����û���Ӧ�������������ĵ��ʺ���ĵ���״̬��ͬ�����ļ��⻯��ķе����ļ��⻯��ķе�߶�����Ӽ�������������йأ���ǽ������أ����ԣ���֤��������Ԫ�طǽ�����ǿ������ʵ��BD��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�Ӧ6NO2+8NH3=7N2+12H2O���ɵ�صķ���������ʵ����Ч��������������ŷţ����ỷ����Ⱦ�����ܳ�����û�ѧ�ܣ�װ����ͼ��ʾ������˵����ȷ���ǣ������� 
A.�缫BΪ����
B.�缫A�ķ�ӦʽΪ2NH3��6e��+6OH��=N2+6H2O
C.��Һ��OH��ͨ�������ӽ���Ĥ��������Ǩ��
D.����4.48LNO2����״���£�������ʱ��ת�Ƶĵ���Ϊ0.4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���������л�ʵ�����г��õ���Ʒ������������ԭ��Ӧ֪ʶ�͵绯ѧ֪ʶ���Լ����������һ��ԭ��ء�����д���пհף�
(1)ʵ��ԭ����Fe��2H��===Fe2����H2��
(2)ʵ����Ʒ���缫(________��________)��ϡ���ᡢ________��________������(���ߵ�����)(��д��ȱ��ʵ����Ʒ)��
(3)ʵ��װ����ͼ��

(4)ԭ�����Ƽ�ע������⣺
�ٰ���ͼ��ʾװ�����Ӻ�ʵ��������ע��۲�(������)�����Ƿ����������������û�У��ɽ�ԭ��ص������缫�е�һ���Ӵ�������ͷ�ϵ�һ��(ע�⣺�Ӵ���ͬʱ��������һ������������ԭ��ص���һ���缫�ϵ�)����ʱ�����������������������ꡭ��������������ԭ������ԭ����У��ɻ�ѧ��ת��Ϊ________���ڶ���������________ת��Ϊ��������������
�������װ���еĶ�����Ϊ��������������Ӧ�ýӵ�������______�����缫��ӦʽΪ____��������______��Ӧ��
��ͭ��Ӧ�ýӵ�������__________�����缫��ӦʽΪ____________________________��������________��Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽����������Է�Ӧ��mA��g��+nB��g��cZ��g����H ��Ӱ�죬��A��B���ʵ���֮��Ϊm��n��ʼ��Ӧ��ͨ��ʵ��õ���ͬ�����´ﵽƽ��ʱZ�����ʵ���������ʵ������ͼ��ʾ�������ж���ȷ���� ��������
A.�ں��º�ѹ�����£����Ѵﵽƽ�����ϵ�м�������Z������ƽ ��ʱ��Z�����ʵ�����������
B.�����¶ȣ������淴Ӧ���ʶ�����ƽ�ⳣ������
C.��H��0��m+n��c
D.�¶Ȳ��䣬����ѹǿ��ƽ�������ƶ�������ƽ��ʱ��A��Ũ�ȱ�ԭƽ���С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��Ũ�ȵ�ϡ����������Һ�μӵ���Ũ�ȵĴ���ϡ��Һ�У����и�ͼʾ������Һ�й��������ʵı仯���ƣ�һ��������ǣ�������
A.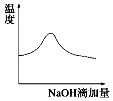
B.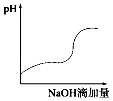
C.
D.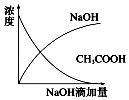
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����һ����CO2�������״�ȼ�ϵķ�����CO2��g��+3H2��g��CH3OH��g��+H2O��g����H=��49.0kJmol��1 �� ��6mol CO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼ��ʾ��ʵ�ߣ���ͼ������a��1��6����ʾ����1minʱH2�����ʵ�����6mol�� 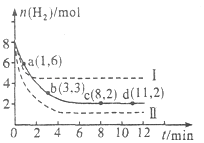
��1��a������Ӧ����������ڡ������ڡ���С�ڡ����淴Ӧ���ʣ�
��2������ʱ���ƽ����Ӧ���������� ��
A.O��1min
B.1��3min
C.3��8min
D.8��11min
��3�����ı�ijһʵ�������ٽ�������ʵ����H2�����ʵ�����ʱ��仯��ͼ����ʾ�����ߣ�������I��Ӧ��ʵ�������ı��� �� ���ߢ��Ӧ��ʵ�������ı��� �� ��������ٳ���3molCO2��4mol H2 �� H2O��g���������������������䡱��С������
��4������1molCO2��3molH2����������У���ַ�Ӧ�ﵽƽ�����CO2ת����Ϊa���������ڵ�ѹǿ����ʼѹǿ֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯���ڻ�ѧ�仯���Ҳ����м������塢Һ�塢�������
A. ʯ�͵ķ���B. ʯ�͵��ѽ�
C. ú�ĸ���D. ú������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣����еı�Ŵ�����Ӧ��Ԫ�ء�
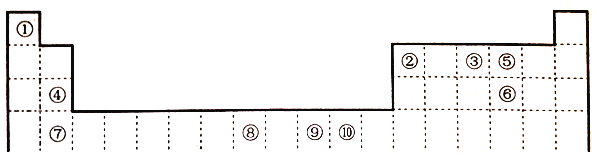
��ش�:
(1)�����ڱ�������10��Ԫ���У��縺����С��Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ_____��
(2)�����ڱ�������10��Ԫ���У������δ�ɶԵ������������ɶԵ������ĸ�����Ϊ3:2��Ԫ��������������û��δ�ɶԵ�������Ԫ���γɵĻ�������______(�ѧʽ)��������ѧ��������_________��
(3)����Ԫ�آ���Ԫ�آ��γɵ�1:1�Ļ��������˵����ȷ����_____(����ĸ���)��
A.�û������е�����ԭ�Ӷ����������8�����ȶ��ṹ
B.�û���������ЦҼ��ͦм���Ŀ��Ϊ1:1
C.�û��������ɼ��Լ��ͷǼ��Լ��γɵļ��Է���
D.�û�������ӵĿռ乹��Ϊֱ����
(4)�ڢ�����γɵ���Է���������С�Ļ�����A�У�Ԫ�آ۵��ӻ�������_____��д���뻯����A��Ϊ�ȵ������һ��������_______(�����ӷ���)��
(5)Ԫ�آ���+3�ۻ�����MCl3��6H2O�����ֲ�ͬ��ɫ���칹�壬Ϊ̽��MCl3��Һ�����İ���ɫ����Ļ�ѧʽ��ȡ0.010molMCl3��6H2O�����Һ���μ�����AgNO3��Һ���õ�����2.870g,�þ���Ļ�ѧʽΪ_______(����ĸ���)��
A.[M(H2O)6]Cl3 B.[M(H2O)5Cl]Cl2��H2O C.[M(H2O)4Cl2]Cl��2H2O
(6)Ԫ�آ���Ԫ�آ��γ�һ�ֻ������侧���ṹ����ͼ��ʾ���û�����Ļ�ѧʽΪ____�����þ����ܶ�Ϊdg/cm3����������Ϊapm�����ӵ�������ֵNAΪ______��
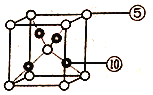
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�������
A. ����ͼװ�õ�⾫��þ
����ͼװ�õ�⾫��þ
B. ����ͼװ����֤�Թ�����˿�������ⸯʴ
����ͼװ����֤�Թ�����˿�������ⸯʴ
C. ��ͼװ����Mg��������Al������
��ͼװ����Mg��������Al������
D.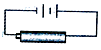 ����ͼװ�öԶ��ε�ؽ��г��
����ͼװ�öԶ��ε�ؽ��г��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com