


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
| A、6.00mol/L |
| B、6.25mol/L |
| C、3.50mol/L |
| D、7.00mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
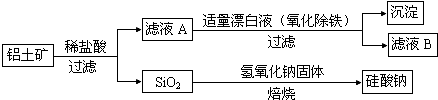

查看答案和解析>>
科目:高中化学 来源: 题型:
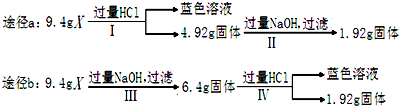
| A、由Ⅰ可知X中一定存在Fe2O3、Cu | ||
| B、由Ⅱ和Ⅲ可得出结论,混合物中无Al2O3 | ||
| C、1.92g固体为SiO2和Cu的混合物 | ||
D、原混合物中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
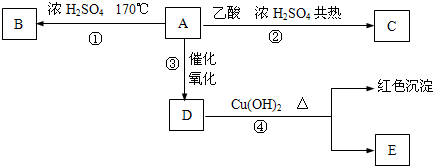
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
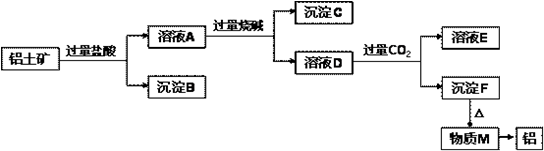
 从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如图所示,请回答下列问题:
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油的分馏是将相对分子质量较大分子变成相对分子质量较小分子的过程 |
| B、石油裂化可提高汽油、煤油和柴油等轻质油的产量 |
| C、石油分馏、裂化、裂解获得的产品都是混合物 |
| D、石油是工业的血液,但石油化工及其产品也对生态环境产生了不良影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com