


科目:高中化学 来源: 题型:
| A、烷烃都能与氯气、溴水在光照和适当的温度下发生取代反应 | ||
| B、烷烃中除甲烷外,很多都能使酸性高锰酸钾溶液的紫色褪去 | ||
| C、CH2Cl2的结构只有一种,能证明了甲烷分子是以碳为中心的正四面体结构,而不是平面正方形的结构 | ||
D、标准状况下,1 L辛烷完全燃烧后,所生成气态产物的分子数为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、萃取操作时,选择的萃取剂的密度必须比水大 |
| D、蒸馏操作时,冷水从下口入,上口出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
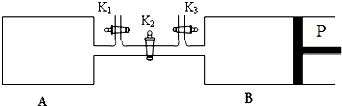
查看答案和解析>>
科目:高中化学 来源: 题型:
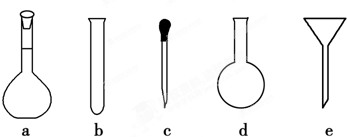
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com