
【题目】向密闭容器中充入CO和![]() 各
各![]() mol,一定温度下发生反应:
mol,一定温度下发生反应:![]() ,下列叙述正确的是
,下列叙述正确的是
A.如果容器内压强不再改变,则证明该反应已达到平衡状态
B.寻找合适的催化剂是加快反应速率并提高![]() 产率的有效措施
产率的有效措施
C.当反应达到平衡后,保持容器内体积不变,再向其中充入CO和![]() 各1mol,达到新的平衡后
各1mol,达到新的平衡后![]() 的产率会增大
的产率会增大
D.如果在某温度下平衡常数为![]() ,则平衡时CO转化率为
,则平衡时CO转化率为![]()
【答案】D
【解析】
![]() 对于反应前后气体分子数不变的反应,容器内的总压强不随时间的变化而改变,如果容器内压强不再改变,不能说明反应达到平衡状态,故A错误;
对于反应前后气体分子数不变的反应,容器内的总压强不随时间的变化而改变,如果容器内压强不再改变,不能说明反应达到平衡状态,故A错误;
B.寻找合适的催化剂是加快反应速率的有效措施,但催化剂不能改变平衡,所以不能提高![]() 产率,故B错误;
产率,故B错误;
C. 当反应达到平衡后,保持容器内体积不变,再向其中充入CO和![]() 各1mol,这是与原投料成比例地再投入反应物,虽然体系的压强会增大,但该反应是前后气体分子数不变的反应,达到平衡后与原平衡等效,
各1mol,这是与原投料成比例地再投入反应物,虽然体系的压强会增大,但该反应是前后气体分子数不变的反应,达到平衡后与原平衡等效, ![]() 的产率不变,故C错误;
的产率不变,故C错误;
D.设容器体积是1L,设CO的变化量为x mol/L,由![]() 可知,各组分的变化量均为x mol/L, 则
可知,各组分的变化量均为x mol/L, 则![]() 的平衡量分别为(0.01 -x)mol/L、(0.01 -x)mol/L、x mol/L、x mol/L,因此,
的平衡量分别为(0.01 -x)mol/L、(0.01 -x)mol/L、x mol/L、x mol/L,因此, ![]() ,解之得,
,解之得,![]() ,CO的平衡转化率
,CO的平衡转化率![]() ,故D正确;
,故D正确;
故选:D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列叙述正确的是
A.4.0 g由CO2和SO2组成的混合物中含有的质子数为2NA
B.2.24 L Cl2与CH4在光照下反应生成的HCl分子数为0.1NA
C.0.1 mol/L K2S溶液中含有的K+数为0.2NA
D.4.2 g CaH2与水完全反应,转移的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是( )

A. a管发生吸氧腐蚀,b管发生析氢腐蚀
B. 一段时间后,a管液面高于b管液面
C. a处溶液的pH增大,b处溶液的pH减小
D. a、b两处具有相同的电极反应式:Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国对“可呼吸”的钠——二氧化碳电池的研究取得突破性进展。该电池的总反应式为4Na+3CO2![]() 2Na2CO3+C,其工作原理如图所示(放电时产生的Na2CO3固体贮存于碳纳米管中)。
2Na2CO3+C,其工作原理如图所示(放电时产生的Na2CO3固体贮存于碳纳米管中)。
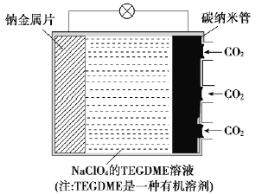
(1)钠金属片作为该电池的___极(填“正”或“负”,下同);放电时,电解质溶液中Na+从___极区向___极区移动。
(2)充电时,碳纳米管连接直流电源的___极,电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3)。其工业流程如下:

回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有__________________(写一条)。
(2)除铁工序中,在加入石灰调节溶液的pH前,加入适量的软锰矿,其作用是______________。
(3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质。若测得滤液中c(F-)=0.01 molL-1,滤液中残留的c(Ca2+)=________________〔已知:Ksp(CaF2)=1.46×10-10〕,
(4)沉锰工序中,298K、c(Mn2+)为1.05 molL-1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如图所示。根据图中信息得出的结论是______________。
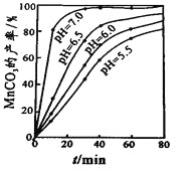
(5)沉锰工序中有CO2生成,则生成MnCO3的离子方程式是______________________。
(6)从沉锰工序中得到纯净MnCO3的操作方法是___________________。副产品A的化学式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个固定容积均为1L密闭容器中以不同的氢碳比![]() 充入
充入![]() 和
和![]() ,在一定条件下发生反应:
,在一定条件下发生反应:![]()
![]() 的平衡转化率
的平衡转化率![]() 与温度的关系如图所示.下列说法正确的是
与温度的关系如图所示.下列说法正确的是![]()
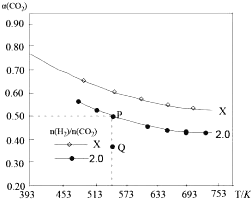
A.该反应在高温下自发进行
B.X的氢碳比![]() ,且Q点在氢碳比为
,且Q点在氢碳比为![]() 时
时![]()
C.若起始时,![]() 、
、![]() 浓度分别为
浓度分别为![]() 和
和![]() ,则可得到P点,对应温度的平衡常数的值为512
,则可得到P点,对应温度的平衡常数的值为512
D.向处于P点状态的容器中,按2:4:1:4的比例再充入![]() 、
、![]() 、
、![]() 、
、![]() ,再次平衡后
,再次平衡后![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为![]() L的密闭容器内,物质D在
L的密闭容器内,物质D在![]() 时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述错误的是
时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述错误的是
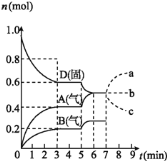
A.从反应开始到第一次达到平衡时,B物质的平均反应速率为![]()
![]()
B.根据如图该反应的平衡常数表达式为![]()
C.若在第5min时升高温度,则该反应的正反应是吸热反应,反应的平衡常数增大,B的反应速率增大
D.若在第7分钟时增加D的物质的量,A的物质的量变化情况符合a曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3和O2在一定条件下发生反应:4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g),现向一容积不变的2 L密闭容器中充入4 mol NH3和3 mol O2,4 min后反应达到平衡,测得生成的H2O(g)占混合气体总体积的40%,则下列表示的此段时间内该反应的平均速率不正确的是( )
2N2(g)+6H2O(g),现向一容积不变的2 L密闭容器中充入4 mol NH3和3 mol O2,4 min后反应达到平衡,测得生成的H2O(g)占混合气体总体积的40%,则下列表示的此段时间内该反应的平均速率不正确的是( )
A. v(N2)=0.125 mol·L-1·min-1B. v(H2O)=0.375 mol·L-1·min-1
C. v(O2)=0.225 mol·L-1·min-1D. v(NH3)=0.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是
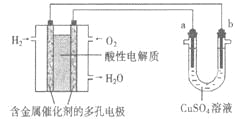
A.若a极是铜,b极为铁时,当电池消耗1.6gO2,b极上析出6.4g铜
B.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH-
C.若a极是粗铜,b极是纯铜时,a极减少的质量等于b极上析出铜的质量。
D.若a、b两极均是石墨时,b极反应为4OH-- 4e-=O2↑+ 2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com