
����Ŀ���������̶��ݻ���Ϊ1L�ܱ��������Բ�ͬ����̼��![]() ����
����![]() ��
��![]() ����һ�������·�����Ӧ��
����һ�������·�����Ӧ��![]()
![]() ��ƽ��ת����
��ƽ��ת����![]() ���¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ����
���¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ����![]()
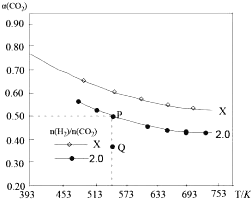
A.�÷�Ӧ�ڸ������Է�����
B.X����̼��![]() ����Q������̼��Ϊ
����Q������̼��Ϊ![]() ʱ
ʱ![]()
C.����ʼʱ��![]() ��
��![]() Ũ�ȷֱ�Ϊ
Ũ�ȷֱ�Ϊ![]() ��
��![]() ����ɵõ�P�㣬��Ӧ�¶ȵ�ƽ�ⳣ����ֵΪ512
����ɵõ�P�㣬��Ӧ�¶ȵ�ƽ�ⳣ����ֵΪ512
D.����P��״̬�������У���2��4��1��4�ı����ٳ���![]() ��
��![]() ��
��![]() ��
��![]() ���ٴ�ƽ���
���ٴ�ƽ���![]() ��С
��С
���𰸡�C
��������
A. ��ͼ���֪�¶�����CO2��ת���ʽ��ͣ�˵��ƽ�������ƶ������H<0���ɡ�S<0��֪��������¡�HT��S>0�������Է����У���A����
B. ����̼��Ϊ2.0ʱ��P���ƽ�⣬Q��δ��ƽ�⣬��ʱ������̼��ת���ʱ�ƽ��ʱС��˵����ʱҪ����ת������Ķ�����̼����Ӧ���������ƶ���������Ӧ���ʴ����淴Ӧ���ʣ���B����
C.2CO2(g)+6H2(g)C2H4(g)+4H2O(g)
��ʼ0.5100
ת��0.250.750.1250.5
ƽ��0.250.250.1250.5
K=0.125��0.5����0.252��0.256��=512����C��ȷ��
D. ��2:4:1:4�ı����ٳ���![]() ��
��![]() ��
��![]() ��
��![]() ���൱���ٰ���4:10����
���൱���ٰ���4:10����![]() ��
��![]() ����̼�ȴ���2�����ƽ���a(CO2)����D����
����̼�ȴ���2�����ƽ���a(CO2)����D����
��ѡ��C��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij��������20 g���ڼ��ȵ�������ͨ��������CO��ȫ��Ӧ�������ɵ�������ʯ��ˮ���գ��õ�����37.5 g���������������Ԫ������Ԫ�ص������ȡ�_________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ����5L�����ܱ������г���
����5L�����ܱ������г���![]() ���壬������Ӧ
���壬������Ӧ![]() ��һ��ʱ���ﵽƽ�⣬��ô˹����д���繲������
��һ��ʱ���ﵽƽ�⣬��ô˹����д���繲������![]() �����������¶ȶȲ���ʱ���ı�ijһ���������н�����ȷ����
�����������¶ȶȲ���ʱ���ı�ijһ���������н�����ȷ����![]()
�����ı� | ���� | |
A | ƽ����������г���1molHe | ƽ�ⳣ�����䣬���������ܶ�Ҳ���� |
B | ��ʼʱ�������г��� | ��Ӧ�ﵽƽ��ǰ |
C | ��ʼʱ�������г��� | �ﵽƽ��ʱ���ų� |
D | ��ʼʱ�������г��� | �ﵽƽ��ʱ�� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����ܱ������г���NO2�������½�������ƽ�⣺2NO2(g)![]() N2O4(g)��H < 0������������100 ����ˮԡ�У����������ʲ��ı����
N2O4(g)��H < 0������������100 ����ˮԡ�У����������ʲ��ı����
A.��ɫB.ѹǿC.����D.ƽ����Է�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������İ�������粒����������Ƶ�������������У���������������䣬��������������Բ��ƣ����ں㶨�¶���ʹ��ﵽ�ֽ�ƽ��NH2COONH4(s) ![]() 2NH3(g)+CO2(g)���������¶Ⱥ�����������䣬�ٳ���n (NH3): n (CO2)=2:1,���ٴδﵽƽ��ʱc (NH3)�� ��
2NH3(g)+CO2(g)���������¶Ⱥ�����������䣬�ٳ���n (NH3): n (CO2)=2:1,���ٴδﵽƽ��ʱc (NH3)�� ��
A.����B.����C.��СD.�������������ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ![]() L���ܱ������ڣ�����D��
L���ܱ������ڣ�����D��![]() ʱ������Ӧ���䷴Ӧ�������������ʵ�����ʱ��t�ı仯��ϵ��ͼ�����������������
ʱ������Ӧ���䷴Ӧ�������������ʵ�����ʱ��t�ı仯��ϵ��ͼ�����������������

A.�ӷ�Ӧ��ʼ����һ�δﵽƽ��ʱ��B���ʵ�ƽ����Ӧ����Ϊ![]()
![]()
B.������ͼ�÷�Ӧ��ƽ�ⳣ������ʽΪ![]()
C.���ڵ�5minʱ�����¶ȣ���÷�Ӧ������Ӧ�����ȷ�Ӧ����Ӧ��ƽ�ⳣ������B�ķ�Ӧ��������
D.���ڵ�7����ʱ����D�����ʵ�����A�����ʵ����仯�������a����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���Ӧ��![]() ��������ͼ��ʾ������˵����ȷ���ǣ� ��
��������ͼ��ʾ������˵����ȷ���ǣ� ��
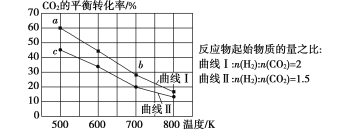
A.�÷�Ӧ��![]()
B.�ﵽƽ��ʱ��![]()
C.b���Ӧ��ƽ�ⳣ��Kֵ����c��
D.a���Ӧ��![]() ��ƽ��ת����Ϊ90%
��ƽ��ת����Ϊ90%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����͵��Ҵ���أ�DEFC�����û����������ܼ�������ʣ��� 200������ʱ���磨 �� �� ͼ �� ʾ ���� �� �� �� �� �� Ч �� �� �� 32 �� �� �� �� �� �� ȫ �� �� �� �� �� Ӧ ΪC2H5OH+3O2==2CO2+3H2O��������˵����ȷ���ǣ� ��
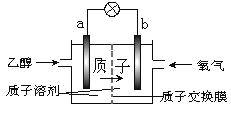
A.a ��Ϊ��ص�����
B.��������ĵ缫��Ӧ��O2 + 4H+ + 4e- = 2H2O
C.��ع���ʱ������ b ���ص��߾������ٵ� a ��
D.��Һ�� H+ �� a �缫�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱ��0.1mo1/LijһԪ��HA��ˮ����0.1���������룬��������������ǣ�
A. ����Һ��pH=4 B. �����¶ȣ���Һ��pH���� C. ����ĵ���ƽ�ⳣ��ԼΪ1��10-7 D. ��HA�������c(H+)ԼΪˮ�������c(H+)��106��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com