
【题目】被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。试回答下列问题:

(1)氢气进入的这极为___极;
(2)写出氢氧燃料电池工作时的正极反应式:___;
(3)该氢氧燃料电池每转移0.1mol电子,消耗标准状态下___L氧气;
(4)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___。
【答案】负 2H2O+O2+4e-═4OH- 0.56 CH4+10OH-﹣8e-═CO32-+7H2O
【解析】
(1)H元素化合价升高,失电子,在负极发生氧化反应,即氢气进入负极,故答案为:负;
(2)氧气在正极得电子,发生还原反应,正极反应式为:2H2O+O2+4e-═4OH-,故答案为:2H2O+O2+4e-═4OH-;
(3)由2H2O+O2+4e-═4OH-可知,每转移4mol电子,消耗标况下22.4L氧气,那么,转移0.1mol电子,消耗标准状态下氧气的体积=![]() =0.56L,故答案为:0.56;
=0.56L,故答案为:0.56;
(4)甲烷在负极失电子,电解质是碱,生成碳酸根,负极反应式为:CH4+10OH-﹣8e-═CO32-+7H2O,故答案为:CH4+10OH-﹣8e-═CO32-+7H2O。


科目:高中化学 来源: 题型:
【题目】氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为
N2(g)+3H2(g)![]() 2NH3(g) △H。
2NH3(g) △H。
(1)已知每破坏1mol有关化学键需要的能量如下表:
H-H | N-H | N-N | N |
435.9KJ | 390.8KJ | 192.8KJ | 945.8KJ |
则△H=_____________。
(2)在恒温、恒压容器中,氨体积比1:3加入N2和H2进行合成氨反应,达到平衡后,再向容器中充入适量氨气,达到新平衡时,c(H2)将_________(填“增大”“减小”或“不变”)
(3)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(φ)如图所示。

①其中,p1、p2和p3由大到小的顺序是________,其原因是__________。
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)______ vB(N2)(填“>”“<”或“=”)
③若在250℃、p1条件下,反应达到平衡时容器的体积为1L,则该条件下合成氨的平衡常数K=___(保留一位小数)。
(4)H2NCOONH4是工业由氨气合成尿素的中间产物。在一定温度下、体积不变的密闭容器中发生反应:H2NCOONH4(s) ![]() 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是_____(填序号)。
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是_____(填序号)。
①混合气体的压强不变
②混合气体的密度不变
③混合气体的总物质的量不变
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3易升华,可用作有机合成的催化剂等.工业上用铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下:

(1)氧化炉中Al2O3、Cl2和C反应的化学方程式______.
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式______.
(3)为了测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,再洗涤、灼烧、冷却、称重、得其质量为0.32g。
①写出上述测定过程中涉及的离子方程式:______、__________。
②AlCl3产品的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出2,2-二甲基-3-乙基戊烷的结构简式___;
(2)写出蔗糖的分子式___;
(3)医院常用消毒酒精的体积分数是___;
(4)乙酸乙酯在酸性条件下水解的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种无机物之间转化关系如下图(反应条件省略。部分产物省略)。下列推断不正确的是
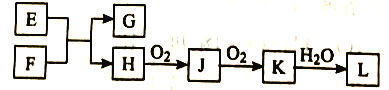
A. 若L为强碱,则E可能为NaCl溶液、F为钾
B. 若L为强酸,则E可能为NaHS、F为HNO3
C. 若L为弱酸,则E可能为Mg、F为CO2
D. 若L为强酸,则E可能为NH4Cl、F为Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种物质的转化关系如图所示,A 是中学富见的金属,常温常压下Y呈液态,J由阴、阳离子个数1: 1构成且阴、阳离子都与氖原子的电子层结构相同。Z遇浓盐酸产生“白烟”。

回答下列问题
(1)J的化学式为_______________。
(2)写出③反应的化学方程式_______________。
(3)写出⑤反应的化学方程式_______________。
(4)实验室制备Z可能选择下列装置的是_______________(填代号)。

(5)为了测定X产品纯度,进行如下实验:取WgX产品溶于足量蒸馏水,将产生的气体全部赶出来并用V1 mLc 1mol/L盐酸吸收( 过量),再用c2mol/L NaOH溶液滴定吸收液至终点。消耗V2mL NaOH溶液。该样品纯度为_________________。若碱式滴定管未用待装溶液润洗,则测得结果__________(填“偏 高”、“偏 低”或“无 影 响” )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应达到平衡时,NO的物质的量浓度是________。
(2)如图中表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________。

(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某同学设计的放热反应的观察装置,

其实验操作步骤如下:
①按图所示将实验装置连接好;
②在U形管内加入少量红墨水(或品红溶液),打开T形管活塞,使U形管内两边的液面处于同一水平面,再关闭T形管活塞;
③在盛有1.0g氧化钙的小试管里滴入2 mL左右的蒸馏水,观察现象。
试回答:
(1)实验前必须进行的一步实验操作是_______________。
(2)实验中观察到的现象是______________________________________________________________。
(3)实验中发生的化学反应方程式:____________________________。
(4)说明CaO、H2O的能量与Ca(OH)2的能量之间的关系:_______________________________________。
(5)若该实验中CaO换成NaCl,实验还能否观察到相同现象?____(填“能”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两气体A、B分别为0.6mol与0.5mol,在0.4L密闭容器中发生反应:3A+B=mC+2D,经5min后达到平衡,此时C为0.2mol,在此时间内D的平均反应速率为0.1molL﹣1min﹣1,下列结论错误的是( )
A.平衡时反应混合物总物质的量为1molB.B的转化率为20%
C.A的平均反应速率为0.15 molL﹣1min﹣1D.m值为2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com