
某化学兴趣小组为验证NO2的氧化性和NO的还原性,设计了如下装置制取NO2和NO,并验证其性质:
(1)写出甲中反应的离子方程式:_________________________________,
乙中的现象是_________________________________________________,
可证明NO2的氧化性;在丙中鼓入空气后的现象是_______________,可证明NO的还原性。
(2)实验前丙中充满水的作用是___________________________________
(用反应的化学方程式和简要文字回答)。
(3)小华对上述实验设计提出了质疑,他认为乙中的现象不足以证明NO2的氧化性,他的理由是___________________________________________。
你认为怎样才能准确证明NO2的氧化性?____________________________________(简要回答出原理和现象即可)。
科目:高中化学 来源: 题型:实验题
由下列仪器组成的一套制取SO2并验证它有氧化性、还原性和漂白性。(图中铁架台、铁夹等省略,装置③中E管气体向上流出)②④⑤装置中所用试剂只能从以下物质中选用:氯水、浓H2SO4、溴水、硝酸、品红溶液、烧碱溶液、石灰水。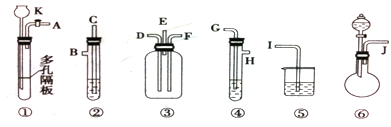
试回答:
(1)连接仪器时,导气管连接顺序从左到右J接_____、_____接_____、H接D、______接I、______接______。
(2)装置②用以检验SO2的还原性,所盛试剂最好是______,装置④中所盛试剂最好是______,装置⑤中所盛试剂最好是_______,目的是
(3)仪器连接好后,怎样检查装置①的气密性,简述操作要点 。
(4)书写①装置中反应的化学方程式 。
书写③装置中反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学学习小组设计下图实验装置(夹持装置略去)制备Cl2,并探究氯气的相关性质。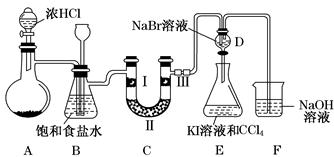
(1)若A装置中固体药品为KClO3,则反应中每生成1 mol Cl2时转移电子的物质的量为________mol。
(2)装置B既能除去氯气中的氯化氢,还能检测实验过程中装置C是否发生堵塞。若C中发生堵塞,则B中将观察到的现象是_______________________________________。
(3)装置C的作用是验证氯气是否具有漂白性,Ⅰ处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是________、________。
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。请简述能说明氯、溴、碘非金属性强弱的实验操作及现象:_____________________________________________。
(5)请用化学方程式说明装置F的作用:_______________________________________。
(6)甲同学提出,装置F中的试剂可改用足量的Na2SO3溶液,乙同学认真思考后认为此法不可行。请用离子方程式解释乙认为不可行的原因:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学兴趣小组为了探究某些气体的性质,设计了如图所示的实验装置。实验时将A、D中产生的气体同时通入C中。(K为止水夹,部分夹持仪器已略去)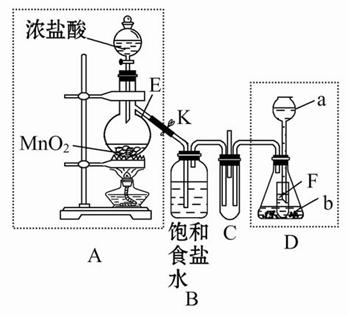
回答下列问题:
(1)简述实验前检查A部分装置气密性的方法_______________________________________。
(2)仪器E的名称是______,锥形瓶内小试管F的作用是______。
(3)若b是生石灰,a是______时,在C中有白烟产生,写出生成白烟的化学方程式________________________。
(4)若a是质量分数为75%的硫酸,b是亚硫酸钠粉末,在C中盛适量的BaCl2溶液时,写出C中发生反应的离子方程式:____________。
(5)从环保的角度出发,上述实验装置中需要改进的是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学课外活动小组在实验室设计了如图所示的实验装置,进行“氨的催化氧化”实验。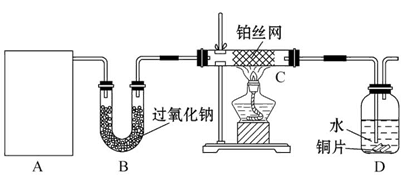
(1)A处是气体发生装置,A中所用的试剂只能从下列物质中选取:
①硝酸铵;②碳酸铵;③碳酸氢铵;④氯化铵;⑤熟石灰;⑥氢氧化钠。
若A中制取气体时只用了一种药品,则该药品可以是_________(填选项编号),在只用一种药品制取氨气时,图中空白处所需仪器应为_________ (选填下列仪器编号,固定装置省略)。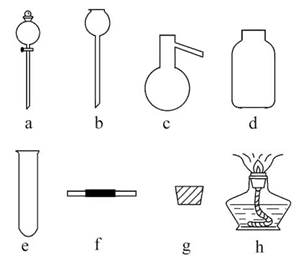
(2)该装置补充完整后,仍然存在一定的缺陷,试从安全与环保的角度来考虑,对该装置进行改进:
①_______________________________________________________________;
②_______________________________________________________________。
(3)按照改进后的装置进行实验,请完成以下问题:
①装置B的作用是__________________________________________________;
②写出C中发生反应的化学方程式: ________________________________;
③若A、B处试剂足量,则装置D中可以观察到的实验现象有_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某研究性学习小组欲利用下列装置制取少量次氯酸钠,并进一步探究次氯酸钠的化学性质。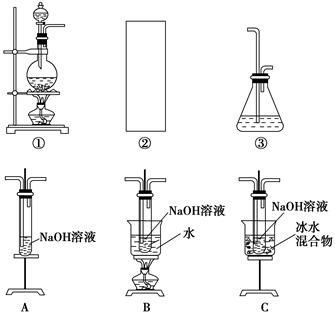
相关资料:反应Cl2+2NaOH=NaClO+NaCl+H2O属于放热反应,温度稍高时便发生副反应3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
(1)制取氯气时,在烧瓶中加入一定量的二氧化锰,通过____________(填写仪器名称)向烧瓶中加入适量的浓盐酸。请在装置A、B、C中选择一个合适的装置放在②处:____________。
(2)部分学生认为上述装置存在缺点,他们指出在①②装置之间应增加如D所示的装置,你认为D中所盛液体是________,其作用是________________________________________。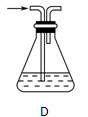
(3)该小组对产品的性质进行了如下探究。
第一步,测其pH=10。结合相关离子方程式解释原因:_________________________________________________________________。
第二步,该小组的同学选用了紫色石蕊试液对次氯酸钠的性质进行探究。请你帮助他们完成下表:
| 实验操作 | 预期现象 | 结论 |
| | | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
已知Cl2和碱溶液在不同条件下,得到的产物不同。某兴趣小组用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。(3Cl2+6KOH KClO3+5KCl+3H2O )
KClO3+5KCl+3H2O )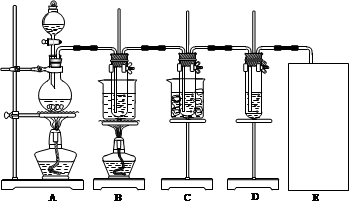
图中:A为氯气发生装置;B的试管里盛有15 mL 30% KOH溶液,并置于水浴中;C的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;D的试管里加有紫色石蕊试液。请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过 (填仪器名称)向圆底烧瓶中加入适量的浓盐酸。装置A中反应的离子方程式为 。需要向烧瓶中加碎瓷片吗? (选填:“需要”、“不需要”)。
(2)反应结束后,烧瓶里的溶液 。
A一定显酸性;B可能显酸性,也可能为中性;C只有氧化性;D只有还原性;E既有氧化性又有还原性
(3)反应完毕,B试管中有少量晶体析出,经冷却后,有大量晶体析出。图中符合该晶体溶解度曲线的是 (填编号字母);从B的试管中分离出该晶体必须用到的玻璃仪器有 。
(4)该小组同学发现制得的氯酸钾产量偏低,可能的一种原因是Cl2中含有HCl气体。对此问题可以通过改进实验装置的方法进行避免。方法是 。
(5)实验中可观察到D的试管里溶液的颜色由紫色先变为_________色,最终变为________色。
(6)C装置中反应完毕的现象是______________________________________________。
(7)请在装置图方框中画出缺少的实验装置,并注明试剂。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用。
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。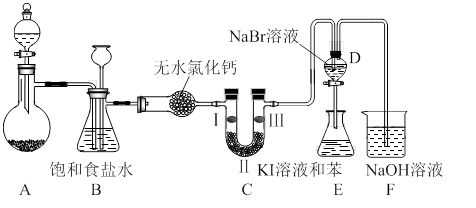
(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,相应的离子方程式为: 。
(2)装置B的作用是 ,监测实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入 。(选a或b或c)
| | a | b | c |
| I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某学校兴趣小组设计如下装置进行实验探究(a、b为弹簧夹,加热及固定装置已略去)。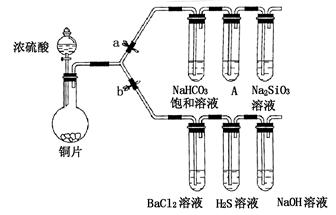
(1)验证碳、硅非金属性的相对强弱
①连接仪器、 、加药品后,打开a关闭b,然后滴入浓硫酸,加热;
②装置A中的试剂是 ;
③能说明碳的非金属性比硅强的实验现象是 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性
①打开b,关闭a。能验证SO2具有氧化性的化学方程式是 ;
②若过量的SO2通入NaOH溶液中,其离子方程式是 ;
③BaCl2溶液中无沉淀现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com