
【题目】目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:

下列说法不正确的是
A. 在海水中加入石灰乳的作用是沉淀Mg2+
B. 可用电解氯化镁的方法获得镁
C. 操作B涉及到加热浓缩(或蒸发结晶)、过滤等操作
D. 上述过程中只涉及到氧化还原反应和复分解反应
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:
【题目】【选修3:物质的结构与性质】Ⅰ.氟元素是电负性最大的非金属元素,且氟原子的半径小,因此氟单质极易和金属单质反应且把它们氧化到最高价态,如MnF7 、VF5 、CaF2 等。氟元素还可以和氧元素形成氟化物,如OF2 等。
请回答下列问题:

(1)V原子的核外电子排布式为 。如图表示一个不完整的CaF2 晶胞,则图中实心球表示 (填“F-或Ca2+ )。 设晶胞边长为a,则最近的F-和Ca2+之间的距离为 (用含a的代数式表示)。
(2)OF2 分子中氧原子的轨道杂化类型为 ,OF2被称为氟化物而不被称为氧化物的原因是 。
Ⅱ.纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物。回答下列问题:
(3)写出基态Cu+ 的核外电子排布式 。C、N、O三种元素的第一电离能由大到小的顺序是 。
(4)如图所示是铜的某种氧化物的晶胞示意图,该氧化物的化学式为 。
(5)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,在滴加氨水至沉淀刚全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀。该深蓝色沉淀中的NH3通过键与中心离子Cu2+结合。NH3分子中的N原子杂化方式是 。与NH3分子互为等电子体的一种微粒是 (任写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-==Cu
C. 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
D. a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A. 5.4 g H2O分子中的氢原子数为0.3NA
B. 25℃,1 L pH=12的氨水中,含有OH-的数目为0.1NA
C. 标准状况下,32 g硫(结构如图所示)含S—S键的数目为NA

D. 在反应KIO3+6HI===3I2+KI+3H2O中,每生成1 mol I2转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸分子的结构式为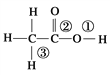 ,下列反应及断键部位正确的是
,下列反应及断键部位正确的是
a.乙酸的电离,是①键断裂 b.乙酸与乙醇发生酯化反应,是②键断裂
c.在红磷存在时,Br2与CH3COOH的反应:CH3COOH+Br2![]() CH2Br—COOH+HBr,是③键断裂
CH2Br—COOH+HBr,是③键断裂
d.乙酸变成乙酸酐的反应:2CH3COOH → ![]() +H2O,是①②键断裂
+H2O,是①②键断裂
A. 只有abc B. abcd C. 只有bcd D. 只有acd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴及其化合物可应用与催化剂、电池、颜料与染料等。
(1)CoO是一种油漆添加剂,可通过反应①②制备。
①2Co(s)+O2(g)=2CoO(s) ΔH1=akJ·mol-1
②2CoCO3(s) =CoO(s) + CO2 (g) ΔH2=akJ·mol-1
则反应2Co(s)+O2(g)+2CO2(g)=2CoO3(s) 的ΔH=_________。
(2)某锂电池的电解质可传导Li+,电池反应式为:LiC6+CoO2![]() C6+LiCoO2
C6+LiCoO2
①电池放电时,负极的电极反应式为_________,Li+向______移动(填“正极”或“负极“)。
②一种回收电极中Co元素的方法是:将LiCoO2与H2O2、H2SO4反应生成CoSO4。该反应的化学方程式为___________________。
(3)BASF高压法制备醋酸采用钴碘催化循环过程如图-1所示,该循环的总反应方程式为_________________(反应条件无需列出)
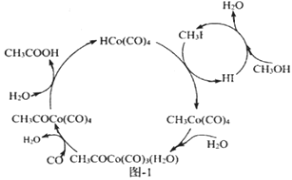
(4)某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx。不同温度下,将10mol模拟尾气(成分如下表所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图-2所示.
模拟尾气 | 气体 | 碳烟 | ||
NO | O2 | He | ||
物质的量分数或物质的量 | 0.25% | 5% | 94.75% | a mol |
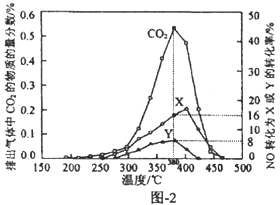
①380℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为__________________。
②实验过程中采用NO模拟NOx,,而不采用NO2的原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铍的原子半径为0.089 nm,下面是几种短周期元素的相关信息(该题中大写字母均为元素代号,不是元素符号)
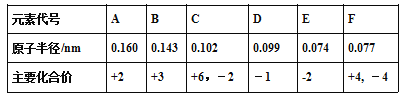
(1)C元素的简单阴离子结构示意图________,F元素在周期表中的位置____________。
(2)D的单质与水反应的离子方程式_____________,该反应生成的含氧酸的电子式________。
(3)F元素与半径最小的元素形成的最简单有机化合物的结构式___________。
(4)钠元素与E元素形成的所有化合物中,可能含有的化学键类型_______(填字母代号)。
a.离子键 b.极性共价键 c.非极性共价键 d.金属键
(5)B、C、E三种元素的简单离子半径由大到小顺序________________(填离子符号)。
(6)某同学选取稀硫酸、过量碳酸氢钠溶液和过量硅酸钠溶液,并设计了下图装置完成硫、碳、硅三种元素非金属性强弱比较的实验研究。下图中装置Ⅰ的名称_______,装置Ⅲ中反应的离子方程式_________________。
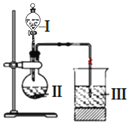
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与我们人类生活息息相关,下列说法不正确的是
A. 开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径
B. 工业上,电解熔融MgCl2制金属镁
C. 研发使用高效催化剂,可提高反应中原料的转化率
D. “冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对十二烷基苯磺酸钠![]() 是常用洗涤剂的主要成分。
是常用洗涤剂的主要成分。
其结构可用图形![]() 来表示,端为链烃基,O端为极性基。根据这一结构特点,试分析和回答下列问题:
来表示,端为链烃基,O端为极性基。根据这一结构特点,试分析和回答下列问题:
(1)十二烷基苯磺酸钠分子在其水溶液表面分布的结构示意图应是下列各图中的____图(填写序号),理由是____________________________________。
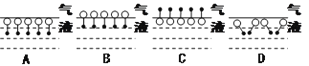
(2)进入介质(水)内部的十二烷基苯磺酸钠分子,可能会以下列结构形式中的____存在(填写序号),理由是____________________________________。
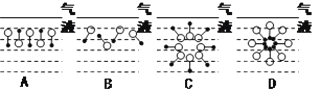
(3)工业合成对十二烷基苯磺酸钠的一种路线如下图所示:
![]()
![]()
请回答下列问题:
①产品中的亲油基是_______。
②由十二烷基苯制取对十二烷基苯磺酸的化学方程式为_________,反应类型为__________。
③在洗涤剂中添加酶制剂能促进污垢中的蛋白质(如奶渍、肉汤)等水解为可溶性的物质而被除去。使用加酶洗衣粉的水溶液中浸泡10~30min,水温在40~50℃最佳。加酶洗衣粉不宜在高温下、潮湿环境中贮存,也不宜久存。请解释原因_________________________________。
④过去使用的合成洗涤剂中常加入三聚磷酸钠(Na5P3O10)做助剂,它可使硬度大的洗涤水软化,对微细的无机粒子或油脂具有分散、乳化、胶溶作用,防止污渍再次沉积到衣物上;它还能维持水溶液的弱碱性,提高洗涤剂的去污能力和洗涤效果。但是,20世纪90年代以来,世界各国先后提出必须生产和使用无磷洗涤剂。请解释原因______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com