
【题目】A为分子式为C7H8的芳香烃根据下面的反应路线及所给信息填空. 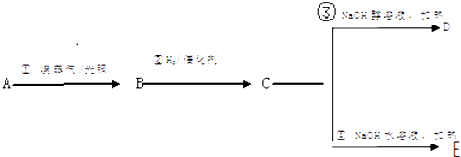
(1)A的名称是 .
(2)①的反应类型是;③的反应类型是 .
(3)简述B中卤素原子的检验方法
(4)反应①的化学方程式是 反应③的化学方程式是
反应④的化学方程式是 .
【答案】
(1)甲苯
(2)加成反应;消去反应
(3)取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素
(4)![]() +Br2
+Br2 ![]()
![]() +HBr;
+HBr;![]() +NaOH
+NaOH ![]()
![]() +NaBr+H2O;
+NaBr+H2O;![]() +NaOH
+NaOH ![]()
![]() +NaBr
+NaBr
【解析】解:A为分子式为C7H8的芳香烃,则A为 ![]() ,反应①为甲苯在光照条件下发生甲基上的取代反应,反应②发生苯环与氢气的加成反应,反应③为醇的消去反应,反应为卤代烃发生水解反应,可推知B为
,反应①为甲苯在光照条件下发生甲基上的取代反应,反应②发生苯环与氢气的加成反应,反应③为醇的消去反应,反应为卤代烃发生水解反应,可推知B为 ![]() ,C为
,C为 ![]() ,D为
,D为 ![]() ,E为
,E为 ![]() .(1)A的名称是甲苯,所以答案是:甲苯;(2)①的反应类型是:取代反应.③的反应类型是消去反应,所以答案是:取代反应;消去反应;(3)B(
.(1)A的名称是甲苯,所以答案是:甲苯;(2)①的反应类型是:取代反应.③的反应类型是消去反应,所以答案是:取代反应;消去反应;(3)B( ![]() )中卤素原子的检验方法:取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素, 所以答案是:取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素;(4)反应①的化学方程式是:
)中卤素原子的检验方法:取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素, 所以答案是:取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素;(4)反应①的化学方程式是: ![]() +Br2
+Br2 ![]()
![]() +HBr,
+HBr,
反应③的化学方程式是: ![]() +NaOH
+NaOH ![]()
![]() +NaBr+H2O,
+NaBr+H2O,
反应④的化学方程式是: ![]() +NaOH
+NaOH ![]()
![]() +NaBr,
+NaBr,
所以答案是: ![]() +Br2
+Br2 ![]()
![]() +HBr;
+HBr;![]() +NaOH
+NaOH ![]()
![]() +NaBr+H2O;
+NaBr+H2O;![]() +NaOH
+NaOH ![]()
![]() +NaBr.
+NaBr.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将一定量的A12O3固体加入100mLNaOH溶液中,固体全部溶解,向所得溶液中逐滴加入1.0 molL-1盐酸,所得沉淀的物质的量与加入盐酸体积的关系如图所示(不考虑溶液体积的变化),则下列说法正确的是

A. 原NaOH溶液的浓度为1.0mol/L B. 原A12O3的质量为0.51g
C. V0的数值为35 D. 沉淀量达到最大时,溶液的溶质有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃ 和101kpa时,乙烷、乙炔和丙烯组成的混合烃32mL与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体的总体积缩小了72mL,原混合烃中乙炔的体积分数为( )
A.12.5%
B.25%
C.50%
D.75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制氯气:MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑下列说法错误的是( )
MnCl2+2H2O+Cl2↑下列说法错误的是( )
A. 还原剂是HCl,氧化剂是MnO2
B. 每生成1 mol Cl2,转移电子的物质的量为2 mol
C. 每消耗1 mol MnO2,起还原剂作用的HCl为4 mol
D. 生成的Cl2中含有HCl杂质,用饱和食盐水除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加碘食盐中通常加入的是KIO3 , 该物质在酸性条件下表现出较强的氧化性,可以和碘化物、亚硫酸盐等还原性物质发生反应.
(1)写出KIO3与KI在稀硫酸介质中发生反应的离子方程式
(2)为测定菜加碘盐中碘元素的含量,某学生甲设计了如下实验: A.准确称取w g食盐,使其完全溶解在适量的蒸馏水中;
B.用稀硫酸酸化所得溶液,加入过量的KI溶液,使其充分反应;
C.以为指示剂,逐滴加入物质的量浓度为2.0×10﹣3mol/L的硫代硫酸钠溶液10.0mL,恰好完全反应,判断反应完全的实验现象为 , 则该加碘盐样品中碘元素的含量为mg/Kg(用含w的代数式表示).
(已知:I2+2S2O32﹣═2I﹣+S4O62﹣)
(3)某学生乙又进行了下列实验: A.准确称取1.0g纯净的NaCl,加3mL蒸馏水配成溶液,溶液为无色;
B.滴入5滴指示剂和1mL 0.lmol/L KI溶液,充分振荡,溶液不变化;
C.继续滴加l滴1mol/L的硫酸溶液,充分振荡,溶液变蓝色
推测实验中产生蓝色现象的原因,用离子方程式表示
根据学生乙的实验结果,请对学生甲的实验结果进行分(偏大、偏小、正确),其原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
A.等物质的量浓度的下列溶液:①H2CO3、②Na2CO3、③NaHCO3、④(NH4)2CO3:其中c(CO ![]() )的大小关系为:②>④>③>①
)的大小关系为:②>④>③>①
B.pH=2 的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH﹣)+c(HC2O ![]() )+c(C2O
)+c(C2O ![]() )
)
C.向0.2 mol?L﹣1NaHCO3 溶液中加入等体积0.1 mol?L﹣1NaOH 溶液:c(CO ![]() )>c(HCO3﹣)>c(OH﹣)>c(H+)
)>c(HCO3﹣)>c(OH﹣)>c(H+)
D.常温下,同浓度的CH3COONa与CH3COOH 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH﹣)>c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原子结构、元素性质的说法正确的是( )
A. 某元素的质量数为其相对原子质量数值上取整
B. ⅠA族金属元素是同周期中金属性最强的元素
C. 同种元素的原子均有相同的质子数和中子数
D. ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置可以验证非金属性的变化规律。

(1)仪器A的名称为_____________________,干燥管D的作用是______________________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、_______、_______,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 根据分散质粒子的大小,可将分散系分为溶液、胶体和浊液
B. 胶体中分散质粒子的直径通常大于100nm
C. 溶液一定是均一、稳定的混合物
D. 向沸腾的蒸馏水中逐滴加入适里FeCl3饱和溶液, 继续煮沸至液体呈红褐色,可制得Fe(OH)3胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com