
【题目】三氟化氮是一种无色、无味、无毒且不可燃的气体,可在铜的催化作用下由F2和过量NH3反应得到,在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO 和 HNO3,请根据要求回答下列问题:
(1)写出制备NF3的化学反应方程式:______________________________。反应过程中,氧化剂与还原剂的物质的量之比为________。
(2)写出三氟化氮与水蒸气反应的化学方程式:______________________________________。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是_____________________________________。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染。其产物除H2O外,还有另三种钠盐:_________________________________(填化学式)。
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A. 107gFe(OH)3胶体中胶体粒子的数目为NA
B. 1L0.1mol·L-1Na2CO3溶液中CO32-和HCO3-的离子数之和为0.1NA
C. 常温常压下,3.6gD2O中含有中子数2NA
D. 30g由14C2H2和C18O组成的混合气体中含有的质子数为14NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体说法的正确组合是

①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-紧邻
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④
C.③⑤⑦ D.③⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示,A为常见调味品,B为常见液体,C、E是金属。D、F为气态单质,其中D为黄绿色。J为红褐色固体,A、C、G、I、K的焰色反应均为黄色。K是一种含+6价元素的含氧酸盐,其摩尔质量为166 g·mol-1。
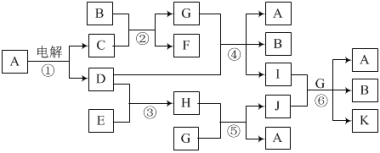
(1)物质B的电子式为___。物质D所含元素在周期表中的位置是___。
(2)写出反应②的化学方程式,并用单线桥表示电子转移的方向和数目:___。
(3)写出反应④的离子方程式:___。
(4)写出反应⑥的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以粗硅(含硅、硼等)为原料制取四氯化硅(SiCl4)的装置示意图如下:
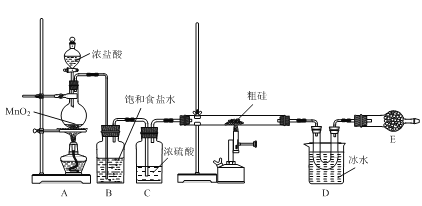
已知:①SiCl4遇水易反应;BCl3与SiCl4互溶。
②高温下硅、硼与氯气反应后所得物质的部分性质如表:
物质 | SiCl4 | BCl3 |
沸点/℃ | 57.7 | 12.8 |
熔点/℃ | -70.0 | -107.2 |
(1)装置A中盛装浓盐酸的仪器名称是___。
(2)用湿润的淀粉KI试纸可以检验Cl2,写出表示该反应原理的离子方程式:___。
(3)装置B中饱和食盐水的作用是___。
(4)装置D中收集到的物质,可用___方法分离出纯净的SiCl4。
(5)装置E中应装入的试剂名称是___,其作用有___、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数(NA)的说法错误的是( )
A. 25℃、101KPa条件下22克CO2所含的原子数目为1.5NA
B. 标准状况下0.1molH2O含有的分子数目为0.1NA
C. 0℃、101KPa条件下03NA氧气的体积是6.72升
D. 58.5克NaCl固体中含有的离子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1Ba(OH)2溶液300 mL(忽略溶液体积变化),反应后溶液中SO42-的物质的量浓度为
A.0.4 mol·L-1B.0.1 mol·L-1C.0.2 mol·L-1D.0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种化合物均由短周期元素组成。其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
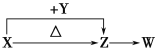
请回答:
(1)W的电子式是 。
(2)X与Y在溶液中反应的离子方程式是 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
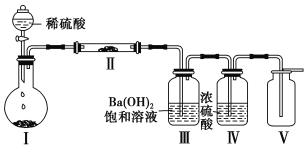
①装置Ⅰ中反应的化学方程式是 ,
装置Ⅱ中物质的化学式是 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 。
(从上图选择必要装置,填写编号)
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖。青蒿素分子式C15H22O5,相对分子质量为282.下面关于青蒿素的说法正确的是
A.1 mol C15H22O5的质量为282 g/mol
B.C15H22O5的摩尔质量等于它的相对分子质量
C.一个C15H22O5微粒的质量约为 ![]() g
g
D.含有6.02×1023个碳原子的C15H22O5的物质的量为1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com