
【题目】烟气中主要污染物为SO2、NO、NO2,可用如图工艺进行脱硫脱硝及产物回收。
(1)空气预处理过程中,发生主要反应的化学方程式为_______。
(2)洗气过程中,尿素作还原剂,转化成两种无污染的气体的化学式是_______
(3)充分曝气氧化过程中,发生反应的含镁化合物是_________。
(4)完成沉镁过程中生成碱式碳酸镁的离子方程式___Mg2++____= MgCO3Mg(OH)2↓+__CO2↑+____H2O
(5)(NH4)2SO4粗品中含有的主要杂质为_________(填名称)。
(6)碱式碳酸镁经过简单加工可循环利用,加工过程发生反应的化学方程式为______。
【答案】2NO + O2 = 2NO2 CO2、N2 MgSO3 2 4HCO3- 3 1 硝酸铵 MgCO3·Mg(OH)2![]() 2MgO+CO2↑+H2O
2MgO+CO2↑+H2O
【解析】
根据题中工业流程可知,烟气中主要污染物为SO2、NO、NO2,在空气中预处理时,主要将NO氧化成NO2,再用含尿素的氧化镁悬浊液还原生成氮气和二氧化碳,同时溶液中有硫酸镁、亚硫酸镁、硝酸镁等物质生成,在充分曝气氧化中,亚硫酸镁被氧化成硫酸镁,再加入碳酸氢铵溶液生成碱式碳酸镁沉淀,过滤后将滤液浓缩结晶可得硫酸铵晶体。
(1)在空气中预处理时,主要将NO氧化成NO2,发生主要反应的化学方程式为2NO+O2=2NO2;
(2)根据上面的分析可知,洗气过程中,生成两种无污染的气体是CO2、N2,
(3)在充分曝气氧化中,亚硫酸镁被氧化成硫酸镁,发生反应的为MgSO3;
(4)镁离子和碳酸氢根离子发生双水解,生成碱式碳酸镁,根据电荷守恒和元素守恒可知其离子反应方程式为2Mg2++4HCO3-=MgCO3·Mg(OH)2↓+3CO2↑+H2O;
(5)根据物料守恒,在Mg2+和HCO3-发生反应生成碱式碳酸镁时,还有硫酸铵、硝酸铵生成,因此(NH4)2SO4粗品中含有的主要杂质为硝酸铵;
(6) 碱式碳酸镁经过加热生成氧化镁和二氧化碳及水,氧化镁可循环利用,反应的方程式为MgCO3·Mg(OH)2![]() 2MgO+CO2↑+H2O。
2MgO+CO2↑+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】物质结构与性质自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用。
(1)请写出Fe的基态原子核外电子排布式__________。
(2)金属A的原子只有3个电子层,其第一至第四电离能如下:

则A原子的价电子排布式为__________________。
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(Ⅰ)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3![]() [Cu(NH3)3CO]Ac ΔH<0。 配合物[Cu(NH3)3CO]Ac中心原子的配位数为__________。
[Cu(NH3)3CO]Ac ΔH<0。 配合物[Cu(NH3)3CO]Ac中心原子的配位数为__________。
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3 ℃,MgO的熔点高达2800 ℃。造成两种晶体熔点差距的主要原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误是

A. Q位于第三周期IA族
B. X、Y、Z三种元素组成的化合物可能是盐或碱
C. 简单离子半径:M->Q+>R2+
D. Z与M的最高价氧化物对应水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A,相对分子质量为140,其中碳的质量分数为0.857。A分子中有两个碳原子不与氢直接相连。A在一定条件下氧化只生成G,G能使石蕊试液变红。

试写出:
(1)A的分子式___________________。
(2)化合物A和G的结构简式: A___________________,G___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象描述正确的是

A. 逸出气体的体积,a电极的小于b电极的
B. 一电极逸出无味气体,另一电极逸出刺激性气体
C. a电极附近呈红色,b电极附近呈蓝色
D. a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法处理酸性污水的工作原理如图所示,下列说法不正确是( )
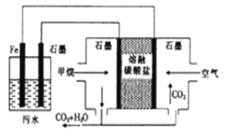
A. 铁电极的电极反应式为Fe-2e-=Fe2+
B. 通入甲烷的石墨的电极反应式为:CH4+4CO32-—8e- ==5CO2+2H2O
C. 为了增强的污水的导电能力,可向污水中加入适量食盐
D. 若左池石墨电极产生44.8L气体,则消耗0.5mol甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个电化学过程的示意图。请回答下列问题:

(1)图中甲池中OH-移向_________极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式:__________________________________
(3)A电极的名称是_____ , 乙池中反应的化学方程式为_____________。若要使溶液恢复电解前的状态,应向乙池中加入________(写化学式)。
(4)当乙池中B(Ag)极质量增加10.8g,甲池中理论上消耗O2的体积为________L(标准状况),此时丙池中某电极析出某金属,则丙池中的某盐溶液可能是____________
A. MgSO4 B.CuSO4 C.NaCl D. AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素。X原子的质子数与电子层数相同,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示。下列说法不正确的是

A. 原子半径:W>Y>Z>M>X
B. 热稳定性:XM>X2Z,沸点:X2Z>YX3
C. X、Y、Z三种元素形成的化合物中不可能含离子键
D. YM3、WM4分子中每个原子最外层均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,进行如下反应:NO(g)+CO(g)![]()
![]() N2(g)+CO2(g);△H=﹣373.2kJ/mol达到平衡后,为提高NO的转化率,采取的正确措施是( )
N2(g)+CO2(g);△H=﹣373.2kJ/mol达到平衡后,为提高NO的转化率,采取的正确措施是( )
A. 加催化剂B. 充入CO增大压强C. 充入N2D. 升高温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com