
【题目】下列所示物质的制备方法合理的是( )
A.实验室从海带中提取单质碘:取样→灼烧→溶解→过滤→萃取→蒸馏
B.金红石(主要成分TiO2)为原料生产金属Ti:金红石、焦炭![]() TiCl4
TiCl4![]() Ti
Ti
C.从海水中提取溴:浓缩海水→溴水![]() Br2
Br2
D.由铝土矿为原料制备金属铝:Al2O3![]() AlCl3(aq)
AlCl3(aq)![]() AlCl3(s)
AlCl3(s)![]() Al
Al
科目:高中化学 来源: 题型:
【题目】按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为所期望的最终产物,原子利用率为100%。下列制备CH3CH2OH的反应中符合“原子经济”要求的是( )
A.CH2=CH2+H2O![]() CH3CH2OH
CH3CH2OH
B.CH3COOCH2CH3+H2O![]() CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH
C.C6H12O6(葡萄糖) ![]() 2CH3CH2OH+2CO2↑
2CH3CH2OH+2CO2↑
D.CH3CH2Cl+NaOH![]() CH3CH2OH+NaCl
CH3CH2OH+NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从煤和石油中可以提炼出化工原料A和H。已知A是石油裂解气的主要产物之一,其产量是衡量一个国家石油化工发展水平的标志。H是一种比水轻的油状液体,H仅由碳氢两种元素组成,H不能使酸性KMnO4溶液褪色,其碳元素与氢元素的质量比为12:l,H的相对分子质量为78。下列是有机物A~G之间的转化关系:

请回答下列问题:
(1)D中所含官能团的名称是_________________;
(2)写出反应③的化学方程式_______________________________________;
(3)G是一种高分子化合物,可以用来制造农用薄膜材料等,其结构简式__________;
(4)在体育竞技比赛中,当运动员肌肉挫伤或扭伤时,随队医生立即对准其受伤部位喷射物质F(沸点12.27℃)进行应急处理。写出由A制备F的化学方程式:___________;
(5)下列关于B的一种同系物甲醇的说法不正确的是___________(填字母)。
a.甲醇的结构简式为CH3OH,官能团为—OH
b.甲醇完全燃烧后的产物为CO2和H2O
c.B与甲醇都极易溶于水,是因为它们都能与水分子间形成氢键
d.甲醇与钠反应可以产生氢气,所以甲醇显酸性
(6)等质量的A、H完全燃烧时消耗O2的物质的量_______(填“A>H、A<H或A=H”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期我国学者研制出低成本的电解“水制氢”催化剂——镍掺杂的磷化钴三元纳米片电催化剂(![]() )。回答下列问题:
)。回答下列问题:
(1)Co在元素周期表中的位置为_________,Co2+价层电子排布式为______________。
(2)Co、Ni可形成![]() 、
、![]() 、
、![]() 等多种配合物。
等多种配合物。
①![]() 的空间构型为__________,
的空间构型为__________,![]() 中N原子的杂化轨道类型为_________。
中N原子的杂化轨道类型为_________。
②C、N、O、S四种元素中,第一电离能最大的是_____________。
③![]() 中含有σ键的数目为__________;已知NF3比NH3的沸点小得多,试解释原因________________________________________。
中含有σ键的数目为__________;已知NF3比NH3的沸点小得多,试解释原因________________________________________。
(3)常用丁二酮肟来检验Ni2+,反应如下:
Ni2+(aq)+2 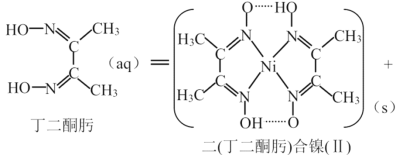 2H+(aq)
2H+(aq)
①1个二(丁二酮肟)合镍(Ⅱ)中含有_________________个配位键。
②上述反应的适宜![]() 为_________________(填字母序号)
为_________________(填字母序号)
A.12 B.5~10 C.1
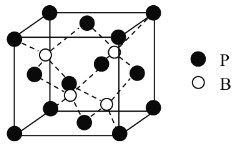
(4)磷化硼是一种备受关注的耐磨涂料,其晶体中磷原子作面心立方最密堆积,硼原子填入四面体空隙中(如图)。已知磷化硼晶体密度为![]() ,计算晶体中硼原子和磷原子的最近核间距为___________
,计算晶体中硼原子和磷原子的最近核间距为___________![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究原电池原理,设计如图装置。下列叙述正确的是( )
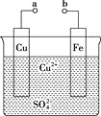
A. a和b不连接时,铁片上会有![]() 产生
产生
B. a和b用导线连接时,铁片上发生的反应为![]()
C. a和b用导线连接时,电子由a流向b
D. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)是一种工业化工原料,可用于制取有机磷农药、长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O2和PCl3为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):
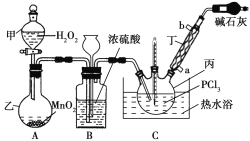
已知PCl3和三氯氧磷的性质如表:
熔点/℃ | 沸点/℃ | 其他物理或化学性质 | |
PCl3 | -112.0 | 76.0 | PCl3和POCl3互溶,均为无色液体,遇水均剧烈水解,发生复分解反应生成磷的含氧酸和HCl |
POCl3 | 1.25 | 106.0 |
(1)装置A中的分液漏斗能否用长颈漏斗代替?做出判断并分析原因:_______
(2)装置B的作用是______________(填标号)。
a.气体除杂 b.加注浓硫酸 c.观察气体流出速度 d.调节气压
(3)仪器丙的名称是___________,实验过程中仪器丁的进水口为__________(填“a”或“b”)口。
(4)写出装置C中发生反应的化学方程式_______,该装置中用温度计控制温度为60~65 ℃,原因是________。
(5)称取16.73 g POCl3样品,配制成100 mL溶液;取10.00 mL溶液于锥形瓶中,加入3.2 mol·L-1的AgNO3溶液10.00 mL,并往锥形瓶中滴入5滴Fe2(SO4)3溶液;用0.20 mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00 mL(已知:Ag++SCN-=AgSCN↓)。则加入Fe2(SO4)3溶液的作用是________,样品中POCl3的纯度为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验一种氮肥的成分,某学习小组的同学进行了以下实验:①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊。②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。由此可知该氮肥的主要成分是( )
A.NH4NO3B.(NH4)2CO3C.NH4ClD.NH4HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
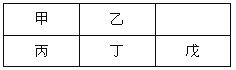
A. 原子半径:丙<丁<戊B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊D. 最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向![]() 溶液中逐滴滴入
溶液中逐滴滴入![]() 溶液,溶液的pH与
溶液,溶液的pH与![]() 溶液体积关系如图所示:(忽略溶液体积变化,且无气体产生)
溶液体积关系如图所示:(忽略溶液体积变化,且无气体产生)
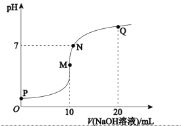
(1)用化学用语表示M点![]() 的原因__________。
的原因__________。
(2)![]() 四点中,水电离产生的
四点中,水电离产生的![]() 浓度最大的是______________点。
浓度最大的是______________点。
(3)下列关系中,正确的是________。
a P点![]()
b N点![]()
c Q点![]()
d ![]() 溶液中
溶液中![]() 小于
小于![]() 溶液中
溶液中![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com