
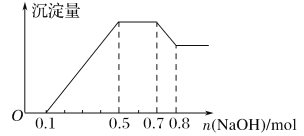
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如下图所示。则下列说法正确的是( )
A. 溶液中的阳离子只有H+、Mg2+、Al3+
B. 溶液中n(NH4+)=0.2mol
C. 溶液中一定不含CO32-,可能含有SO42-和NO3-
D. n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
【答案】B
【解析】
若加入锌粒,产生无色无味的气体,说明气体是氢气,因此溶液显酸性,则CO32-和NO3-不能大量共存;加入NaOH溶液,产生白色沉淀,说明不存在铁离子;根据产生的沉淀量与加入NaOH的物质的量之间的关系图可知,溶液中一定含有Mg2+、Al3+;又因为当沉淀达到最大值时,继续进入氢氧化钠,沉淀不变,这说明溶液中还存在NH4+,其n(NH4+)=0.7mol-0.5mol=0.2mol;由于溶液中还必须存在阴离子,所以一定还有SO42。根据图可知,氢离子的物质的量时0.1mol、铝离子的物质的量是0.1mol,但镁离子是(0.5mol-0.1mol-0.3mol)÷2=0.05mol。
A.由上述分析可知,溶液中的阳离子只有H+、Mg2+、Al3+、NH4+,故A错误;
B.由上述分析可知,溶液中n(NH4+)=0.2mol,故B正确;
C.由上述分析可知,溶液中一定不含CO32-、NO3-,一定含有SO42-,故C错误;
D.由上述分析可知,溶液中n(H+):n(Al3+):n(Mg2+)=0.1mol:0.1mol:0.05mol=2:2:1,故D错误;
故选B。


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 金刚石和石墨互为同位素B. CH3CH2CH2CH3和CH3CH(CH3)2互为同系物
C. C2H4和C2H6互为同系物D. C2H6和C5H12互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用自来水养鱼,在将水注入鱼缸之前需把水在阳光下爆嗮一段时间,目的是( )
A.增加水中含氧量B.利用阳光中紫外线杀菌
C.使自来水中少量次氯酸分解D.通过日照提高水的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在某酸性的无色溶液中大量共存的是( )
A.NH4+、Mg2+、SO42﹣、Cl﹣B.Ca2+、I﹣、Na+、NO3﹣
C.Al3+、Cu2+、SO42﹣、Cl﹣D.K+、Cl﹣、HCO3﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:①高温下用碳还原二氧化硅制得粗硅;②粗硅与Cl2加热反应制得四氯化硅;③四氯化硅经精馏提纯后与过量H2在高温下反应制得高纯硅。请依次写出所涉及的反应方程式:
①___________________________________________;
②____________________________________________;
③_____________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
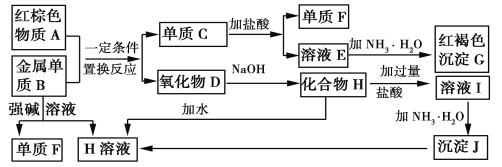
请回答下列问题:
(1)物质A的化学式为__________。
(2)写出单质B与强碱溶液反应的离子方程式____________________________。
(3)溶液E中加入氨水时,先生成白色沉淀L,L最终变为红褐色沉淀G,写出L变为G的化学反应方程式___________。
(4)溶液E敞口放置容易变质,为了防止溶液E的变质,可往溶液中加入___________。
(5)溶液I中所含金属离子是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得。
(1)元素第一电离能:Al______Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为: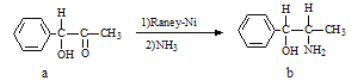 化合物b中进行sp3杂化的原子有__________个。
化合物b中进行sp3杂化的原子有__________个。
(3)一种铝镍合金的晶胞结构如下图,与其晶胞结构相似的化合物是____________(选填序号)。
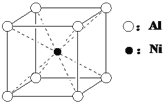
a.氯化钠 b.氯化铯 c.石英 d.金刚石
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
①Ni2+在基态时,核外电子排布式为____________________。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)______。
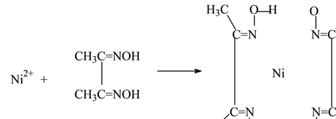
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应COCl2(g) ![]() CO(g)+Cl2(g) ΔH>0。改变下列条件,能加快反应速率,且CO的物质的量分数增大的是
CO(g)+Cl2(g) ΔH>0。改变下列条件,能加快反应速率,且CO的物质的量分数增大的是
A. 恒容下通入He B. 恒容下增大COCl2的浓度
C. 加催化剂 D. 升温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com