
【题目】电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是
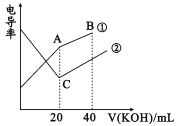
A. B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B. A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C. C点水电离的c(OH-)大于A点水电离的c(OH-)
D. A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
【答案】A
【解析】溶液电导率与离子浓度成正比,HCl是强电解质、醋酸是弱电解质,所以相同浓度的盐酸和醋酸,盐酸中离子浓度大于醋酸,则相同浓度的盐酸和醋酸,盐酸电导率较大,根据图象知,①是醋酸和KOH的混合、②是HCl和KOH的混合。A. B点溶液中KOH过量,溶液中溶质为等物质的量浓度的CH3COOK和KOH,醋酸根离子水解生成OH-,但水解程度较小,溶液呈强碱性,则离子浓度大小顺序是c(K+)>c(OH-)>c(CH3COO-)>c(H+),A项正确;B.A点溶液中,醋酸和KOH恰好完全反应生成CH3COOK,溶液中存在电荷守恒,则c(CH3COO-)+c(OH-)-c(H+)═c(K+),A点溶液体积增大一倍,则离子浓度降为原来的一半,所以c(CH3COO-)+c(OH-)-c(H+)═c(K+)=0.05mol/L,B项错误;C .C点HCl和KOH恰好完全反应生成KCl,对水的电离无影响;A的溶质为CH3COOK,促进水电离,所以C点水电离的c(OH-)小于A点水电离的c(OH-),C项错误;D.离子积常数与温度有关,温度相同,离子积常数相同,温度不一定是常温,数值不一定是1.0×10-14,D项错误;故选B。


科目:高中化学 来源: 题型:
【题目】取Fe、FeO、Fe2O3的均匀混合物质量为7.2g,向其中加入200 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出1120 mL(标准状况)的气体。所得溶液中,加入KSCN溶液无血红色出现,那么若用足量的CO在高温下还原相同质量的此混合物,能产生铁的质量为 ( )
A. 1.4g B. 2.8g C. 5.6g D. 11.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.1 mol CH≡CH可以与Br2发生加成反应,消耗2 mol Br2
B.苯的邻位二元取代物只有一种可以说明苯分子不具有碳碳单键和碳碳双键的交替结构
C.甲苯(![]() )中所有原子都在同一平面内
)中所有原子都在同一平面内
D.己烷的沸点高于2-甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间(t)产生氢气体积(V)的数据,根据数据绘制如图,则曲线a、b、c、d所对应的实验组别可能是( )

组别 | c(HCl)/(molL-1) | 温度/℃ | 状态 |
1 | 2.0 | 25 | 块状 |
2 | 2.5 | 30 | 块状 |
3 | 2.5 | 50 | 粉末状 |
4 | 2.5 | 30 | 粉末状 |
A.④—③—②—①B.①—②—③—④
C.③—④—②—①D.①—②—④—③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯常用做香料,用于化妆品、洗涤用品、皂用及室内清新剂等。乙酸苯甲酯可以用下面的设计方案合成。

回答下面问题:
(1)写出A、C的结构简式:A___________ C__________;
(2)A→B属于_____反应, C→D属于_________反应;
(3)写出乙酸苯甲酯在NaOH溶液中水解的反应方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.利用甲烷催化还原NOx消除氮氧化物的污染
①CH4(g)+4NO2(g) ![]() 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO(g) ![]() 2N2(g)+CO2(g)+2H2O(g) ΔH2=-1 160 kJ·mol-1
2N2(g)+CO2(g)+2H2O(g) ΔH2=-1 160 kJ·mol-1
③CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(g) ΔH3=-867 kJ·mol-1
N2(g)+CO2(g)+2H2O(g) ΔH3=-867 kJ·mol-1
(1)如果三个反应的平衡常数依次为K1、K2、K3,则K3=________(用K1、K2表示)。
(2)在2L恒容密闭容器中充入1 mol CH4和2 mol NO2进行反应③,CH4的平衡转化率α(CH4)与温度和压强的关系如图所示。
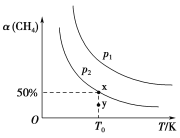
①若容器中的压强为p2,y点:v正________(填“大于”“等于”或“小于”)v逆。
②x点对应温度下反应的平衡常数K=________。
Ⅱ.甲烷蒸气转化法制H2的主要反应为:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)
CO(g)+3H2(g)
(3)在恒容密闭容器中充入2 mol CH4和H2O(g)的混合气体,且CH4和H2O(g)的物质的量之比为x,相同温度下达到平衡时测得H2的体积分数φ(H2)与x的关系如图所示。
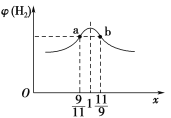
则CH4的转化率:a点________(填“>”“=”或“<”,下同)b点,CH4(g)的浓度:a点________b点,氢气的产率:a点________b点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g),生成2molHI(g)反应放出热量akJ,已知(a、b、c均大于零),下列说法正确的是( )
2HI(g),生成2molHI(g)反应放出热量akJ,已知(a、b、c均大于零),下列说法正确的是( )

A.反应物的总能量低于生成物的总能量
B.断开1molH—H键和1molI—I键所需能量大于断开2molH—I键所需能量
C.向密闭容器中加入2molH2和2molI2,充分反应后放出的热量等于2akJ
D.断开2molH—I键所需能量为(c+b+a)kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常采取CO(g)和H2(g)合成CH3OH(g)
(1)已知某温度和压强下
①2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
③2CH2OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H=-1275.6kJ·mol-1
则在相同温度和压强下,CO(g)与H2(g)合成CH3OH(g)的热化学方程式__________。若反应生成6.4g甲醇,则转移电子的物质的量为__________。
(2)可利用甲醇燃烧反应设计一个燃料电池。如图1,用Pt作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
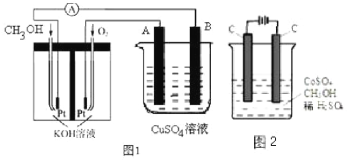
①写出燃料电池负极的电极反应式__________。
②若利用该燃料电池提供电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是__________极(填“A”或“B”);当铁件的质量增重6.4g时,燃料电池中消耗氧气的标准状况下体积为__________L。
(3)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后将甲醇氧化成CO2和H+(用石墨烯除去Co2+)现用如图2所示装置模拟上述过程,则Co2+在阳极的电极反应式为__________。除去甲醇的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向 20 mL 0.1 mol·L 1 的两种酸 HA、HB 中分别滴加0.1 mol·L 1 NaOH 溶液, 其 pH 变化分别对应下图中的 I、II。下列说法不正确的是( )
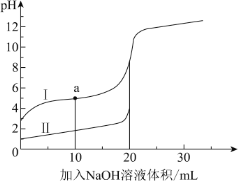
A.向 NaA 溶液中滴加 HB 可产生 HA
B.滴加 NaOH 溶液至 pH=7 时,两种溶液中 c(A-)=c(B-)
C.a 点,溶液中微粒浓度:c(A-) > c(Na+)
D.滴加 20 mL NaOH 溶液时,I 中 H2O 的电离程度大于 II 中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com