
【题目】25℃、101 kPa时,1 g甲醇(CH3OH)完全燃烧生成CO2和液态H2O,同时放出22.68 kJ热量。下列表示该反应的热化学方程式中正确的是( )
A.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=-725.8 kJ/mol
O2(g)=CO2(g)+2H2O(l) ΔH=-725.8 kJ/mol
B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=+1 451.6 kJ/mol
C.2CH3OH+3O2=2CO2+4H2O(l) ΔH=-22.68 kJ/mol
D.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(g) ΔH=-725.8 kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH=-725.8 kJ/mol
【答案】A
【解析】
1g甲醇(CH3OH)完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量,可知1molCH3OH完全燃烧生成CO2和液态H2O,放热为22.68kJ×32=725.8 kJ,结合物质的状态、焓变来解答。
A. 1molCH3OH完全燃烧生成CO2和液态H2O,放热为22.68kJ×32=725.8 kJ,则热化学方程式为CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l)△H=725.8 kJ/mol,故A正确;
O2(g)=CO2(g)+2H2O(l)△H=725.8 kJ/mol,故A正确;
B. 放热反应,焓变为负,故B错误;
C. 应注明物质的状态,且物质的量与热量成正比,故C错误;
D. 水的状态应为液态,故D错误;
答案选A。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出氮元素的原子结构示意图:_____________。
(2)通常情况下,氮气性质不活泼,其原因是__________。
A.氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
(3)N2的电子式:__________,将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______
A.N2和H2在一定条件下反应生成NH3
B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO
D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:__________________。
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式______________。
(6)下面是实验室制取氨气的装置和选用的试剂,其中错误的是________。
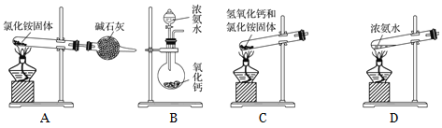
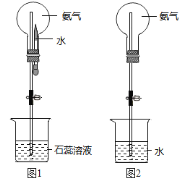
(7)用圆底烧瓶收集干燥的氨气,用图1装置进行喷泉实验,挤压滴管的胶头时,可以得到红色喷泉,原因(用方程式表示) _________________________。
(8)如果只提供如图2的装置,请说明引发喷泉的方法__________________________。
(9)NH4NO3是常用的铵态氮肥,在施用时若受热会释放出________而降低肥效。检验NH4+的方法是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。

实验记录如下:

请回答下列问题:
(1)A中反应的离子方程式是__________________________________________________。
(2)实验操作Ⅱ吹入热空气的目的是_________________________________________。
(3)装置C的作用是____________,C中盛放的药品是_____________。
(4)实验操作Ⅲ,混合液逐渐变成红棕色,其对应的离子方程式_______________________。
(5)由上述实验得出的结论是_________________________________________________。
(6)实验反思:
①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是_____________________________________________________________________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是(写出一条即可):____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来我国在天然气脱硫研究方面取得了新进展,利用如图1装置可完成天然气脱硫,甲池中发生反应如图2所示。


下列关于该装置工作原理的说法中,正确的是( )
A.碳棒为该脱硫装置的负极
B.乙池中发生的反应为:H2S+2e-=S+2H+
C.AQ与H2AQ间的转化属于非氧化还原反应
D.除I![]() /I-外,Fe3+/Fe2+也能实现如图所示循环过程
/I-外,Fe3+/Fe2+也能实现如图所示循环过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,我国秋冬季雾霾天气呈现常态化趋势,造成严重空气污染,对人类身心健康造成极大威胁。硫酸盐气溶胶作为PM2.5的主要构成成分,是雾霾产生的一个重要元凶。科学家最近发现了一种利用水催化促进硫酸盐形成的化学新机制。如图所示:
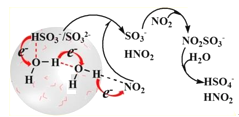
(1)NO2和SO2作为大气初期污染物的主要成分,主要来自_____。
(2)电子传递可以促进HSO![]() 中O—H键的解离,进而形成中间体SO
中O—H键的解离,进而形成中间体SO![]() ,反应的离子方程式为_____。
,反应的离子方程式为_____。
(3)通过“水分子桥”,处于纳米液滴中的SO![]() 或HSO
或HSO![]() 可以将电子快速转移到周围的气相NO2分子。观察图示可知“水桥”主要靠____形成。写出HSO
可以将电子快速转移到周围的气相NO2分子。观察图示可知“水桥”主要靠____形成。写出HSO![]() 与NO2间发生的总反应的离子方程式:_____。
与NO2间发生的总反应的离子方程式:_____。
(4)亚硝酸(HNO2)是一种弱酸,酸性比醋酸稍强,极不稳定,只能存在于稀的水溶液中,加热时发生歧化反应,生成一种强酸和一种遇空气变为红棕色的气体,写出该反应的化学方程式:_____。
(5)结合题中信息,请写出一种鉴别NaNO2和NaCl的方法:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,浓度均为1 mol·L-1的A2和B2两种气体,在密闭容器内反应生成气体C,反应达平衡后,测得:c(A2)=0.16 mol·L-1,c(B2)=0.58 mol·L-1,c(C)=0.84 mol·L-1,则该反应的正确表达式为 ( )
A.2A2+B2 ![]() 2A2BB.A2+B2
2A2BB.A2+B2 ![]() 2AB
2AB
C.A2+B2 ![]() A2B2D.A2+2B2
A2B2D.A2+2B2 ![]() 2AB2
2AB2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的恒容密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)反应在三种不同的条件下进行,反应物SO2的物质的量(mol)随反应时间(min)的变化情况如下表所示:
2SO3(g)反应在三种不同的条件下进行,反应物SO2的物质的量(mol)随反应时间(min)的变化情况如下表所示:
实验序号 | 时间 物质的量 温度 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
1 | 490℃ | 2.00 | 1.00 | 0.50 | 0.30 | 0.25 | 0.20 | 0.20 |
2 | 490℃ | 2.00 | 0.30 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
3 | 500℃ | 2.00 | 0.50 | 0.35 | 0.30 | 0.30 | 0.30 | 0.30 |
(1)对照实验1,实验2改变的某一外界条件可能是_______。
(2)反应达平衡后,向实验2中加入少量的18O2,一段时间18O后可能存在于哪些物质中________(填选项)。
A 只存在氧气 B 只存在三氧化硫 C 只存在反应物 D 存在反应物与生成物
(3)实验3中,在5~15min时段,用O2表示的平均反应速率为______ mol/(L·min)。
(4)若将实验1置于绝热体系中,测得实验到达平衡的时间比原来缩短了,则参加反应的SO2和O2的总能量______(填“>”、“<”或“=”)生成的SO3的总能量。
(5)能说明实验3达到平衡状态的标志是_______(任写一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L密闭容器中充入4molA气体和3molB气体,发生下列反应:2A(g)+B(g) ![]() C(g)+xD(g),5s达到平衡。达到平衡时,生成了1mol C,测定D的浓度为1mol/L。
C(g)+xD(g),5s达到平衡。达到平衡时,生成了1mol C,测定D的浓度为1mol/L。
(1)求x =____。
(2)求这段时间A的平均反应速率为_____。
(3)平衡时B的浓度为______。
(4)下列叙述能说明上述反应达到平衡状态的是_____
A 单位时间内每消耗2 mol A,同时生成1molC
B 单位时间内每生成1molB,同时生成1mol C
C D的体积分数不再变化
D 混合气体的压强不再变化
E B、C的浓度之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol/L的一元碱BOH与等浓度的HCl溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
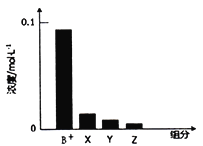
A. BOH为强碱 B. 该混合液pH=7
C. 图中X表示BOH,Y表示H+,Z表示OH- D. 该混合溶液中:c(Cl-)=c(Y)+c(B+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com