
【题目】实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
A. 950 mL,111.2 g B. 500 mL,117 g
C. 1 000 mL,117 g D. 1 000 mL,111.2 g
科目:高中化学 来源: 题型:
【题目】下列对热化学方程式:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH1=-a kJ/mol(a>0)的描述,错误的是
2SO3(g) ΔH1=-a kJ/mol(a>0)的描述,错误的是
A. 该热化学方程式中,物质状态发生变化时,a值发生变化
B. 将方程式的系数缩小1/2,则新方程式的ΔH=1/2ΔH1
C. 该方程式的逆反应ΔH>0
D. 开始时充入2 mol SO2和1 mol O2,达平衡时,放出a kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l)ΔH1=-67.7kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l)ΔH2=-57.3kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s)ΔH3<0
下列说法正确的是( )
A. HF的电离方程式及热效应:HF(aq)![]() H+(aq)+F-(aq) ΔH>0
H+(aq)+F-(aq) ΔH>0
B. 在氢氧化钠溶液与盐酸的反应中,氢氧化钠溶液量越多,中和热越大
C. ΔH2=-57.3 kJ·mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热
D. 稀硫酸与稀氢氧化钡溶液反应的热化学方程式为H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.
(1)该反应的离子方程式为 __________________________________ .
实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01molL-1、0.001molL-1,每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1molL-1)的用量均为2mL.在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
KMnO4酸性溶液的浓度/molL-1 | 溶液褪色所需时间t/min | ||
第1次 | 第2次 | 第3次 | |
0.01 | 14 | 13 | 11 |
0.001 | 6 | 7 | 7 |
(2)计算用0.001molL-1KMnO4酸性溶液进行实验时KMnO4的平均反应速率___________________________ (忽略混合前后溶液的体积变化).
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行? _____________________ .(填“行”或“不行”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员研制出一种可作为鱼雷和潜艇的储备电源的新型电池——锂水电池(结构如图),使用时加入水即可放电。下列关于该电池的说法不正确的是( )
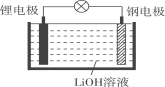
A. 锂为负极,钢为正极B. 工作时负极的电极反应式为Li-e-=Li+
C. 工作时OH-向钢电极移动D. 放电时电子的流向:锂电极→导线→钢电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组混合液:①四氯化碳和氯化钠溶液;②实验室制蒸馏水;③溴化钠和单质溴的水溶液.分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏B.萃取、蒸馏、分液C.分液、蒸馏、萃取D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KAl(SO4)2·12H2O] 在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、 Al2O3及少量SiO2和FeO ·xFe2O3)可制备明矾。工艺流程如下:回答下列问题:
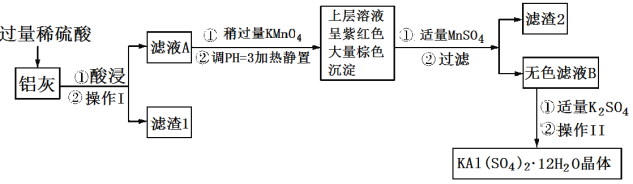
(1)明矾净水的原理是______________________________(用离子方程式表示)。
(2)操作Ⅰ是________,操作Ⅱ是蒸发浓缩、__________、过滤、__________、干燥。
(3)检验滤液A中是否存在Fe2+的试剂是________________(只用一种试剂)。
(4)将铝灰投入氢氧化钠溶液中生成气体的化学方程式是_______________________,在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下MnO4—转化为Mn2+):________________。
(5)已知:在pH=3、加热条件下,MnO![]() 可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:________,滤渣2含有的物质是_______________。
可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:________,滤渣2含有的物质是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生用如下图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物。

请回答下列问题:
(1)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。装置Ⅱ中生成有机物的反应为__________________________________________(填化学方程式),装置Ⅲ中小试管内苯的作用是__________________________________。
(2)能说明苯与液溴发生了取代反应的现象是_____________________。
(3)反应结束后,要让装置Ⅰ中的水倒吸入装置Ⅱ中,这样操作的目的是___________。简述这一操作的方法__________。
(4)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①用蒸馏水洗涤、振荡、分液;②用5%的NaOH溶液洗涤、振荡、分液;③用蒸馏水洗涤、振荡、分液;④加入无水CaCl2粉末干燥;⑤_______________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为纪念 Dmitri Mendeleev 发明的元素周期表诞生 150 周年,联合国将 2019 年定为“国际化学元素周期表年”。 a、 b、 c、 d、四种短周期元素分别位于三个周期,其原子的最外层电子数和原子半径之间的关系如图所示。下列说法中错误的是

A. a为氢元素
B. 原子半径 c<d
C. b的最高价氧化物对应的水化物为强酸
D. a与 c组成的一种化合物中既含极性键又含非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com