
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是________,操作②的名称是____________。
(2)试剂a是____________(填化学式,下同),试剂b是__________,固体B是____________。
(3)加入试剂a所发生反应的化学方程式为__________________________________。
加入试剂b所发生反应的化学方程式为____________________________________。
(4)该方案能否达到实验目的:__________________________(填“能”或“不能”)。若不能,应如何改进?(若能,此问不用回答)__________。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____的质量。
【答案】溶解 过滤 K2CO3 HCl BaCl2 K2CO3+BaCl2BaCO3↓+2KCl BaCO3+2HClBaCl2+ CO2↑+ H2O 不能 应在操作②的滤液中加入过量盐酸后再蒸发结晶 沉淀A1或固体B
【解析】
试题(1)将固体混合物形成溶液的操作为溶解;操作②是将固体和溶液分离,为过滤。(2分离氯化钾和氯化钡,应将氯化钡转化为沉淀而分开,所以先加入碳酸钾,生成碳酸钡沉淀,所以试剂a为碳酸钾,沉淀A为碳酸钡,洗涤后加入盐酸,碳酸钡和盐酸反应生成氯化钡,再蒸发结晶即可得B氯化钡,所以试剂b为盐酸。滤液为氯化钾。(3) 加入碳酸钾,氯化钡和碳酸钾反应生成碳酸钡沉淀和氯化钾,方程式为K2CO3+BaCl2=BaCO3↓+2KCl;碳酸钡和盐酸反应生成氯化钡和水和二氧化碳,方程式为BaCO3+2HCl= BaCl2+CO2↑+H2O。(4)因为加入了碳酸钾,所以滤液中有碳酸钾,直接蒸发结晶有碳酸钾杂质,应在操作②的滤液中加入过量盐酸后再蒸发结晶。(5)要的定氯化钾或氯化钡的质量分数,需要知道氯化钾或氯化钡的质量,所以需要获得的数据有沉淀A1或固体B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
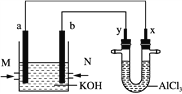
【题目】图是以甲烷和O2构成的燃料电池电解AlCl3溶液的装置,电极材料均为石墨。用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。下列说法正确的是( )
A. 原电池中电解质溶液的pH增大
B. 电解池中电解AlCl3溶液的总反应为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. M处通入的气体为CH4,电极反应式为CH4+10OH--8e-===CO![]() +7H2O
+7H2O
D. 电解池中Cl-向x极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁制品容易生锈,对钢铁制品防腐措施合理的是
A. 暂时不使用的铁锅涂上油 B. 铁质自来水管缠上铜线
C. 铜铁帽的防护栏涂上油漆 D. 自行车钢圈镀铬
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 23 g Na与足量H2O反应完全后可生成NA个H2分子(已知:2Na+2H2O===2NaOH+H2↑)
B. 18 g D2O和18 g H2O中含有的质子数均为10NA
C. 标准状况下,22.4 L N2和H2的混合气中含NA个原子
D. 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数小于2NA(已知反应:2NO+O2===2NO2,2NO2![]() N2O4)
N2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为__________mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是________(填字母)。
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl-的数目
D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取________mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面(____)
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水(____)
(4)①假设该同学成功配制了0.400 mol·L-1的盐酸,他又用该盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需取________mL盐酸。
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是________。(填字母)
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1 mol Na2CO3·10H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1 mol Na2 CO3(s)溶于水会使溶液温度升高,热效应为△H2;Na2CO3·10H2O受热分解的化学方程式为Na2CO3·10H2O (s) ![]() Na2CO3(s)+10H2O(1),热效应为△H3。则下列判断正确的是( )
Na2CO3(s)+10H2O(1),热效应为△H3。则下列判断正确的是( )
A.△H2 <△H3 B.△H1>△H3 C.△Hl+△H3=△H2 D.△H1+△H2>△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国预计在2020年前后建成自己的载人空间站。为了实现空间站的零排放,循环利用人体呼出的CO2并提供O2,我国科学家设计了一种装置(如下图),实现了“太阳能一电能一化学能”转化,总反应方程式为2CO2=2CO+O2 。关于该装置的下列说法不正确的是

装置a 装置b
附:⊕表示阳离子,Θ表示阴离子
A. 装置a将太阳能转化为电能,装置b将电能转化为化学能
B. 工作过程中OH-向Y电极周围移动
C. 人体呼出的气体参与X电极的反应:CO2+2e-+H2O=CO+2OH-
D. 反应完毕后恢复到原温度,装置b中电解质溶液的碱性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,下列五种溶液:
① 0.1mol/L NH4Cl
② 0.1mol/L CH3COONH4
③ 0.1mol/L NH4HSO4
④ 0.1mol/L NH3·H2O和0.1mol/L NH4Cl的混合液
请根据要求填写下列空白:
(1)溶液①呈酸性,其原因是__________________________________(用离子方程式表示)
(2)比较溶液②、③中c(NH4+)的大小关系是②____③(填“>”“=”或“<”)。
(3)在溶液④中,_________离子的浓度为0.1mol/L;NH3·H2O和 ___________离子的浓度之和为0.2 mol/L。
(4)室温下,测得溶液②的pH=7, CH3COO-与NH4+浓度的大小关系是:c(CH3COO-)______c(NH4+)(填“>”“=”或“<”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com