
【题目】某课外活动小组的同学们在老师的帮助下,探究用赤铁矿(主要成分是Fe2O3)炼铁的主要反应原理。他们设计的实验装置如图所示,回答下列问题:
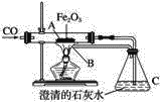
(1)写出用一氧化碳还原氧化铁的化学方程式_________,装置A中看到的现象是________。
(2)在C处看到的现象是_________,发生反应的化学方程式是________,说明反应后有________生成。
(3)本实验设计中,在B处所采取措施的目的是____________,其反应的化学方程式为__________。
(4)在给氧化铁加热时,要先通入一氧化碳气体后加热,其目的是_______。
【答案】3CO+Fe2O3![]() 2Fe+3CO2 红棕色粉末变黑 澄清的石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O 二氧化碳 既能利用一氧化碳燃烧提供能量又能防止一氧化碳污染空气 2CO+O2
2Fe+3CO2 红棕色粉末变黑 澄清的石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O 二氧化碳 既能利用一氧化碳燃烧提供能量又能防止一氧化碳污染空气 2CO+O2![]() 2CO2 排尽装置内的空气,防止加热时产生爆炸
2CO2 排尽装置内的空气,防止加热时产生爆炸
【解析】
根据已有的一氧化碳还原氧化铁的知识进行分析解答,一氧化碳能与氧化铁反应生成铁和二氧化碳,氧化铁是红色的,生成的铁粉是黑色的;生产的二氧化碳能使澄清的石灰水变浑浊;一氧化碳是有毒的气体,需要进行尾气处理,一氧化碳具有可燃性,可以进行燃烧处理,据此解答.
(1)一氧化碳能与氧化铁高温反应生成铁和二氧化碳,氧化铁是红色的粉末,铁粉是黑色的粉末,故会观察到红色粉末变黑,
故答案为:3CO+Fe2O3![]() 2Fe+3CO2;红色粉末变黑;
2Fe+3CO2;红色粉末变黑;
(2)C处的澄清石灰水变浑浊,说明有二氧化碳生成,二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,
故答案为:澄清的石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O,二氧化碳;
(3)在B处所采取措施既能利用一氧化碳燃烧提供能量,又能防止一氧化碳污染空气,一氧化碳能与氧气点燃生成二氧化碳,
故答案为:既能利用一氧化碳燃烧提供能量又能防止一氧化碳污染空气;
(4)在给氧化铁加热时,要先通入一氧化碳气体后加热,是为了排尽装置内的空气,防止加热时产生爆炸,
故答案为:排尽装置内的空气,防止加热时产生爆炸.


科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.用于新版人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质
B.芯片制造中的“光刻技术”是利用光敏树脂在曝光条件下成像,该过程并不涉及化学变化
C.纳米级的钛白可由TiCl4水解制得:TiCl4+2H2O![]() TiO2+4HCl
TiO2+4HCl
D.被誉为“中国天眼”的射电望远镜,其“眼眶”的结构钢梁属于合金材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有以下六种物质:①乙醇 ②![]() 溶液 ③
溶液 ③![]() 固体 ④液态氯化氢 ⑤纯
固体 ④液态氯化氢 ⑤纯![]() ⑥石墨,上述状态下的物质中,能导电的有___________(填序号,下同),属于强电解质的有___________。
⑥石墨,上述状态下的物质中,能导电的有___________(填序号,下同),属于强电解质的有___________。
(2)![]() 和浓盐酸常用于实验室制氯气,请用双线桥法标出电子转移方向和数目。________________
和浓盐酸常用于实验室制氯气,请用双线桥法标出电子转移方向和数目。________________
(3)配平下列化学方程式,在横线上填写化学计量数。
_________![]() _________
_________![]() _________
_________![]() =_________
=_________![]() _________
_________![]() _________
_________![]()
(4)已知反应:![]() ,当反应生成2.40gBr2时,电子转移的数目为____________。
,当反应生成2.40gBr2时,电子转移的数目为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化锰![]() 可以用作储氢材料,也能用于科学研究。以富锰渣(含60% MnO,还含有SiO2、Al2O3、CaO、FeO)为原料制备硼氢化锰的工艺流程如下。
可以用作储氢材料,也能用于科学研究。以富锰渣(含60% MnO,还含有SiO2、Al2O3、CaO、FeO)为原料制备硼氢化锰的工艺流程如下。
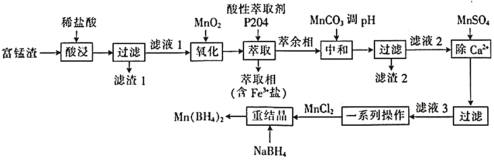
已知几种氢氧化物的Ksp 的值如下表:
氢氧化物 |
|
|
|
|
Ksp |
|
|
|
|
请回答下列问题:
(1) NaBH4中B的化合价为________价。
(2)下列物质中与滤渣1不发生反应(高温或常温下)的是________(填字母)。
A.浓硝酸 B.氢氧化钠溶液 C.碳酸钠 D.氢氟酸
(3)“氧化”中发生反应的离子方程式为________________,该反应中氧化性:![]() ________(填“
________(填“![]() ”或“
”或“![]() ”) MnO2。
”) MnO2。
(4)“中和”时,调节pH约为________。(当溶液中的离子浓度小于![]() 时,沉淀达到完全,结果保留2位有效数字)
时,沉淀达到完全,结果保留2位有效数字)
(5) Mn(BH4)2能与稀盐酸反应生成H3BO3,该反应的化学方程式为________________。
(6)测定富锰渣中铁的含量:取20g富锰渣,经过上述“酸浸”“过滤”“氧化”“萃取”后,将萃取相(假设Fe3+span>全部被萃取)转入烧杯中,加入足量稀硫酸,充分反应后静置、分液,再向含Fe3+的溶液中加入足量KI,充分反应后,将溶液配制成500mL,取25mL于锥形瓶中并加入淀粉指示剂,最后用![]() 的Na2S2O3标准液滴定,进行三次平行实验,测得消耗Na2S2O3标准液的体积如表所示。
的Na2S2O3标准液滴定,进行三次平行实验,测得消耗Na2S2O3标准液的体积如表所示。
实验次数 | 1 | 2 | 3 |
Na2S2O3标准液体积/ | 23.20 | 24.80 | 25.20 |
已知:I2+2Na2S2O3==2NaI+Na2S4O6
①滴定达到终点时溶液的颜色变化为________。
②富锰渣中铁的含量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;
②FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;
③实验②生成的溶液滴在KI试纸上,试纸变蓝
下列判断正确的是( )
A.上述实验证明氧化性:![]() >Cl2>Fe3+>I2
>Cl2>Fe3+>I2
B.上述实验中共有两个氧化还原反应
C.实验①生成的气体不能使湿润的KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“点击化学”是指快速、高效连接分子的一类反应,例如铜催化的Huisgen环加成反应:![]() +
+![]()
![]()
![]() 。我国科研人员利用该反应设计合成了具有特殊结构的化合物F。合成线路如图所示:
。我国科研人员利用该反应设计合成了具有特殊结构的化合物F。合成线路如图所示:
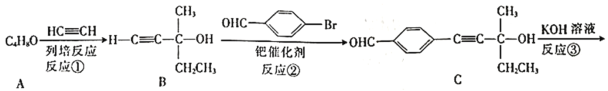
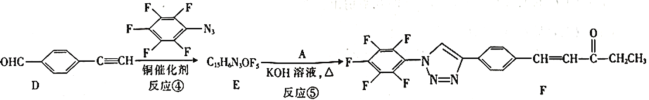
已知:![]() +
+
![]()
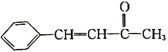 +H2O
+H2O
⑴A的名称是________。C中官能团的名称是________。
⑵反应④的反应类型为________。
⑶有机物分子中的1个碳原子上连接4个不同的原子或原子团时,该碳原子称为手性碳原子。上述流程中,存在手性碳原子的有机物有________(填字母)。
⑷反应③属于消去反应,反应③的化学方程式为________________。
⑸芳香族化合物G与C互为同分异构体,G的苯环上只有两个对位的取代基,且其中一个取代基为乙烯基(CH2=CH—)。G分子中只有两种官能团,且1molG与足量银氨溶液发生银镜反应生成4mol Ag,则G的结构有________种,其中核磁共振氢谱图中只有7组吸收峰的结构简式为________________(写出一种结构即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应A2(g)+2B2(g)![]() 2AB2(g) ΔH<0,下列说法正确的是( )
2AB2(g) ΔH<0,下列说法正确的是( )
A. 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
B. 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
C. 升高温度有利于反应速率增加,从而缩短达到平衡的时间
D. 升高温度,正向反应速率增加,逆向反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学校实验小组欲探究硫粉与铁粉的反应,并验证反应后的产物中铁元素的化合价,如图是铁粉和硫粉反应的装置图。
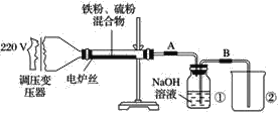
(1)将硫粉和铁粉按物质的量之比1∶1充分混合。
(2)按装置图将仪器连接好。
(3)____________。
(4)将混合物均匀地放在硬质玻璃管内。
(5)接通电源,将电压指示盘调到35 V,电炉丝很快变红,并引发左边混合物发生反应。关闭电源。
(6)将反应后的混合物冷却后加入稀硫酸中,然后取上层清液滴加硫氰酸钾溶液验证产物中铁元素的化合价。
(思考探究)
(1)步骤(3)中缺少的实验操作是什么?____。
(2)关闭电源后,反应仍继续进行的原因是什么?_____________。
(3)将盛有NaOH溶液的瓶中A、B导管位置反接是否可以?为什么?______________。
(4)某同学认为,若Fe粉与S粉反应产物中铁元素的化合价是+2价,则上述步骤(6)中的溶液不变红,你认为他的说法正确吗?__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4molA和 2molB进行如下反应:3A(g)+2B(g)![]() 4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6molC,则下列说法正确的是( )
4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6molC,则下列说法正确的是( )
A.该反应的化学平衡常数表达式是 K=![]()
B.此时,B的平衡转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加 B,平衡向右移动,B的平衡转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com