
����Ŀ�����ð�Һ������ӡˢп��ʱ����ϡ���ḯʴп���õ��ġ���Һ��(����������Cl����Fe3��)��ij��ѧ��ȤС�����á��ð�Һ����ȡZn(NO3)2��6H2O�Ĺ������£�

��֪��Zn(NO3)2��6H2O��һ����ɫ���壬ˮ��Һ�����ԣ�Zn(NO3)2����Ӧ���õ��IJ���������ԡ�
��1�����ð�Һ�������ʵ���Ҫ�ɷ���______(�ѧʽ����ͬ)��
��2�����������Ҫ�ɷ���____________��
��3���������м�����е�Ŀ����_____________���˲�����������������_______________��
��4�������ܱ���pH��2��Ŀ����____________��
���𰸡���1��Zn(NO3)2 ��2��Zn(OH)2��Fe(OH)3
��3����ʹFe3����ȫˮ�� �¶�Խ����ˮ��̶�Խ�� ��4������Zn2��ˮ��ΪZn(OH)2
��������
������������ð�Һ���к��д�����п���ӡ������ӡ���������Ӻ�������Cl����Fe3+�������������Ƶ�����Һ��PH=8ʹ�����ӡ�п������ȫ������Ȼ���ڳ������м������ܽ⣬��Һ���к��д���п���ӡ������ӡ���������Ӻ������������ӣ�������Һ��PHʹ�����ӳ�������Һ��������п��Һ�������������¼���Ũ�������ᾧ���õ�Zn��NO3��26H2O��һ����ɫ���壮��1���ð�Һ�������ʵ���Ҫ�ɷ���Zn��NO3��2��
��2�������������ƣ�Zn2+��Fe3+��ȫ����������Ӧ����������ʴ�Ϊ��Fe��OH��3��Zn��OH��2��
��3������д�ʹFe3+��ȫˮ�⣬ԭ�����¶�Խ�ߣ�ˮ��̶�Խ�ʴ�Ϊ���ٽ�Fe3+��ȫˮ�⣻ˮ�ⷴӦ���ȣ��¶ȸߣ�ˮ��̶ȴ�
��4��п������ˮ������������п�����������¿�����п���ӵ�ˮ�⣬������ܱ���pH=2��Ŀ��������Zn2+ˮ��ΪZn��OH��2��


 �ܿ�����ĩ��̾�ϵ�д�
�ܿ�����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͻ�������Ͼ�����������������ܣ���������ܵĿ���������Ҫ����
��1��һ���¶��£�ij����Ͻ�M�������������ͼ��ʾ������Ϊƽ��ʱ������ѹǿ��p���������ʾ��������ԭ�������ԭ�ӵĸ����ȣ�H/M������OA�Σ����ܽ���M���γɹ�����MHx����������ѹǿ������H/M���������AB�Σ�MHx�����������⻯��Ӧ�����⻯��MHy���⻯��Ӧ����ʽΪ��zMHx(s)+ H![]() (g)==zMHy(s) ��H(��)����B�㣬�⻯��Ӧ��������һ����������ѹǿ��H/M�������䡣��Ӧ������z=_____���ú�x��y�Ĵ���ʽ��ʾ�����¶�ΪT1ʱ��2gij�Ͻ�4min����������240mL����������v=______mLg-1min-1����Ӧ���ʱ��H(��)_____0���>����<����=����
(g)==zMHy(s) ��H(��)����B�㣬�⻯��Ӧ��������һ����������ѹǿ��H/M�������䡣��Ӧ������z=_____���ú�x��y�Ĵ���ʽ��ʾ�����¶�ΪT1ʱ��2gij�Ͻ�4min����������240mL����������v=______mLg-1min-1����Ӧ���ʱ��H(��)_____0���>����<����=����

��2���DZ�ʾ��λ��������Ͻ����⻯��Ӧ�ε����������ռ�����������ı��������¶�ΪT1��T2ʱ���ǣ�T1��____ �ǣ�T2�����>����<����=����������Ӧ������ͼ��a��ʱ�������¶Ȳ��䣬�������ϵ��ͨ�������������ﵽƽ���Ӧ�����ܴ���ͼ�е�_____�㣨�b����c����d������������Ͻ��ͨ��________��________�ķ�ʽ�ͷ�������
��3������Ͻ�ThNi5�ɴ���CO��H![]() �ϳ�CH
�ϳ�CH![]() �ķ�Ӧ���¶�ΪTʱ���÷�Ӧ���Ȼ�ѧ����ʽΪ_______ ����֪�¶�ΪTʱ��CH
�ķ�Ӧ���¶�ΪTʱ���÷�Ӧ���Ȼ�ѧ����ʽΪ_______ ����֪�¶�ΪTʱ��CH![]() (g)+2H2O=CO
(g)+2H2O=CO![]() (g)+4H
(g)+4H![]() (g) ��H=+165KJmol1
(g) ��H=+165KJmol1
CO(g)+H2O(g)=CO![]() (g)+H
(g)+H![]() (g) ��H=-41KJmol1
(g) ��H=-41KJmol1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E����Ԫ�ء��������Ϣ���£�
Ԫ�� | �����Ϣ |
A | AԪ�ص�һ��ԭ��û�����ӣ�ֻ��һ������ |
B | B�ǵ縺������Ԫ�� |
C | C�Ļ�̬ԭ��2p���������δ�ɶԵ��� |
D | DΪ����Ԫ�أ�����Eͬ���ڣ�����������������˶�״̬��ͬ�ĵ��� |
E | E���γ�ש��ɫ����ɫ����E2O��EO���������� |
�ش��������⡣
��1��д��EԪ��ԭ�ӻ�̬ʱM��ĵ����Ų�ʽ ��
��2��CԪ�ص��ʷ����к������������ļ���֮��Ϊ ��
��3��������ˮ�е��ܽ��C7H15OH���Ҵ��͵�ԭ���ǣ� ��
��4��A��C��E����Ԫ�ؿ��γɣ�E��CA3��42+�����ӣ����д��ڵĻ�ѧ�������� ������ţ���
����λ�� �������� �����Թ��ۼ� ���Ǽ��Թ��ۼ� �����Ӽ� �����
�� E��CA3��42+���жԳƵĿռ乹�ͣ��ҵ� E��CA3��42+�е�����CA3���ӱ�����Clȡ��ʱ���ܵõ����ֲ�ͬ�ṹ�IJ���� E��CA3��42+�Ŀռ乹��Ϊ ������ţ���
a��ƽ�������� b���������� c�������� d��V��
��5�����������ǻ���ɫ��״�ᾧ����ṹ��ͼ��ʾ��

������������Pԭ�Ӳ�ȡ____�ӻ�����PO3����Ϊ�ȵ�����Ļ�������ӵĻ�ѧʽΪ________����NA��ʾ�����ӵ���������ֵ��0��1mol�����������к��еŵ��Ӷ���Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ����������������й㷺���ڡ�
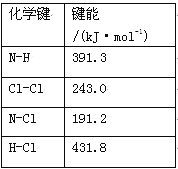
��1�����Ȱ���NH2Cl���ĵ���ʽΪ ����ͨ����ӦNH3(g)��Cl2(g)=NH2Cl(g)��HCl(g)�Ʊ��Ȱ�����֪���ֻ�ѧ���ļ�����������ʾ���ٶ���ͬ������ͬ�ֻ�ѧ���ļ���һ��������������Ӧ�Ħ�H= ��
��NH2Cl��ˮ��Ӧ����ǿ�����Ե����ʣ�������Ч�������������÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2���ý�̿��ԭNO�ķ�ӦΪ��2NO(g)+C(s) ![]() N2(g)+CO2(g)�����ݻ���Ϊ1 L�ļס��ҡ����������ݺ��£���Ӧ�¶ȷֱ�Ϊ400�桢400�桢T���������зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
N2(g)+CO2(g)�����ݻ���Ϊ1 L�ļס��ҡ����������ݺ��£���Ӧ�¶ȷֱ�Ϊ400�桢400�桢T���������зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��

���÷�ӦΪ ������ȡ������ȡ�����Ӧ��
����������200 min�ﵽƽ��״̬����0��200 min����NO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(NO)= ��
��3���ý�̿��ԭNO2�ķ�ӦΪ��2NO2(g)+2C(s)![]() N2(g)+2CO2(g)���ں��������£�1 mol NO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)���ں��������£�1 mol NO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��

��A��B�����Ũ��ƽ�ⳣ����ϵ��Kc(A) Kc(B)�������������=������
��A��B��C������NO2��ת������ߵ��� ������A������B������C��������
�ۼ���C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp(C)= ��Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E���ֶ�����Ԫ��, ���ǵ�ԭ�������������� ��֪A��Bԭ�Ӿ�����ͬ�ĵ��Ӳ���, ��A�������������Ǵ���������������, C�Ǹ�������ԭ�Ӱ뾶����Ԫ�أ� C�ĵ����ڼ�������B�ĵ��ʳ�ַ�Ӧ, ���Եõ���D������ɫ��ͬ�ĵ���ɫ��̬������,E��D���ڡ� �Ը������������ش�:
��1��Ԫ������: A C __________ E
��2��д��AB2���������������Һ��Ӧ�����ӷ���ʽ ;д�� C2B2��AB2��Ӧ�Ļ�ѧ����ʽ ;
��3������D��ԭ�ӽṹʾ��ͼ ,�õ���ʽ��ʾ������ C2D ���γɹ��� ;
��4��D��E����̬�⻯����ȶ��� ���� ���ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.05 mol Na2CO3��������ˮ���100mL��Һ������Һ�м����������ʡ��йؽ�����ȷ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B����������֪A�ķ���ʽΪC5Hmht��B�����ʽΪC5Hn(m��n��Ϊ������)����ش��������⣺
��1�����й�����A����B��˵������ȷ���� (�����)��
a.��A����B���ܻ�Ϊͬϵ��
b.��A����B���ܻ�Ϊͬ���칹��
c.��m=12ʱ����Aһ��Ϊ����
d.��n=11ʱ����B���ܵķ���ʽ��2��
��2������AΪ�������ҷ���������̼ԭ�Ӷ���ͬһ��ֱ���ϣ���A�Ľṹ��ʽΪ ��
��3������AΪ�������ҷ���������̼ԭ��һ�����棬��һ�������£�1 mol A������1 mol H2�ӳɣ���A�������� ��
��4������BΪ����ͬϵ�ȡһ��������B��ȫȼ�պ���������ͨ��������Ũ���ᣬŨ�������������1.26 g����ͨ�������ļ�ʯ�ң���ʯ�ҵ���������4.4 g������B�ķ���ʽΪ �����䱽���ϵ�һ�����ֻ��һ�֣�����ϴ���������B�� �֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������A����C��H��O����Ԫ�أ���Է�������Ϊ60������̼����������Ϊ60%�������������Ϊ13��3%��A�ڴ���Cu�������±�����������B��B�ܷ���������Ӧ����A�Ľṹ��ʽ��_________________________��
��2������֧���Ļ�����C�ķ���ʽΪC4H6O2��C����ʹBr2�����Ȼ�̼��Һ��ɫ��1 mol C��1 mol NaHCO3����ȫ��Ӧ����C�Ľṹ��ʽ��_______________��
��3��һ������ij����ͬϵ��M��ȫȼ�ա���������ͨ�������ij���ʯ��ˮ���õ���ɫ����20g������������ʯ������ȼ�ղ������11��32g������M��5�ֿ��ܵ�һ�������������Ը��������Һ������һ�������л���N������ʽΪC8H6O4����Nֻ����һ��һ������� ��M�ķ���ʽΪ____________M�Ľṹ��ʽΪ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������۾����ɼ���ϩ����������CH2��C��CH3��COOCH2CH2OH�ݵĸ߾���HEMA�Ƴɵij�����Ƭ����ϳ�·�߿����ǣ�

��֪���� ![]()
�� CH3COOCH2CH2OH������Ϊ��������������д����
��1��A��E�Ľṹ��ʽ�ֱ�Ϊ��A ��E ��
��2��д�����з�Ӧ�ķ�Ӧ���ͣ�C��D ��E��F ��
��3��д������ת���Ļ�ѧ����ʽ��
I��G ��
G+F��H ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com