
【题目】下列各组液体混合物,出现分层且水层在上层的一组物质是
A. 乙酸乙酯和水 B. 溴乙烷和水 C. 甲苯和水 D. 甲醇和水
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】冬季的降雪给机场和马路带来诸多不便,其中醋酸钾(CH3COOK)是融雪效果较好的融雪剂,下列关于醋酸钾说法正确的是
A. 1 mol CH3COOK的质量为98 g·mol-1
B. CH3COOK的摩尔质量等于它的相对分子质量
C. 一个CH3COOK微粒的质量约为![]() g
g
D. 含有6.02×1023个碳原子的CH3COOK的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A原子核中无中子且A和C同主族,A和B形成的化合物在水中呈碱性,单质D在单质E中可燃烧产生白色烟雾。回答下列问题:
(1)除B外,上述元素的电负性从大到小依次为 ;(用元素符号表示)
(2)B的氢化物与同主族第三、第四周期所形成的氢化物沸点由高到低的排列顺序是 (用化学式表示),原因是 ;
(3)A和D形成的化合物的中心原子的杂化类型为 ;A和B形成的化合物BA5中存在的化学键类型为 ;
(4)单质D的一种含氧酸可表示为H3DO3,它是二元弱酸,请写出它与足量的氢氧化钠溶液反应的离子方程式____________;
(5)C 的一种氧化物的晶胞结构如图所示,晶胞参数a=0.566 nm,晶胞中C原子的配位数为 ;此晶体的密度(g·cm-3)为 (只列式不计算)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z 为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:
Y+X→甲(g),Y+Z→乙(g)。甲为10电子分子,Z为黄绿色气体。甲、乙可化合生成离子化合物。
(1)X 的电子式是______________。
(2)写出Y+X→甲(g)的化学方程式_____________________。
(3)向一定浓度的 BaCl2溶液中通入 SO2气体,未见沉淀生成,若在通入 SO2气体的同时加入或通入某纯净物(从X、Y、Z、甲、乙中选择),即可生成白色沉淀,该纯净物的化学式为________,生成的白色沉淀的化学式为___________。
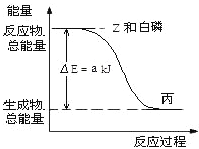
(4)已知常温下,PCl3为液体,PCl5为固体。白磷(P4)在Z气体中燃烧生成液态丙分子,白磷固体和 Z 气体反应,生成1 mol液态丙时,能量变化如图所示,写出该反应的热化学方程式_______________。
已知1 mol白磷固体和Z气体反应,生成固态丁时,放热b kJ,则1 mol固态丁转化为液态丙时的反应热ΔH=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4在实验室和工业生产中有广泛用途。
Ⅰ.某小组拟用酸性KMnO4溶液与H2C2O4溶液(弱酸)的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010 mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)
物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010 mol/L KMnO4溶液)/mL | m(MnSO4固体)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.0 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
回答下列问题:
(1)完成上述反应原理的离子反应方程式_______________________。
(2)上述实验①②是探究____________对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则a为___________;乙是实验需要测量的物理量,则表格中“乙”应填写___________;上述实验②④是探究_________对化学反应速率的影响。

Ⅱ.某化学小组利用如图装置进行实验证明氧化性:KMnO4>Cl2>Br2。限选试剂:KBr溶液、KMnO4、浓盐酸、浓硫酸。
(3)装置d中观察到的现象为____________________;此实验装置的不足之处是无尾气吸收装置,请写出处理尾气的离子方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】U常见化合价有+4和+6。硝酸铀酰[UO2(NO3)2]加热可发生如下分解:
[UO2(NO3)2]―→UxOy+NO2↑+O2↑(未配平)
将气体产物收集于试管中并倒扣于盛水的水槽中,气体全部被吸收,水充满试管。则生成的铀的氧化物化学式是( )
A.UO2 B.2UO2·UO3
C.UO3 D.UO2·2UO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰(MnSO4·H2O)是一种粉色晶体,易溶于水,不溶于乙醇,是重要的微量元素肥料之一,可促进多种经济作物生长从而增加其产量。甲、乙两组同学拟制取硫酸锰并探究其性质。
(1)甲组同学拟制备MnSO4·H2O。
首先称取5.0gMnO2于200mL烧杯中,加入12.00mL6.00mol/L硫酸和6.00mLH2O。然后再称取8.0g草酸晶体[H2C2O4·2H2O],将溶液稍加热后,在搅拌下缓慢向烧杯中分批加入草酸晶体粉末。待充分反应后过滤得到浅粉色溶液,将溶液蒸发浓缩,加入适量乙醇冷却结晶,干燥后得MnSO4·H2O。
①实验中配制100mL6.00mol/L硫酸时,需要的仪器有量筒、烧杯、玻璃棒、胶头滴管和____________。
②在上述过程中,若MnO2的转化率为97.44%,则最终得到MnSO4·H2O晶体的质量为____________g。
(2)乙组同学拟研究硫酸锰的高温分解产物,用下图装置测量生成的Mn3O4、SO2、SO3及水蒸气。

①装置正确的连接顺序为_________________(按气流方向,填装置序号)。
②实验自始至终均需通入N2,其目的是______________。
③若起始时,在装置Ⅱ中加入MnSO4·H2O50.7g,充分反应后,测得装置Ⅲ增重6.4g,则MnSO4·H2O分解的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】γ-Fe2O3在磁性、催化、气敏等方面用途非常广泛,以硫铁矿烧渣(含Fe2O3、SiO2、CaO、Al2O3等)为原料生产γ-Fe2O3的流程如下:

(1)“还原焙烧”时,焦炭的作用是______________,起还原作用的主要物质是__________(填化学式)。
(2)“浸取”时,为提高铁的浸取率,可采取的措施除粉碎焙烧后的熔体、适当增大硫酸的用量外,还可采取的措施有______________(任写一条)。
(3)“过滤”前,将溶液的pH调至5~5.5的目的是将Al3+转化为___________(填化学式)。
(4)“缓慢干燥”生成铁黄的化学方程式为_____________。
(5)经上述流程制得的γ-Fe2O3中含有少量FeO和Al2O3杂质,某课题小组称取8.1380gγ-Fe2O3样品,溶于100mL2.00mol/LH2SO4溶液中,完全溶解后加入过量H2O2溶液,然后加入1.00mol/L的NaOH溶液,生成固体的质量与加入NaOH溶液体积的关系如图,则该样品中γ-Fe2O3的百分含量为___________(百分数保留到小数点后两位)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念。在该工艺中,理想状态是反应中原子全部转化为目标产物,即原子利用率为100%。利用以下各种化学反应类型的合成过程最符合绿色化学的是
A. 取代反应 B. 水解反应 C. 加聚反应 D. 酯化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com