
【题目】某溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子.向该溶液中滴加NaOH溶液,生成沉淀的物质的量变化曲线如右图所示.下列有关判断正确的是
等离子.向该溶液中滴加NaOH溶液,生成沉淀的物质的量变化曲线如右图所示.下列有关判断正确的是![]()
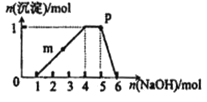
A.m点处反应:![]()
B.p点:![]()
C.若取原溶液做焰色反应实验,焰色应为黄色
D.原溶液中存在的主要离子:![]()
【答案】D
【解析】
由图可知,开始加入NaOH没有沉淀和气体产生,则一定有![]() ;后来有沉淀产生且最后完全消失,则一定没有
;后来有沉淀产生且最后完全消失,则一定没有![]() ,一定含有
,一定含有![]() ;中间段沉淀的质量不变,应为
;中间段沉淀的质量不变,应为![]() 的反应,则含有
的反应,则含有![]() ,由电荷守恒可知一定含有
,由电荷守恒可知一定含有![]() ,
,
A.m点后沉淀的量逐渐增加,发生反应为![]() ,选项A错误;
,选项A错误;
B.p点溶质为一水合氨和硫酸钠,氢氧根离子来自水的电离和一水合氨的电离,则![]() ,选项B错误;
,选项B错误;
C.根据分析可知,无法确定是否含有![]() ,则取原溶液做焰色反应实验,焰色不一定为黄色,选项C错误;
,则取原溶液做焰色反应实验,焰色不一定为黄色,选项C错误;
D.开始加入1molNaOH时,溶液无沉淀产生,说明溶液中有![]() ,且其物质的量为1mol;产生沉淀和沉淀溶解所需的NaOH的物质的量为3:1,所以溶液中有
,且其物质的量为1mol;产生沉淀和沉淀溶解所需的NaOH的物质的量为3:1,所以溶液中有![]() 且其物质的量为1mol;当加入
且其物质的量为1mol;当加入![]() 时,发生的反应为
时,发生的反应为![]() ,所以溶液中
,所以溶液中![]() 为1mol,则原溶液中
为1mol,则原溶液中![]() ,选项D正确;
,选项D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是
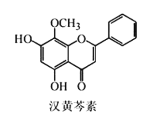
A.汉黄芩素的分子式为C16H13O5
B.该物质能与Na2CO3溶液反应,遇FeCl3溶液显色
C.1mol该物质与溴水反应最多可与2molBr2发生加成反应
D.该分子最多能与6molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数。
(1)在CB3分子中C元素原子的原子轨道发生的是____杂化,CB3分子的空间构型为____。
(2)C的氢化物极易溶于水的原因是____。
(3)D元素与同周期相邻元素的第一电离能由大到小的关系是:____(用元素符号表示);
(4)氧原子的价层电子的轨道表示式为____。
(5)X与Y所形成化合物晶体的晶胞如图所示。
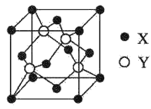
①在一个晶胞中,X离子的数目为____;
②若该化合物的密度为ag·cm-3,则晶胞的体积是____cm3(只要求列出计算式,阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制变量法是化学实验的一种常用方法。下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题。

(1)化学反应速率本质上是由_____________ 决定的,但外界条件也会影响反应速率的大小。本实验中实验2和实验3表明_____________ 对反应速率有影响,该因素对反应速率的具体影响是其他条件相同时,_____________反应速率越快。
(2)我们选取实验_____________(填实验序号)研究锌的形状对反应速率的影响。我们发现在其他条件相同时,反应物间的_____________反应速率越快。
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少硫酸铜溶液,发现反应速率明显加快,原因是 _____________。
(4)利用表中数据,可以求出硫酸的物质的量浓度是_____________![]() (计算结果精确到小数点后一位)。
(计算结果精确到小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列8种与人们生产生活相关的有机物:① HCHO(防腐剂)② CH3CH2CHO(化工原料)③CH3CH2CH2CH3(打火机燃料)④ ![]() (冷冻剂)⑤
(冷冻剂)⑤ ![]() (汽车防冻液)⑥
(汽车防冻液)⑥ ![]() (杀菌剂)⑦
(杀菌剂)⑦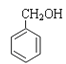 (定香剂)⑧
(定香剂)⑧ ![]() (汽油添加剂)请回答:
(汽油添加剂)请回答:
(1)属于醇的是____(填序号,下同)。
(2)互为同系物的是_____。
(3)互为同分异构体的是__。
(4)用系统命名法给④命名,其名称为_____。
(5)写出②与银氨溶液发生银镜反应的化学方程式__。
(6)写出⑧与浓硝酸反应生成TNT的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 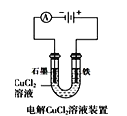 中阳极处能产生使湿润淀粉KI试纸变蓝的气体
中阳极处能产生使湿润淀粉KI试纸变蓝的气体
B. 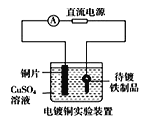 中待镀铁制品应与电源正极相连
中待镀铁制品应与电源正极相连
C. 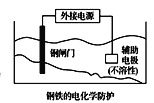 中钢闸门应与外接电源的正极相连,称为牺牲阳极的阴极保护法
中钢闸门应与外接电源的正极相连,称为牺牲阳极的阴极保护法
D. 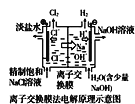 中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛的化合物如TiO2、Ti(NO3)4、TiCl4、 Ti(BH4)2等均有着广泛用途。
(1)写出Ti的基态原子的外围电子排布式____________。
(2)TiCl4熔点是-25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于_____晶体;BH4-中B原子的杂化类型为____________;
(3)在 TiO2催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子化学式为_________________。
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2H2O(绿色),两者配位数_____(填“相同”或“不同”),绿色晶体中配体是______。

(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为____________。
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为![]() g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)乙醇—氧气燃料电池是一种清洁能源,该电池用金属铂片插入氢氧化钾溶液中作电极,在两极区分别加入乙醇和氧气,其负极反应式为:_____________。
(2)古代铁器(埋藏在地下)在严重缺氧的环境中,仍然锈蚀严重。原因是一种叫做硫酸盐还原菌的细菌,能提供正极反应的催化剂,可将土壤中的![]() 还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。①写出该电化学腐蚀的正极反应式:____________。
还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。①写出该电化学腐蚀的正极反应式:____________。
②文物出土前,铁器表面的腐蚀产物可能有(写化学式)____________。
(3)对金属制品进行抗腐蚀处理,可延长其使用寿命。以下为铝材表面处理的一种方法:
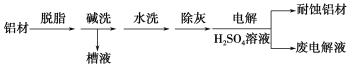
①碱洗的目的是除去铝材表面的自然氧化膜。碱洗时常有气泡冒出,原因是(用离子方程式表示):____________。
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为:____________。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是____________。
(4)采用石墨电极电解CuSO4溶液一段时间后,向所得溶液中加入0.1molCu(OH)2后,恰好使溶液恢复到电解前的浓度。则电解过程中通过导线的电量为____________C(已知NA=6.02×1023mol—1,1个电子所带的电量为1.60×10-19C)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com