
【题目】含C、N化合物在生产、生活中有着重要的作用。请按要求回答下列问题。
N在元素周期表中的位置:______________。
元素C、N最简单气态氢化物的稳定性强弱比较(填化学式): ____________.
I.氨气应用于侯德榜制碱工艺,原理如下图所示:
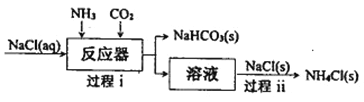
(1)过程i通入NH3和CO2的顺序是___________。
(2)过程ii有利于析出更多NH4Cl(s)的原因是_____________。
(3)制碱副产品NH4Cl可用于生产NH3和HCl。但直接加热分解NH4Cl, NH3和HCl的产率很低,原因是(用化学方程式表示)_________________。 而采用在N2氛围中,将MgO与NH4Cl混合加热至300℃,可获得高产率的NH3,该反应的化学方程式为____________。
Ⅱ.电镀工业中含CN-的废水在排放前的处理过程如下:
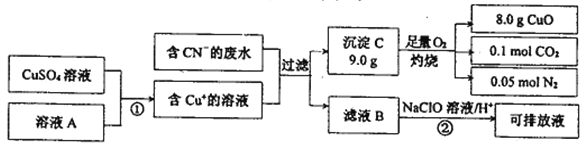
(1)溶液A具有的性质是(填“氧化性”或“还原性”) _______. C的化学式为:______。
(2)反应② 可将CN一转化为无害物质,其离子方程式为:_____________。
【答案】 第二周期VA族 CH4<NH3 先通NH3,后通CO2 NH4Cl(s)![]() NH4+(aq)+Cl-(aq),增大c(Cl-),平衡左移,促进NH4Cl析出 NH3+HCl= NH4Cl MgO+2NH4Cl
NH4+(aq)+Cl-(aq),增大c(Cl-),平衡左移,促进NH4Cl析出 NH3+HCl= NH4Cl MgO+2NH4Cl ![]() 2NH3+MgCl2+H2O↑ 还原性 CuCN 2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O
2NH3+MgCl2+H2O↑ 还原性 CuCN 2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O
【解析】N的原子序数是7,在元素周期表中的位置是第二周期VA族;氮元素非金属性强于碳元素,非金属性越强,氢化物越稳定,则稳定性是CH4<NH3。
I.(1)氨气极易溶于水,CO2在水中的溶解度很小,因此过程i要首先通入NH3,然后再通入CO2。(2)溶液中存在:NH4Cl(s)![]() NH4+(aq)+Cl-(aq),加入氯化钠固体,增大c(Cl-),平衡左移,从而促进NH4Cl析出。(3)加热分解NH4Cl生成的NH3和HCl冷却后又转化为氯化铵,从而得不到氨气,方程式为NH3+HCl= NH4Cl。而采用在N2氛围中,将MgO与NH4Cl混合加热至300℃,可获得高产率的NH3,根据原子守恒可知还有氯化镁和水生成,该反应的化学方程式为MgO+2NH4Cl
NH4+(aq)+Cl-(aq),加入氯化钠固体,增大c(Cl-),平衡左移,从而促进NH4Cl析出。(3)加热分解NH4Cl生成的NH3和HCl冷却后又转化为氯化铵,从而得不到氨气,方程式为NH3+HCl= NH4Cl。而采用在N2氛围中,将MgO与NH4Cl混合加热至300℃,可获得高产率的NH3,根据原子守恒可知还有氯化镁和水生成,该反应的化学方程式为MgO+2NH4Cl ![]() 2NH3↑+MgCl2+H2O。
2NH3↑+MgCl2+H2O。
Ⅱ.(1)反应中铜离子得到电子转化为亚铁离子,这说明溶液A具有还原性。9.0g沉淀C在氧气中灼烧后,产生8.0g CuO,物质的量为8g÷80g/mol=0.1mol,0.1molCO2,碳元素质量为0.1mol×12g/mol=1.2g,氮气的物质的量为0.05mol,质量是1.4g,CuO的C、N、Cu元素总质量为1.2g+1.4g+0.1mol×64g/mol=9g,等于沉淀C的质量,故C由Cu、C、N三种元素组成,且三原子物质的量之比为0.1mol:0.1mol:0.05mol×2=1:1:1,故C的化学式为CuCN。(2)反应② 可将CN一转化为无害物质,应该是氮气和CO2,则其离子方程式为2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
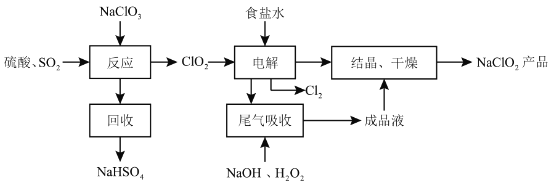
回答下列问题:
(1)NaClO2中![]() 的化合价为__________。
的化合价为__________。
(2)写出“反应”步骤中生成![]() 的化学方程式____________。
的化学方程式____________。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去![]() 和
和![]() ,要加入的试剂分别为__________、__________。
,要加入的试剂分别为__________、__________。
(4)“尾气吸收”是吸收“电解”过程排出的少量![]() ,此吸收反应中,氧化剂与还原剂的物质的量之比为__________,该反应中氧化产物是____________。
,此吸收反应中,氧化剂与还原剂的物质的量之比为__________,该反应中氧化产物是____________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克![]() 的氧化能力。
的氧化能力。![]() 的有效氯含量为____________。(计算结果保留两位小数)。
的有效氯含量为____________。(计算结果保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3.9克的镁铝合金,投入到500mL 2mol/L的盐酸中,金属完全溶解,再加入4mol/L的氢氧化钠溶液,若要生成沉淀最多,加入这种氢氧化钠溶液的体积是()
A.125mL B.200mL C.250mL D.560mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列物质①NaCl晶体 ②液态SO2 ③纯醋酸④硫酸钡 ⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KNO3 ⑧NaOH溶液 ⑨氨水 请用以上物质回答下列问题(填序号)。
在上述状态下能导电的强电解质是__________________; 属于弱电解质的是________________;属于非电解质,但溶于水后的水溶液能导电的是_________________。
(2)化学平衡移动原理同样也适用于其他平衡,已知在氨水中存在下列平衡:NH3·H2O ![]() NH4++OH-。
NH4++OH-。
①向氨水中加入NH4Cl固体时,平衡____________移动,(填“向右”或“向左”),c(OH-)____(填“增大”或“减小”,下同),c(NH4+)______。
②向氨水中加入MgCl2固体时,平衡_____移动,(填“向右”或“向左”),c(OH-)____(填“增大”或“减小”,下同),c(NH4+)_________。
③升高温度,c(OH-)______(填“增大”或“减小”,下同),c(NH4+)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 298K时,反应2Mg(s)+CO2(g)===C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
B. 电解法精炼铜时,粗铜作阳极,精铜作阴极
C. 在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
D. 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明某溶液只含有Fe2+而不含有Fe3+的实验方法是
A.先滴加氯水,再滴加KSCN溶液后显红
B.只需滴加KSCN溶液
C.先滴加KSCN溶液,不显红色,再滴加氯水后显红色
D.加Na2O2固体后观察沉淀颜色的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用40gNaOH固体溶于水配制成250ml溶液,此溶液的物质的量浓度是____,取该溶液10ml,再加水稀释成100ml时,所得稀溶液的物质的量浓度为___,在这100ml溶液中含____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com