
【题目】碱性锌锰电池的反应方程式为: 2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2,其构造如图所示。有
关说法不正确的是
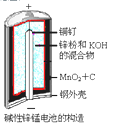
A. 负极反应式:Zn+2OH--2e-=Zn(OH)2
B. 放电时正极MnO2得到电子,发生氧化反应
C. 该电池使用一段时间后,电解液pH增大
D. 放电时,锌粉失去的电子,从负极通过外电路流向正极
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】已知:还原性强弱:I﹣>Fe2+ . 往100mL碘化亚铁溶液中缓慢通入3.36L(标准状况)氯气,反应完成后溶液中有一半的Fe2+被氧化成Fe3+ . 则原碘化亚铁溶液的物质的量浓度为( )
A.0.12molL﹣1
B.0.1molL﹣1
C.1.2molL﹣1
D.1.0molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(七水合硫酸亚铁)和胆矾晶体,以探索工业废料的再利用.其实验方案如下:试回答下列问题:

(1)写出合金溶于试剂①溶液时相关反应的离子方程式 ____________________________,操作②的名称是 ______________ 。
(2)滤液A中通入过量气体的离子反应方程式为_______________________________,由滤液A制AlCl3溶液有途径I和途径II两种,与途径I相比,途径II存在着明显的缺陷是: _________________________________________________________。
(3)溶液E中的主要溶质为 _____________________ ;如何检验滤液E是否已被氧化(写出操作过程、现象和结论) _______________________________________________。
(4)按环保要求,写出用滤渣F制备硫酸铜溶液的各步反应的化学方程式 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如图所示,试回答: 
(1)a点之前的反应的离子方程式为 .
(2)a点到b点之间的反应的离子方程式是、 .
(3)c点二氧化碳体积是L.
(4)混合稀溶液中Ba(OH)2和NaOH的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氮及其化合物的说法正确的是
A. 硝酸氧化性强,不能用铁或铝制容器贮运
B. 氮氧化合物与“光化学烟雾”、“臭氧空洞”的形成有关
C. 氮的固定只有在高温、高压、有催化剂存在的条件下才能实现
D. 实验室可用NH4Cl和石灰水制取氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据生活经验,判断下列物质或其水溶液按pH的一定顺序依次排列正确的是( )
A.“84”消毒液、洁厕灵、食盐、可乐
B.可乐、洁厕灵、食盐、“84”消毒液
C.洁厕灵、可乐、食盐、“84”消毒液
D.洁厕灵、食盐、可乐、“84”消毒液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 在任何条件下,1mol任何气体的体积都约是22.4L
B. 化学的特征就是认识分子和制造分子
C. 在化学反应中,反应物的物质的量之和一定等于生成物的物质的量之和。
D. 英国科学家道尔顿提出元素周期律,把化学元素及其化合物纳入一个统一的理论体系。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaOH溶液与CuSO4溶液加入某病人的尿液中,微热时如果观察到红色沉淀,则说明该病人的尿液中含有
A. 乙酸 B. 乙醇 C. 氯化钠 D. 葡萄糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com