
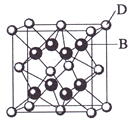
【题目】已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。
请回答:
(1)A元素的名称是 ;
(2)B的元素符号是 ,C的元素符号是 ,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
(3)E属元素周期表中第 周期,第 族的元素,其元素名称是 , 它的+2价离子的电子排布式为 :
(4)从图中可以看出,D跟B形成的离子化合物的化学式为 ;该离子化合 物晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出算式)。
【答案】(1)氢 (2)F Cl 氟化氢分子间存在氢键,氯化氢分子间没有氢键
(3)四 ⅦB 锰 1s22s22p63s23p63d5
(4)CaF2![]()
【解析】从D、E是周期表中1-18列中E排第7列可判断E是第4周期VIIB族的Mn元素,原子序数为25,所以D也在第4周期,D的原子序数比E小5,则原子序数为20,应为Ca元素,图中离子化合物D与B的离子个数比值为:(8×1/8+6×1/2):8=1:2,且D为Ca,则B的化合价为-1价,应为第ⅦA族元素,B和C属同一主族,B的序数在前面,B为F,C为Cl;A与其他4种元素既不在同一周期又不在同一主族,所以A为H。
(1)A为H元素,名称为氢;(2)B为F元素,C为Cl元素,HF中含有氢键,分子间的作用力较强,沸点较高;(3)E为Mn元素,位于周期表第四周期第七列,则应位于VIIB族,原子的核外电子的排布式为1s22s22p63s23p63d54s2,失去2个电子 ,离子的电子排布式为 1s22s22p63s23p63d5;(4)从图中可以看出,晶胞中含有Ca的离子个数为8×1/8+6×1/2=4,含有F的离子个数为8,二者比值为1:2,则化学式为CaF2,晶胞中:ρ=m/V=  ,则V=
,则V=![]() 。
。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成,其中C中有两种阳离子:

为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出C、D的化学式:C________,D________。
(2)将含1 mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为___________。
(3)在A溶液中加入少量澄清石灰水,其离子方程式为_____________________________。
(4)若向含溶质l mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为_______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法能达到目的是
A. 用焰色反应鉴別Na2CO3溶液和NaCl溶液
B. 用分液漏斗分离食醋中的乙酸与水
C. 用结晶的方法分离氯化钠和硝酸钾的混合物
D. 用NaOH溶液除去Cl2中混有的少量HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为________________________________________________________________________。
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是________________________________________________________________________。
(3)SO![]() 中S以sp3杂化,SO
中S以sp3杂化,SO![]() 的立体构型是________。
的立体构型是________。
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,金原子最外层电子排布式为____________。一种铜合金晶体具有立方最密堆积的结构,在晶胞中铜原子处于面心,金原子处于顶点位置,则该合金中铜原子与金原子数量之比为________;该晶体中,原子之间的作用力是________________________________________________________________________。
(5)CuSO4晶体的构成微粒是________和________,微粒间的作用力是________,该晶体属于________晶体。
(6)上述晶体具有储氢功能,氢原子可进入到由铜原子与金原子构成的四面体空隙中。若将铜原子与金原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似,该晶体储氢后的化学式应为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机花儿会务X(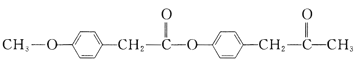 )是有机精细化工的重要中间体,实验室中以M(
)是有机精细化工的重要中间体,实验室中以M(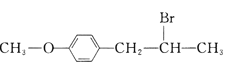 )为原料合成X的路线如下:
)为原料合成X的路线如下:
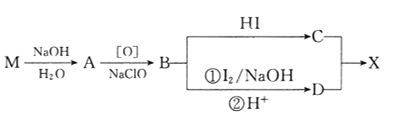

回答下列问题:
(1)B的核磁共振氢谱上有________组峰。
(2)D分子中含有的官能团有_________________________。(填名称)
(3)下列常见含钠试剂能与C反应的有______________。(填标号)
a.氯化钠 b.氢氧化钠 c.纯碱 d.碳酸氢钠
(4)由B转化为C的化学方程式为______________________________,该反应的反应类型是_______________________。
(5)E是D的同分异构体,在苯环的对位上各有一个取代基,能够发生银镜反应和水解反应,1molE与足量钠反应可生成0.5molH2,则E可能的结构有_____种。
(6)有机物F(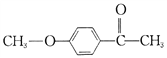 )也是一种重要的有机精细化工中间体,写出由
)也是一种重要的有机精细化工中间体,写出由 ![]() 制备F的合成路线。(其他试剂任选;已知马氏规则:在不对称烯烃的加成反应中,氢原子总是加在含氢较多的碳原子上。如:
制备F的合成路线。(其他试剂任选;已知马氏规则:在不对称烯烃的加成反应中,氢原子总是加在含氢较多的碳原子上。如:![]() )_________________.
)_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1949年度诺贝尔化学奖授予为研究臭氧做出贡献的化学家。臭氧能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图:呈V形,键角116.5°。三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子提供1个电子,构成一个特殊的化学键(虚线内部分)——三个O原子均等的享有着4个电子。请回答:
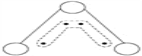
(1)题中非极性共价键是__键,特殊的化学键是 键。
(2)臭氧与氧气是_____。
(3)下列物质的分子与O3分子的结构最相似的是_______。
A.H2O B.CO2 C.SO2 D.BeCl2
(4)子中某一原子有1对没有跟其他原子共用的电子叫孤电子对,那么 O3分子有___对孤电子对。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“胃舒平”的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·nH2O)等化合物。下列叙述中错误的是( )
A. 镁元素基态原子的核外电子排布式是:1s22s22p63s2
B. 铝元素原子核外共有5种不同运动状态的电子
C. 钠元素离子半径比铝离子半径大
D. 金属铝与钠的最高价氧化物的水化物溶液发生反应的离子方程式为2Al+2OH-+2H2O===2AlO+3H2↑
【答案】B
【解析】试题分析:A.镁元素基态原子的核外电子排布式是:1s22s22p63s2,A正确;B.铝元素原子核外共有13种不同运动状态的电子,B错误;C.钠元素离子半径比铝离子半径大,C正确;D.金属铝与钠的最高价氧化物的水化物溶液发生反应的离子方程式为2Al+2OH-+2H2O===2AlO+3H2↑,D正确,答案选B。
考点:考查核外电子排布、微粒半径等有关判断
【题型】单选题
【结束】
17
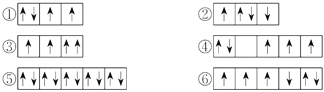
【题目】(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况,试判断哪些违反了泡利原理__________,哪些违反了洪特规则__________。
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为__________;其最高价氧化物对应水化物的化学式是__________。
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列。
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com