
【题目】NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如左图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如右图![]() 下列说法正确的是
下列说法正确的是
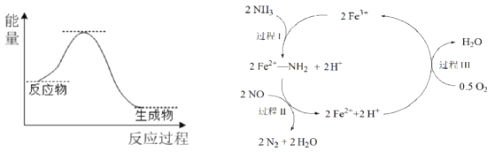
A.NH3催化还原NO为吸热反应
B.过程Ⅰ中NH3断裂离子键
C.过程Ⅱ中NO为氧化剂,Fe2+为还原剂
D.脱硝的总反应为:4NH3(g)+4NO(g)+O2(g) ![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法正确的是

A.用澄清的石灰水可鉴别NaHCO3和Na2CO3
B.溴元素在第③、⑤中被氧化,在第④中被还原
C.工业上一般用金属钠与无水MgCl2反应制取Mg单质
D.海水中还含有碘元素,只需将海水中的碘升华就可以得到碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其制备途径及性质如图所示(假设恰好完全反应)。下列说法正确的是
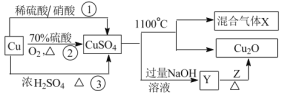
A.途径①所用混酸中,H2SO4与 HNO3物质的量之比为2:3
B.1molCuSO4在 1100℃所得混合气体中,O2为 0.75mol
C.Z 只能是葡萄糖
D.相对于途径①、③,途径②更好地体现了绿色化学思想
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋为第五周期VA族元素,利用湿法冶金从辉铋矿(含Bi2S3、Bi、Bi2O3等)提取金属铋的工艺流程如下图所示:
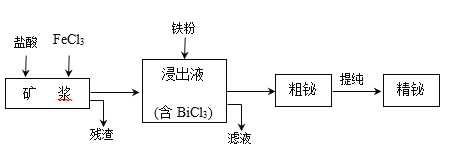
已知:BiCl3水解的离子方程式为:BiCl3+H2O![]() BiOCl+2H++2Cl。
BiOCl+2H++2Cl。
(1)矿浆浸出时加入盐酸的作用是____。
(2)浸出时,Bi溶于FeCl3溶液的化学方程式为____。
(3)残渣中含有一种单质,该单质是_______。
(4)滤液的主要溶质是(化学式)_____,该物质可在工艺中转化为循环利用的原料,转化的反应方程式为____。
(5)精辉铋矿中含有Ag2S,被氧化溶解后不会进入浸出液,银元素以______(填化学式)进入残渣中。
(6)粗铋电解精炼时应放在_______极。
(7)某温度下饱和的Ag2S溶液中,银离子的浓度为10-4mol/L,且Ag2S的KSP=5.8×10-39,则此溶液中硫离子的浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质互为同分异构体的是( )
A. CH3—CH3和CH3—CH2—CH3
B. 12C和14C
C. CH3—CH2—CH2—CH3和(CH3)2CHCH3
D. 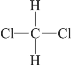 和
和 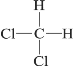
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种有机物,它们的分子分别由—CH3、—OH、—COOH、—CHO、—C6H5( 代表苯基)中的两种组成,这些化合物的性质如下所述:
①A能够发生银镜反应,且相对分子质量为44;
②B溶液加入氯化铁溶液中,溶液显紫色;
③C和E在有浓硫酸存在并加热的条件下,能发生酯化反应,C和E的相对分子质量之比为8:15;
④B和E都能跟氢氧化钠溶液反应,而A、C、D则不能;
⑤D属于烃类,且D能使酸性高锰酸钾溶液褪色,还能发生硝化反应。
请回答下列问题:
(1)B、D的结构简式是:B_____D______
(2)写出A发生银镜反应的化学方程式:________
(3)C和E发生酯化反应的化学方程式:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
A. 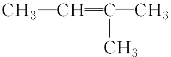 ―→
―→
B. CH2===CH—CH2—CH3+HCl![]()
C. CH3—CH===CH2+H2O![]()
D. nCH2===CH2+nCH2===CH—CH3![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组设计实验对硫燃烧的产物及其性质进行验证,实验装置如下图所示。
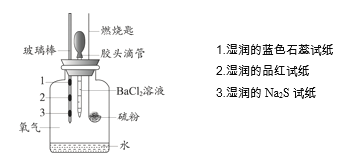
下列实验事实与所得结论相符的是
实验事实 | 所得结论 | |
A | 湿润的品红试纸褪色 | 证明硫燃烧的产物中有SO2 |
B | 湿润的Na2S试纸上出现淡黄色固体 | 证明硫的燃烧产物能被还原成硫 |
C | 湿润的蓝色石蕊试纸变红 | 证明硫的燃烧产物中有酸类物质 |
D | 加入BaCl2溶液产生白色沉淀 | 证明硫燃烧的产物中有SO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期主族元素。通常状况下,X与W元素均能形成-1价的气态氢化物,Y为同周期主族元素中原子半径最大的元素,X、Z和W的原子最外层电子数之和为20。回答下列问题:
(1) W在元素周期表中的位置是__________。
(2)X和Y元素简单离子的半径较大的是________(填离子符号);Z和W元素气态氢化物的稳定性较弱的是__________(填化学式)。
(3)Y的氧化物中既含离子键又含共价键的是__________(用电子式表示)。
(4)Z的最高价氧化物对应水化物的浓溶液(过量)和氧化亚铜共热,反应的化学方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com