
【题目】不具有放射性的同位素称为稳定同位素,如2H、13C、15N、18O、34S等,在陆地生态系统研究中常被用作环境分析指示物。下列说法中正确的是( )
A.18O原子核内的质子数为16
B.12C32S2比12C34S2更易挥发
C.13C和15N原子核内的质子数相差2
D.2H+的氧化性比1H+的氧化性强
科目:高中化学 来源: 题型:
【题目】有一包白色固体物质,可能含有CuSO4、K2SO4、Na2CO3、Ca (NO3)2 、KCl 中的一种或几种。将该白色固体少量溶于水中,得到无色透明溶液,取100 mL该溶液先滴加足量硝酸钡溶液,再滴加足量稀硝酸,实验过程中沉淀质量的变化如图所示:

(1)由此可知,该白色固体中一定含有 ,一定没有 。
(2)实验过程中发生有关反应的化学方程式: 。
(3)请设计实验证明可能有的物质是否存在 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
①碳元素参与生物体内所有化合物的组成
②地球上的生命是在碳元素的基础上建立起来的
③碳元素是各种大分子化合物中数量最多的元素
④碳元素是组成生物体有机化合物的最基本元素
A. ②③④ B. ③④ C. ①②④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据物质的量的有关公式计算(注:(2)(3)(4)计算结果保留小数点后两位)
(1)3.01×1023个NH4+,其质量为 g。
(2)欲配制1L 0.2 mol.L-1的盐酸溶液,需标准状况下HCl的体积为 L。
(3)现将50 mL密度为1.84 g/cm3,质量分数为98.0 %的浓硫酸,稀释至250 mL,则稀释后,溶液的物质的量浓度为 。
(4)19克MgCl2中含有离子数目 。
(5)所含原子数相等的甲烷和氨气(NH3)的质量比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g) + H2O(g) ![]() CO2(g) + H2(g)△H<0。CO和H2O(g)浓度变化如右图
CO2(g) + H2(g)△H<0。CO和H2O(g)浓度变化如右图
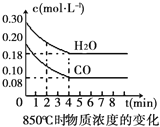
(1)0~4min的平均反应速率v(CO)=___________molL-1min-1.
(2)该条件下,此反应的平衡常数K=___________(写表达式).
(3)该反应平衡时CO的转化率为________________。
(4)能判断该反应达到化学平衡状态的依据是______________。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
(5)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表.
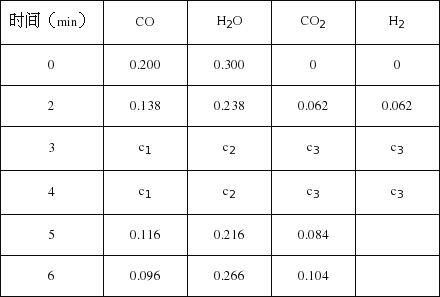
① c1数值___________0.08molL-1(填大于、小于或等于).
②反应在4min~5min间,平衡向逆方向移动,可能的原因是________________,表中5min~6min之间数值发生变化,可能的原因是_______________。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下:
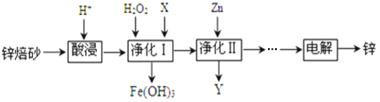
回答下列问题:
(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
① ZnFe2O4中Fe的化合价是___________,从物质分类角度说,ZnFe2O4属于__________(填“酸”、“碱”或“盐”)。
② 工业上利用反应ZnFe2(C2O4)3·6H2O![]() ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是______________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是______________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。
(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是___________(任答一条);已知ZnFe2O4能溶于酸,则酸浸后溶液中存在的金属离子有______________。
(3)净化Ⅰ中H2O2参与反应的离子方程式为_______________;试剂X的作用是___________。
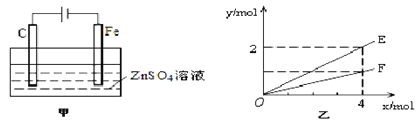
(4)钢铁镀锌是钢铁防护的一种有效方法。按图甲装置进行模拟铁上镀锌的实验,实验结果如图乙所示。乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量。
① C电极的电极反应式为________________________。
② E可以表示的量是_________________________(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49%
B.配制0.1mol/L的Na2CO3溶液480mL,需用500mL容量瓶
C.在标况下,将22.4L氨气溶于1 L水中,得到1mol/L的氨水
D.向两等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com