
【题目】已知25 ℃、101 kPa时,1 mol H2与溴蒸气完全反应生成气态溴化氢放出能量Q kJ,则下列热化学方程式书写正确的是 ( )。
A.H2(g)+Br2(g)=2HBr(g) ΔH=-2Q kJ·mol-1
B.H2(g)+Br2(l)=2HBr(g) ΔH=-Q kJ·mol-1
C.![]() H2(g)+
H2(g)+![]() Br2(g)=HBr(g)ΔH=+
Br2(g)=HBr(g)ΔH=+![]() kJ·mol-1
kJ·mol-1
D.HBr(g)=![]() H2(g)+
H2(g)+![]() Br2(g)ΔH=+
Br2(g)ΔH=+![]() kJ·mol-1
kJ·mol-1
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,已知:四种原了最外层电子数之和为24。下列说法止确的是
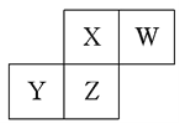
A. 元索Ⅹ和元Z的最高正化合价相同
B. 单核阴离子半径的大小顺序为:r(W)>r(X)
C. 气态简单氢化物的热稳定性顺序为:Y<Z<X<W
D. 元素Z的氧化物对应水化物都是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁4种物质分别含2种或3种元素,它们的分子中均含18个电子,甲是气态氢化物,在水中分步电离出两种阴离子,下列推断错误的是
A. 若某钠盐溶液含甲电离出的阴离子,则该溶液既可能与酸反应又可能与碱反应
B. 若乙与氧气的摩尔质量相同,则乙只能由2种元素组成
C. 若丙中含有第2周期IVA族的元素,则丙可能是甲烷的同系物
D. 若丁中各元素质量比跟甲中各元素质量比相同,则丁中一定含有-1价的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为 Fe—S m—As—F—O 组成的化合物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为____,其氢化物沸点比NH3的__________(填“高”或“低”), 其判断理由是________________ 。
(2)Fe成为阳离子时首先失去______轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为____________。
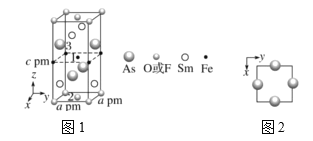
(3)一种四方结构的超导化合物的晶胞如图 1 所示。晶胞中 Sm 和 As 原子的投影位置如图2所示。图中 F- 和 O2-共同占据晶胞的上下底面位置, 若两者的比例依次用x 和 1— x 代表,则该化合物的化学式表示为___________;通过测定密度ρ和晶胞参数,可以计算该物质的 x 值,完成它们关系表达式:ρ=_______gcm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:![]() 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A. 若甲为焦炭,则丁可能是O2 B. 若甲为SO2,则丁可能是氨水
C. 若甲为Fe,则丁可能是盐酸 D. 若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法中错误的是 ( )。

A.负极的电极反应式为CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a向电极b移动
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,可逆反应A2(g)+3B2(g)![]() 2AB3(g)达到平衡的标志是( )
2AB3(g)达到平衡的标志是( )
A.容器内每减少1mol A2,同时生成2mol AB3
B.容器内每减少1mol A2,同时生成3mol B2
C.容器内A2、B2、AB3的物质的量之比为1:3:2
D.容器内A2、B2、AB3的物质的量浓度之比为1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸进行中和热的测定。
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体_____g。
(2)从下表中选择,称量NaOH固体所需要的仪器是(填字母)________。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如图所示。
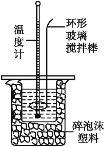
(1)若生成1 mol H2O时反应放出的热量为57.3 kJ,写出该反应的热化学方程式:__________。
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ______ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②用上述实验数值计算结果为____kJmol-1,与57.3 kJmol-1有偏差,产生偏差的原因可能是_____(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置和方法进行相应实验,能达到实验目的是( )

A.装置A用于检验1-溴丙烷的消去产物
B.装置B用于石油的分馏
C.装置C用于实验室制硝基苯
D.装置D用于除去甲烷中混有的乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com