
| A、铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、硫酸和氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
| C、稀硝酸滴在碳酸钙上:CO32-+2H+═CO2↑+H2O |
| D、二氧化碳通入澄清石灰水中:CO2+Ca2++2OH-═CaCO3↓+H2O |


 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,22.0 gCO2所含的电子数为22NA |
| B、常温常压下,1mol氦气含有原子数为NA |
| C、0.5mol?L-1 Na2CO3溶液中含有Na+离子的数目为NA |
| D、标准状况下,22.4LCCl4含有的氯原子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 g H2 |
| B、2 mol Cl2 |
| C、1.5 NA CO2 |
| D、22.4 L O2(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,反应2A (s)+B (g)=2C (g)+D (g)不能自发进行,则该反应△H一定大于0 |
| B、铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓船体的腐蚀速率 |
| C、其他条件不变,向纯水中加入盐酸或氢氧化钠都能抑制水的电离,降低水的离子积 |
| D、能与酸反应的氧化物,一定是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2+H2O═HCl+HClO |
| B、Zn+H2SO4═ZnSO4+H2↑ |
| C、Na2O+H2O═2NaOH |
| D、NaCl+AgNO3═AgCl↓+NaNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
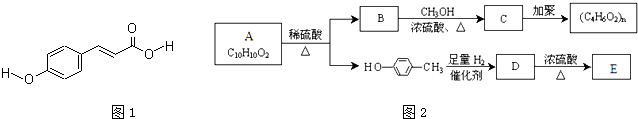
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
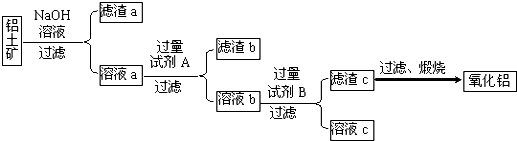
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com