
【题目】已知:[FeCl4(H2O)2]-为黄色,下列实验所得结论不正确的是( )
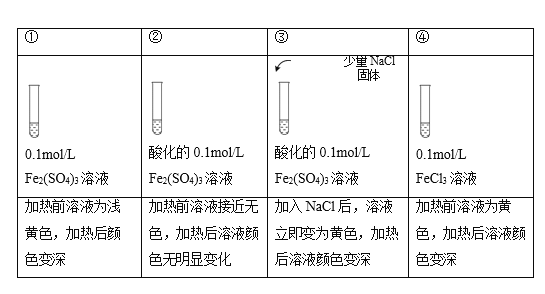
注:加热为微热,忽略体积变化。
A.实验①中,Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3
B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C.实验③中,存在可逆反应: Fe3+ + 4Cl-+ 2H2O ![]() [FeCl4(H2O)2]-
[FeCl4(H2O)2]-
D.实验④,可证明升高温度,Fe3+水解平衡正向移动
【答案】D
【解析】
A.加热促进水解,铁离子水解生成氢氧化铁,则实验①中,Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3, A项正确;
B.由Fe3++3H2OFe(OH)3+3H+可知,酸化后加热溶液颜色无明显变化,氢离子抑制水解,则实验②中酸化对Fe3+水解的影响程度大于温度的影响,B项正确;
C.加入NaCl后,溶液立即变为黄色,发生Fe3++4Cl-+2H2O[FeCl4(H2O)2]-,[FeCl4(H2O)2]-为黄色,加热时平衡正向移动,溶液颜色变深,C项正确;
D.由实验③可知,④中存在Fe3++4Cl-+2H2O[FeCl4(H2O)2]-,升高温度平衡正向移动,溶液颜色变深,不能证明对Fe3+水解平衡的影响,D项错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。生产钕铁硼磁铁的主要原材料有稀土金属钕、纯铁、铝、硼以及其他稀土原料。
(1)写出三价铁离子的外围电子排布图:___,在短周期元素中,与Al的化学性质最相似的元素符号是:___。
(2)实验测得AlCl3的蒸气以二聚分子Al2Cl6的形式存在,已知Al2Cl6分子中Al与Cl交替排列,为非极性分子,Al与Cl均满足8电子稳定结构,则Al2Cl6分子中Al原子采取___杂化,Al2Cl6分子的结构式为:___。
(3)硼(B)元素及与其同周期相邻的两种元素第一电离能由小到大的顺序为:___(用元素符号表示)。
(4)已知AlCl3的熔点为194℃,易升华,AlF3的熔点为1040℃,其原因为:___。
(5)已知立方氮化硼(BN)其晶胞结构类似于金刚石(如图所示),则N的配位数是___,与N原子距离最近的B原子构成的立体构型是___。

若图中b号原子的坐标为(![]() ,
,![]() ,0)写出a原子的坐标___,设晶胞中B、N原子半径分别为pnm、qnm,晶胞边长为rnm,则以a原子为中心形成的最小立方体的空间利用率为___(写代数式即可,不必化简);设晶胞中最近的B、N原子之间的距离为a nm,晶体的密度为bg·cm-3,则阿伏加德罗常数为___mol-1(用含a、b的代数式表示)。
,0)写出a原子的坐标___,设晶胞中B、N原子半径分别为pnm、qnm,晶胞边长为rnm,则以a原子为中心形成的最小立方体的空间利用率为___(写代数式即可,不必化简);设晶胞中最近的B、N原子之间的距离为a nm,晶体的密度为bg·cm-3,则阿伏加德罗常数为___mol-1(用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀溶液中含有![]() 、
、![]() 、
、![]() ,向其中逐渐加入铁粉,溶液中
,向其中逐渐加入铁粉,溶液中![]() 的浓度
的浓度![]() 纵坐标
纵坐标![]() 和加入铁粉的物质的量
和加入铁粉的物质的量![]() 横坐标
横坐标![]() 之间的关系如图所示。下列说法正确的是
之间的关系如图所示。下列说法正确的是
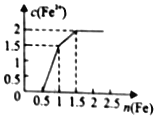
A.三种物质和铁反应的先后顺序依次为![]() 、
、![]() 、
、![]()
B.溶液中![]() 、
、![]() 物质的量浓度之比为4:1
物质的量浓度之比为4:1
C.溶液中![]() 、
、![]() 物质的量浓度之比为1:2
物质的量浓度之比为1:2
D.在此过程中,消耗56gFe可生成![]() 无色气体
无色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①盐卤(含MgCl2)![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液
MgCl2溶液![]() 无水MgCl2
无水MgCl2
②铝土矿![]() AlO2-
AlO2-![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3
③NH3![]() NO
NO![]() NO2
NO2![]() HNO3
HNO3
④NaCl溶液![]() Cl2
Cl2![]() 无水FeCl2
无水FeCl2
⑤S![]() SO3
SO3![]() H2SO4
H2SO4
⑥SiO2![]() Na2SiO3溶液
Na2SiO3溶液![]() H2SiO3
H2SiO3
A. ③⑥B. ③⑤⑥C. ①④⑤D. ①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列化学实验示意图及表中实验现象,从理论上分析得出的结论正确的是

选项 | 实验 | 实验现象 | 结论 |
A | a | 左烧杯中铁表面有气泡,右烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
B | b | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C | c | 白色固体先变为淡黄色,后变为黑色 | 溶解度:AgCl < AgBr < Ag2S |
D | d | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组混合物中,不论二者以什么比例混合,只要总质量一定,完全燃烧时生成CO2的质量也一定的是( )
A.甲烷、辛醛B.丙炔、苯乙烯C.甲醛、甲酸甲酯D.苯、甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,3-二异丙烯基苯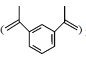 是重要的化工原料,下列说法正确的是( )
是重要的化工原料,下列说法正确的是( )
A.不可发生加聚反应B.不能使稀的高锰酸钾溶液褪色
C.分子中所有原子共平面D.其苯环上二氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组以黄铜矿(主要成分CuFeS2)为原料进行如下实验探究.为测定黄铜矿中硫元素的质量分数,将m1 g该黄铜矿样品放入如图所示装置中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铜矿样品.

(1)锥形瓶A内所盛试剂是_________;装置B的作用是_________;锥形瓶D内发生反应的离子方程式为:_______________________。
(2)反应结束后将锥形瓶D中的溶液进行如下处理:

如图向锥形瓶D中加入过量H2O2溶液反应的离子方程式为_________;操作Ⅱ是洗涤、烘干、称重,其中洗涤的具体方法________;该黄铜矿中硫元素的质量分数为_________(用含m1、m2的代数式表示)。
(3)反应后固体经熔炼、煅烧后得到泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO),要验证熔渣中存在FeO,应选用的最佳试剂是__________。
A.KSCN溶液、氯水
B.稀盐酸、KMnO4溶液
C.稀硫酸、KMnO4溶液
D.NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。
回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加___溶液,溶液颜色无明显变化,由此可知样品中无Fe3+。
(2)为测定绿矾中结晶水含量,称石英玻璃管(带开关K1和K2)(设为装置A)的质量,记为m1g。将样品装入石英玻璃管中,再次称其质量,记为m2g。按如图连接好装置进行实验。
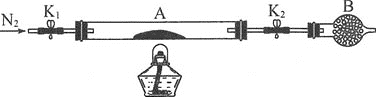
①仪器B的名称是___。
②将下列实验操作步骤正确排序___(填字母);重复上述操作步骤,直至A质量不变,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式,结晶水数目x=___。若实验时按a、d次序操作,则使x___(填偏大偏小或无影响)。
(3)为探究硫酸亚铁的分解产物,将(2)中已质量不变的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
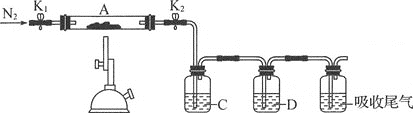
①C、D中的溶液依次为___(填字母),可观察到C、D中有气泡冒出。
a.品红 b.NaOH C.BaCl2 d.Ba(NO3 )2 e.浓硫酸
②写出硫酸亚铁高温分解反应的化学方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com