
【题目】某化学兴趣小组以黄铜矿(主要成分CuFeS2)为原料进行如下实验探究.为测定黄铜矿中硫元素的质量分数,将m1 g该黄铜矿样品放入如图所示装置中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铜矿样品.

(1)锥形瓶A内所盛试剂是_________;装置B的作用是_________;锥形瓶D内发生反应的离子方程式为:_______________________。
(2)反应结束后将锥形瓶D中的溶液进行如下处理:

如图向锥形瓶D中加入过量H2O2溶液反应的离子方程式为_________;操作Ⅱ是洗涤、烘干、称重,其中洗涤的具体方法________;该黄铜矿中硫元素的质量分数为_________(用含m1、m2的代数式表示)。
(3)反应后固体经熔炼、煅烧后得到泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO),要验证熔渣中存在FeO,应选用的最佳试剂是__________。
A.KSCN溶液、氯水
B.稀盐酸、KMnO4溶液
C.稀硫酸、KMnO4溶液
D.NaOH溶液
【答案】氢氧化钠 干燥气体 SO2+2OH =SO32+H2O H2O2+SO32= SO42+H2O 固体放入过滤器中,用玻璃棒引流向过滤器中加入蒸馏水至浸没沉淀,待滤液自然流下后,重复上述操作2~3 次 ![]() ×100% C
×100% C
【解析】
根据题意可知,本题考查实验探究及评价,运用实验装置安装步骤,离子方程式的书写步骤,除杂原理分析。
(1)为防止二氧化碳的干扰,应将空气中的二氧化碳用碱液除掉,锥形瓶A内所盛试剂是氢氧化钠溶液,通过碱石灰干燥吸收水蒸气,生成的二氧化硫能和过量氢氧化钠反应生成亚硫酸钠盐和水,反应的离子方程式为:SO2+2OH=SO32+H2O,
故答案为:氢氧化钠;干燥气体;SO2+2OH=SO32+H2O;
(2)亚硫酸根离子具有还原性能被过氧化氢氧化生成硫酸根离子,反应的离子方程式为:H2O2+ SO32=SO42+H2O,洗涤固体在过滤器中进行,加水至浸没固体使水自然流下,重复几次洗涤干净,具体操作为:固体放入过滤器中,用玻璃棒引流向过滤器中加入蒸馏水至浸没沉淀,待滤液自然流下后,重复上述操作23次,m2g固体为硫酸钡的质量,结合硫元素守恒计算得到硫元素的质量分数=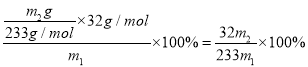 ,
,
故答案为:H2O2+SO32= SO42+H2O;固体放入过滤器中,用玻璃棒引流向过滤器中加入蒸馏水至浸没沉淀,待滤液自然流下后,重复上述操作23次;![]() ×100%;
×100%;
(3)反应后固体经熔炼、煅烧后得到泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO),要验证熔渣中存在FeO,应选用的最佳试剂是加入硫酸溶解后加入高锰酸钾溶液观察高锰酸钾溶液是否褪色设计检验方案,
故答案为:C。


科目:高中化学 来源: 题型:
【题目】酪醇是合成药物的中间体。由芳香化合物A为原料制备酪醇的一种合成路线如图:
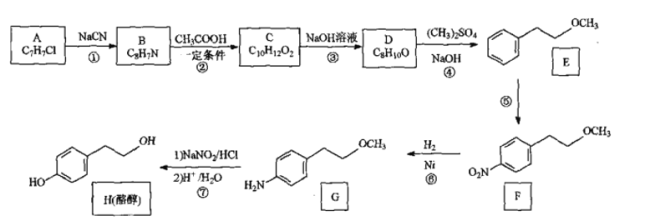
已知:
回答下列回题:
(1)B的结构简式为_____________________。
(2)F中的官能团的名称为__________________。
(3)写出C→D的化学方程式:___________________________。
(4)反应④的反应类型是_______________________________。
(5)反应⑤所需的试剂和条件是_________________________________。
(6)C的一种同分异构体,能发生银镜反应和水解反应,其核磁共振氢谱有4组峰,面积比为6:3:2:1,写出一种符合要求的同分异构体的结构简式:_____________。
(7)已知: ![]() (苯胺)易被氧化。设计以甲苯为原料制备2,4,6一三羟基苯甲酸的合成路线:____________________________________________________ (无机试剂任用)。
(苯胺)易被氧化。设计以甲苯为原料制备2,4,6一三羟基苯甲酸的合成路线:____________________________________________________ (无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:[FeCl4(H2O)2]-为黄色,下列实验所得结论不正确的是( )
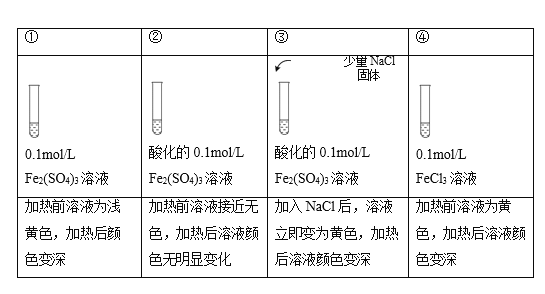
注:加热为微热,忽略体积变化。
A.实验①中,Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3
B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C.实验③中,存在可逆反应: Fe3+ + 4Cl-+ 2H2O ![]() [FeCl4(H2O)2]-
[FeCl4(H2O)2]-
D.实验④,可证明升高温度,Fe3+水解平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应3NaH+Fe2O3![]() 2Fe+3NaOH。
2Fe+3NaOH。
(1)基态Fe原子核外共有__种运动状态不相同的电子;Fe3+的价电子排布图为__。
(2)1molNaOH含有σ键数目为__;Fe3+可以和SCN-形成配合物,该反应是典型的可逆反应,说明配位原子配位能力__(填“强”或“弱”)。
(3)上述反应中含Na的化合物晶体类型均为__晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、Ni均为Ⅷ族元素,与C、N、O、P等组成的化合物有广泛的用途。回答下列问题:
![]() 基态
基态![]() 的价层电子排布图
的价层电子排布图![]() 轨道表达式
轨道表达式![]() 为________,C、N、O的第一电离能从小到大的顺序为________
为________,C、N、O的第一电离能从小到大的顺序为________
![]() 、P可形成一些复杂离子,如
、P可形成一些复杂离子,如![]() 、
、![]() 、
、![]() 等。
等。
![]() 中N原子的杂化类型为________,
中N原子的杂化类型为________,![]() 的空间构型是为________
的空间构型是为________
![]() 是一种白色固体,在加压下于
是一种白色固体,在加压下于![]() 时液化,形成一种能导电的熔体。熔体能导电的原因是________
时液化,形成一种能导电的熔体。熔体能导电的原因是________
![]() 、Ni易与
、Ni易与![]() 与
与![]() 互为等电子体
互为等电子体![]() 形成配合物,
形成配合物,![]() 中
中![]() 键与
键与![]() 键个数比为________,
键个数比为________,![]() 熔点
熔点![]() ,沸点
,沸点![]() ,不溶于水,溶于乙醇、苯等有机溶剂,
,不溶于水,溶于乙醇、苯等有机溶剂,![]() 属于________晶体
属于________晶体
![]() 、NiO的晶体类型与结构和NaCl相同。
、NiO的晶体类型与结构和NaCl相同。
![]() 熔点FeO________
熔点FeO________![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]()
![]() 晶胞如下图,
晶胞如下图,![]() 的配位数为________
的配位数为________

![]() 在氧气中加热,部分
在氧气中加热,部分![]() 被氧化为
被氧化为![]() ,晶体结构产生铁离子缺位的缺陷,其组成变为
,晶体结构产生铁离子缺位的缺陷,其组成变为![]() ,测得晶胞边长为acm,密度为
,测得晶胞边长为acm,密度为![]() ,则
,则![]() ________
________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中正确的是( )
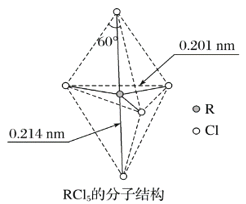
A. 每个原子都达到8电子稳定结构
B. 键角(Cl—R—Cl)有90°、120°、180°几种
C. RCl5受热后会分解生成分子RCl3,RCl5和RCl3都是极性分子
D. 分子中5个R—Cl键键能不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2-二溴乙烷,装置如下图所示:
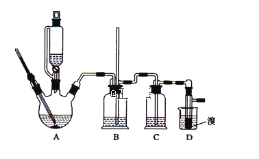
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)写出由乙醇制备乙烯的化学方程式______________________________,乙烯制备1,2-二溴乙烷的化学方程式_______________________________。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___________;(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置A中除了浓硫酸和乙醇外,还应加入_____,其目的是_______装置A中生成副产物乙醚的化学反应方程式 ___________________。
(4)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放 ________________,
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液d.品红和酸性KMnO4
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____层(填“上”、“下”);若产物中有少量副产物乙醚。可用_______的方法除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 物质结构与性质
物质结构与性质![]() VA族元素单质及其化合物在工农业生产中有重要用途。回答下列问题:
VA族元素单质及其化合物在工农业生产中有重要用途。回答下列问题:
![]() 基态As原子的核外电子排布式为
基态As原子的核外电子排布式为![]() ________,有________个未成对电子。
________,有________个未成对电子。
![]() 元素周期表中,与P紧邻的4种元素中电负性最大的是________(填元素符号
元素周期表中,与P紧邻的4种元素中电负性最大的是________(填元素符号![]() 。Si、P、S三种元素的第一电离能由大到小的顺序是________。
。Si、P、S三种元素的第一电离能由大到小的顺序是________。
![]() 铵盐大多不稳定,
铵盐大多不稳定,![]() F、
F、![]() 中,较易分解的是________,原因是________。
中,较易分解的是________,原因是________。
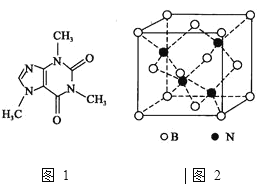
![]() 咖啡因对中枢神经有兴奋作用,其结构简式如图1。常温下,咖啡因在水中的溶解度为
咖啡因对中枢神经有兴奋作用,其结构简式如图1。常温下,咖啡因在水中的溶解度为![]() ,加适量水杨酸钠
,加适量水杨酸钠![]() 可使其溶解度增大,其原因可能是________,分子中氮原子的杂化类型有________。
可使其溶解度增大,其原因可能是________,分子中氮原子的杂化类型有________。
![]() 氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示:
氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示:
物质 | BN | AIN | GaN |
熔点 | 3000 | 2200 | 1700 |
![]() 试从结构的角度分析它们熔点不同的原因________。
试从结构的角度分析它们熔点不同的原因________。
![]() 的晶胞结构如图2所示,晶体中一个B原子周围距离最近的N原子有________个;若B、N的原子半径分别为
的晶胞结构如图2所示,晶体中一个B原子周围距离最近的N原子有________个;若B、N的原子半径分别为![]() 和
和![]() ,密度为
,密度为![]() ,阿伏加德罗常数值为
,阿伏加德罗常数值为![]() ,则BN晶胞中原子的体积占晶胞体积的百分率为________。
,则BN晶胞中原子的体积占晶胞体积的百分率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C2H2)是基本有机化工原料。由A制备聚乙烯醇缩丁醛和顺式异戊二烯的合成路线(部分反应条件略去)如下所示:

回答下列问题:
(1)A的名称是_______,B含有的官能团是_______________。
(2)①的反应类型是____________,⑦的反应类型是________________。
(3)C和D的结构简式分别为______________、_________________。
(4)异戊二烯分子中最多有________个原子共平面,顺式聚异戊二烯的结构简式为___________。
(5)写出与A具有相同官能团的异戊二烯的所有同分异构体__________(填结构简式)。
(6)参照异戊二烯的上述合成路线,设计一条由A和乙醛为起始原料制备1,3-丁二烯的合成路线___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com