
【题目】如图是实验室制备SO2并验证SO2某些性质的装置图。试回答:

(1)写出仪器A的名称___,写出此实验中制备SO2化学方程式___。
(2)C中的现象是___,此实验证明SO2是___气体。
(3)D中的反应现象证明SO2有___性;F中的现象是___,G中SO2与碘水反应的方程式:___。
(4)H中的试剂是氢氧化钠溶液,用于吸收多余的二氧化硫气体,防止污染空气;反应的离子方程式为___。
【答案】分液漏斗 Na2SO3+H2SO4=Na2SO4+H2O+SO2↑ 石蕊变红 酸性 漂白 酸性KMnO4溶液褪色 SO2+I2+2H2O=H2SO4+2HI SO2+2OH-=SO32-+H2O
【解析】
实验室制备SO2并验证SO2某些性质,B中浓硫酸与亚硫酸钠反应生成二氧化硫;C中二氧化硫与水反应生成亚硫酸遇石蕊试液变红;D中品红溶液褪色;E中二氧化硫与硫化氢发生氧化还原反应生成硫单质;F中酸性高锰酸钾溶液能够氧化二氧化硫导致紫色褪去;G中二氧化硫与碘水发生氧化还原反应生成硫酸和HI酸;H为尾气处理装置,二氧化硫与氢氧化钠反应可防止空气污染。据此分析解答。
(1)装有浓硫酸的仪器A为分液漏斗,装置B中生成SO2 化学方程式为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;
答案为:分液漏斗;Na2SO3+H2SO4=Na2SO4+H2O+SO2↑。
(2)C中SO2与水反应生成亚硫酸,紫色石蕊试液变红,说明SO2是酸性气体;
答案为:石蕊变红;酸性。
(3)D中品红溶液褪色,说明SO2有漂白性,因为SO2有还原性,与酸性高锰酸钾溶液发生氧化还原反应,导致高锰酸钾溶液的紫色褪去,G中SO2与碘水发生氧化还原反应生成硫酸和HI酸,化学方程式为:SO2+I2+2H2O=H2SO4+2HI;
答案为:漂白;酸性KMnO4溶液褪色;SO2+I2+2H2O=H2SO4+2HI 。
(4) SO2气体有毒性,为防SO2污染空气,尾气中的SO2用氢氧化钠溶液吸收,反应的离子方程式为:SO2+2OH-=SO32-+H2O;
答案为:SO2+2OH-=SO32-+H2O。


科目:高中化学 来源: 题型:
【题目】GaAs晶体的熔点很高, 硬度很大, 密度为ρ g·cm-3,Ga 和As 的摩尔质量分别为MGag·mol-1和MAs g·mol-1, 原子半径分别为rGa pm 和rAs pm, 阿伏加德罗常数值为NA, 其晶胞结构如下图所示, 下列说法错误的是
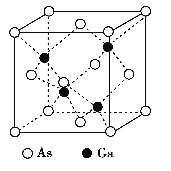
A. 该晶体为原子晶体
B. 在该晶体中,Ga和As均无孤对电子,Ga和As的配位数均为4
C. 原子的体积占晶胞体积的百分率为![]()
D. 所有原子均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。已知:

(1)探究BaCO3和BaSO4之间的转化,实验操作:
试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
实验Ⅰ | BaCl2 | Na2CO3 | Na2SO4 | …… |
实验Ⅱ | Na2SO4 | Na2CO3 | 有少量气泡产生,沉淀部分溶解 |
①实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入盐酸后,__________
②实验Ⅱ中加入稀盐酸后发生反应的离子方程式是_______。
③实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:______
(2)探究AgCl和AgI之间的转化,实验Ⅲ:
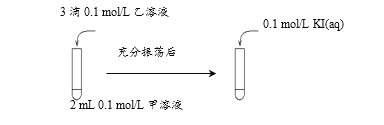
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。

注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
① 实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是______(填序号)。
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
② 实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是 _______________
③ 结合信息,解释实验Ⅳ中b<a的原因:______。
④ 实验Ⅳ的现象能说明AgI转化为AgCl,理由是_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年12月,全球首条光伏高速公路亮相济南。下列有关说法不正确的是

A. 光伏发电将太阳能转变为电能
B. 汽车尾气中的CO2会造成酸雨
C. 光伏发电代替燃煤发电可减少雾霾
D. 光伏发电所用太阳能电池板的主要材料是硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )

A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2 + 2H2O + 4e == 4OH–
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H+ + 2e == H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL 0.1 mol·L-1 NaOH溶液中加入0.1 mol·L-1的一元
酸HA,溶液pH的变化曲线如图所示。下列说法正确的是

A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. b点所示溶液中c(A-)>c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的,如下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化。则下列说法正确的是

A. 通常情况下,NO比N2稳定
B. 通常情况下,N2(g)和O2(g)混合能直接生成NO
C. 1molN2(g)和1molO2(g)具有的总能量小于2mol NO(g)具有的总能量
D. 1molN2(g)和1molO2(g)反应放出的能量为180kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲醛是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置已略去)制备苯甲醛。
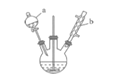
已知有机物的相关数据如下表所示:
有机物 | 沸点℃ | 密度为g/cm3 | 相对分子质量 | 溶解性 |
苯甲醛 | 178.1 | 1.04 | 106 | 微溶于水,易溶于乙醇、醚和卤代烃 |
苯甲醇 | 205.7 | 1.04 | 108 | 微溶于水,易溶于乙醇、醚和卤代烃 |
二氯甲烷 | 39.8 | 1.33 | 难溶于水,易溶于有机溶剂 |
实验步骤:
①向容积为500mL的三颈烧瓶加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9-10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。
请回答下列问题:
(1)仪器b的名称为______,搅拌器的作用是______。
(2)苯甲醇与NaClO反应的化学方程式为_______。
(3)步骤①中,投料时,次氯酸钠不能过量太多,原因是____;步骤③中加入无水硫酸镁,若省略该操作, 可能造成的后果是______。
(4)步骤②中,应选用的实验装置是___(填序号),该操作中分离出有机相的具体操作方法是___。
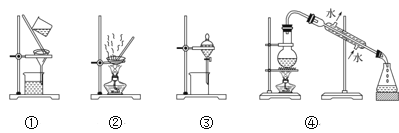
(5)步骤④中,蒸馏温度应控制在_______左右。
(6)本实验中,苯甲醛的产率为________(保留到小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的某有机物完全燃烧后,将燃烧产物通过足量的石灰水,经过滤可得沉淀10g,但称量滤液时,其质量只比原石灰水减少2.9g,则此有机物可能是:
A. C2H4 B. C2H4O2
C. C2H6O D. C4H10O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com