
【题目】聚合硫酸铝铁(PAFS)是一种高效净水剂,其组成表示为[AlFe(OH)x(SO4)(3-![]() )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。

回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为__。
(2)PAFS中铁元素的化合价为_______;沉淀A的化学式为_________。
(3)如图所示,过滤操作中的一处错误是__________。
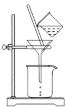
(4)生成沉淀B的离子方程式为______。
(5)PAFS中Al元素的质量分数为_______(用同m、n的代数式表示)。
【答案】100mL容量瓶 +3 Fe(OH)3 漏斗下端尖嘴未紧贴烧杯内壁 CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-或CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-、CO2+CO32-+H2O=2HCO3- ![]() 或
或![]()
【解析】
为检测PAFS中Al含量,PAFS加入足量氢氧化钠溶液反应生成氢氧化铁沉淀和偏铝酸钠溶液,过滤后得到氢氧化铁,滤液中通入过量二氧化碳气体,生成氢氧化铝沉淀,灼烧得到氧化铝。
(1)配制1.0mol/L的NaOH溶液100mL,涉及称量、溶解、移液、洗涤、定容等操作,则需要的仪器有玻璃棒、托盘天平(量筒)、烧杯、胶头滴管,还需要100mL容量瓶,故答案为:100mL容量瓶;
(2)化学式为:[AlFe(OH)x(SO4)(3-![]() )]y,其中Al为+3价,设Fe的化合价为m,则3+m=x+2×(3-
)]y,其中Al为+3价,设Fe的化合价为m,则3+m=x+2×(3-![]() ),m=+3,沉淀A的化学式为:
),m=+3,沉淀A的化学式为:
Fe(OH)3,故答案为:+3;Fe(OH)3;
(3)过滤时,漏斗下端应紧贴烧杯内壁,避免液体飞溅,故答案为:漏斗下端尖嘴未紧贴烧杯内壁;
(4)偏铝酸钠溶液中通入过量二氧化碳气体生成氢氧化铝沉淀,反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-、CO2+CO32-+H2O=2HCO3-,故答案为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-、CO2+CO32-+H2O=2HCO3-;
(5)m g PAFS生成n g氧化铝,铝的质量为:![]() g,则铝的含量为
g,则铝的含量为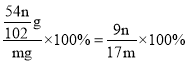 ,故答案为:
,故答案为:![]() 或
或![]() 。
。


 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】698 K时,向某V L的密闭容器中充入2 mol H2(g)和2 mol I2(g),发生反应:H2(g)+I2(g)2HI(g) ΔH=-26.5 kJ·mol-1,测得各物质的物质的量浓度与时间的变化关系如图所示。
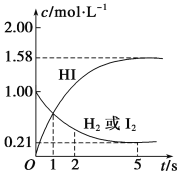
该反应达到平衡状态时,______(填“吸收”或“放出”)的热量为:____kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】易混易错题组:按题目要求填写下列空白。
(1) 用价层电子对互斥模型预测下列微粒的立体结构,并指出后两种物质中中心原子的杂化方式。
H2Se______________ CF4_______________SO2______________ 、______SO42-______________、_______
(学法题)简述价层电子对互斥模型与分子的立体结构之间的关系_________________________
(2)写出下列物质的系统命名:
①(CH3)3COH________________②CH3CHClCOOH ___________________
③![]() ________________ ④
________________ ④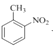 ________________
________________
(3)下列原子核外电子排布中,违背“泡利不相容原理”的是_________;违背“洪特规则”的是_______;违背“洪特 规则特例”的是___________。违背“能量最低原理”的是________;(填编号)
① 6 C轨道表示为![]()
②7N轨道表示为:![]()
③29 Cu电子排布式为:1s 2 2s 2 2p 6 3s 2 3p 6 3d 9 4s 2
④20 Ca电子排布式为:1s 2 2s 2 2p 6 3s 2 3p 6 3d 2
⑤O: ![]()
(学法题)在解答此题时必须明确概念,简述泡利原理,洪特规则的概念:___________________________
(4)按要求书写化学方程式
①CH3CH(OH)CH3的催化氧化:__________________________________________
②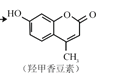 和氢氧化钠溶液反应____________________________________________
和氢氧化钠溶液反应____________________________________________
③过量乙酸与甘油的酯化反应_________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据碘与氢气反应的热化学方程式:
(i)I2(g)+H2(g) ![]() 2HI(g)+9.48kJ (ii)I2(s)+H2(g)
2HI(g)+9.48kJ (ii)I2(s)+H2(g)![]() 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是( )
A.![]() 中通入
中通入![]() ,反应放热
,反应放热![]()
B.![]() 固态碘与
固态碘与![]() 气态碘所含的能量相差
气态碘所含的能量相差![]()
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(ii)的反应物总能量比反应(i)的反应物总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ba(AlO2)2可溶于水。右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系。下列有关叙述正确的是 ( )
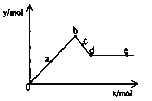
A. a—b时沉淀的物质的量:A1(OH)3比BaSO4多
B. c—d时溶液中离子的物质的量:AlO2–比Ba2+多
C. a—d时沉淀的物质的量:BaSO4可能小于A1(OH)3
D. d—e时溶液中离子的物质的量:Ba2+不能等于OH–
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述中,不正确的是( )
A. 纤维素![]() 葡萄糖
葡萄糖 ![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B. 淀粉![]() 葡萄糖
葡萄糖 ![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C. 蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
D. 油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。答:____________________________。
(2)下列操作会使配制的KOH溶液的物质的量浓度偏大的是_______
A、转移溶液后未洗涤烧杯和玻璃棒就直接定容
B、转移溶液过程中有液体溅出容量瓶
C、定容时俯视刻度线
D、配制溶液定容摇匀后发现容量瓶中液面低于刻度线,又补足了水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是某工厂的生产流程:
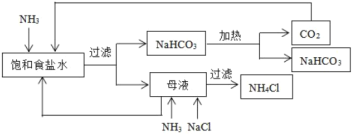
下列分析正确的是( )
A.母液中只含有:NH3和CO2B.母液中只含有:NH4+和Cl-
C.向母液中通NH3、加NaCl时加热D.该工厂的产品是纯碱和NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2RCH2CHO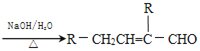 ,水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:
,水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:
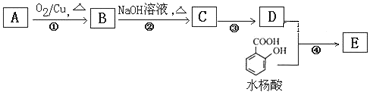
已知D的相对分子质量是130。请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%,则A的分子式为______, 结构分析显示A只有一个甲基,A的名称为______;
(2)第④步的反应条件为______;写出E的结构简式______:
(3)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为:______;
(4)写出同时符合下列条件水杨酸的同分异构体的结构简式:______
(a)能与FeCl3发生显色反应;
(b)能与银氨溶液反应
(c)能发生水解反应
(d)核磁共振氢谱显示有四组峰。且峰面积比为1:2:2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com