
【题目】已知2RCH2CHO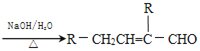 ,水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:
,水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:
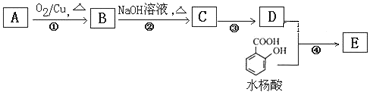
已知D的相对分子质量是130。请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%,则A的分子式为______, 结构分析显示A只有一个甲基,A的名称为______;
(2)第④步的反应条件为______;写出E的结构简式______:
(3)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为:______;
(4)写出同时符合下列条件水杨酸的同分异构体的结构简式:______
(a)能与FeCl3发生显色反应;
(b)能与银氨溶液反应
(c)能发生水解反应
(d)核磁共振氢谱显示有四组峰。且峰面积比为1:2:2:1
【答案】C4H10O 1﹣丁醇(或正丁醇) 浓H2SO4、加热 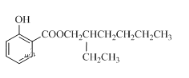 CH3CH2CH2CHO+2Cu(OH)2+NaOH
CH3CH2CH2CHO+2Cu(OH)2+NaOH ![]() CH3CH2CH2COONa+Cu2O↓+3H2O
CH3CH2CH2COONa+Cu2O↓+3H2O 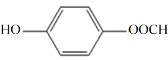
【解析】
饱和一元醇A中氧的质量分数约为21.6%,设该一元醇的通式为CnH2n+2O,氧元素的质量分数=![]() =21.6%,n=4,则A的分子式为C4H10O,结构分析显示A只有一个甲基,则A的结构简式为CH3CH2CH2CH2OH,A在Cu作催化剂、加热条件下被氧化生成B,B能发生银镜反应,则B结构简式为CH3CH2CH2CHO,1-丁醛在NaOH/H2O条件下发生加成生成C,结合题中信息可知,C结构简式为CH3CH2CH2CH=C(CH2CH3)CHO,C反应生成D,E为水杨酸酯,根据图中转化关系知,D中含有醇羟基,且D相对分子质量为130,则D结构简式为CH3CH2CH2CH2CH(CH2CH3)CH2OH,C和氢气发生加成反应生成D,D和水杨酸发生酯化反应生成E,E结构简式为
=21.6%,n=4,则A的分子式为C4H10O,结构分析显示A只有一个甲基,则A的结构简式为CH3CH2CH2CH2OH,A在Cu作催化剂、加热条件下被氧化生成B,B能发生银镜反应,则B结构简式为CH3CH2CH2CHO,1-丁醛在NaOH/H2O条件下发生加成生成C,结合题中信息可知,C结构简式为CH3CH2CH2CH=C(CH2CH3)CHO,C反应生成D,E为水杨酸酯,根据图中转化关系知,D中含有醇羟基,且D相对分子质量为130,则D结构简式为CH3CH2CH2CH2CH(CH2CH3)CH2OH,C和氢气发生加成反应生成D,D和水杨酸发生酯化反应生成E,E结构简式为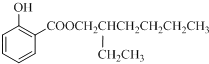 ,以此解答该题。
,以此解答该题。
(1)通过以上分析知,A的分子式为C4H10O,A的名称为1-丁醇,故答案为:C4H10O;1-丁醇(或正丁醇);
(2)第④步为CH3CH2CH2CH2CH(CH2CH3)CH2OH与水杨酸发生酯化反应的过程,其条件是浓H2SO4、加热;生成的E的结构简式为: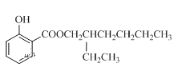 ;
;
(3)加热条件下,丁醛和新制氢氧化铜反应生成丁酸钠、氧化亚铜和水,反应方程式为CH3CH2CH2CHO+2Cu(OH)2+NaOH ![]() CH3CH2CH2COONa+Cu2O↓+3H2O;
CH3CH2CH2COONa+Cu2O↓+3H2O;
(4)水杨酸的分子式为C7H6O3,其不饱和度为![]() ,能与FeCl3发生显色反应,则说明分子内含酚羟基;能与银氨溶液反应同时能发生水解反应,根据分子式及不饱和度可知,分子内含甲酸酯基,又核磁共振氢谱显示有四组峰,且峰面积比为1:2:2:1,则酚羟基与甲酸酯基在苯环的对位,其结构简式为:
,能与FeCl3发生显色反应,则说明分子内含酚羟基;能与银氨溶液反应同时能发生水解反应,根据分子式及不饱和度可知,分子内含甲酸酯基,又核磁共振氢谱显示有四组峰,且峰面积比为1:2:2:1,则酚羟基与甲酸酯基在苯环的对位,其结构简式为: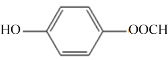 。
。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案科目:高中化学 来源: 题型:
【题目】聚合硫酸铝铁(PAFS)是一种高效净水剂,其组成表示为[AlFe(OH)x(SO4)(3-![]() )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。

回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为__。
(2)PAFS中铁元素的化合价为_______;沉淀A的化学式为_________。
(3)如图所示,过滤操作中的一处错误是__________。
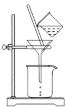
(4)生成沉淀B的离子方程式为______。
(5)PAFS中Al元素的质量分数为_______(用同m、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以“物质的量”为中心的计算是化学计算的基础。下列与“物质的量”相关的计算正确的( )
A.现有CO、CO2、O3三种气体,它们分别都含有1molO,则三种气体的物质的量之比为 3∶2∶1
B.5.6g CO 和22.4L CO2中含有的碳原子数一定相等
C.标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D.n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为 35.5m/n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列三个反应:①2FeCl3+2KI===2FeCl2+2KCl+I2,②2Fe+3Cl2![]() 2FeCl3,③2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑,若某溶液中有Fe2+、I和Cl,要氧化除去I而不除去Fe2+和Cl,可加入的试剂是
2FeCl3,③2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑,若某溶液中有Fe2+、I和Cl,要氧化除去I而不除去Fe2+和Cl,可加入的试剂是
A. Cl2B. KMnO4C. FeCl3D. HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾[KAl(SO4)2·12H2O]的过程如图所示。下列说法正确的是
![]()
A. 试剂①可选用盐酸或NaOH溶液
B. 过滤操作中使用的玻璃仪器只有漏斗、烧杯
C. 滤液A到沉淀B的反应中无CO2生成
D. 最后一步操作是蒸发结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知4NH3+5O2═4NO+6H2O,反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的是( )
A.4/5v(O2)= v(NO)
B.5/6v(O2)= v(H2O)
C.2/3v(NH3)= v(H2O)
D.4/5v(NH3)= v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A由C、H、O三种元素组成,相对分子质量为90。将4.5 g A完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重2.7 g和6.6 g。A能与NaHCO3溶液产生CO2,且两分子A之间脱水可生成六元环状化合物。有关A的说法正确的是
A. 有机物A的分子式为C3H8O3
B. 0.1 mol A与足量Na反应生成2.24 L H2
C. A催化氧化的产物不能发生银镜反应
D. A能在一定条件下发生缩聚反应生成![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证氧化性:Cl2>Fe3+>SO2,某化学研究性学习小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕):
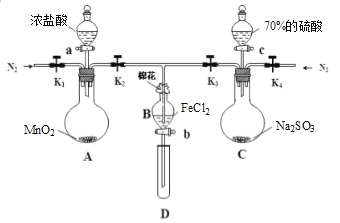
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是__________________________________________________________。
(2)棉花中浸润的溶液为________________,作用是_____________________________________________ 。
(3)A中发生反应的化学方程式________________________________________________。
(4)导致步骤Ⅲ中溶液变黄的离子反应是________________________________________,用________(写试剂化学式)检验氧化产物,现象是____________________________________________ 。
(5)能说明氧化性Fe3+>SO2的离子方程式是_______________________________。
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性:Cl2>Fe3+>SO2的是_______(填“甲”“乙”“丙”)。
过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
甲 | 有Fe3+无Fe2+ | 有SO42﹣ |
乙 | 既有Fe3+又有Fe2+ | 有SO42﹣ |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可通过蒸馏石油得到多种沸点范围不同的馏分,装置如图所示。下列说法不正确的是
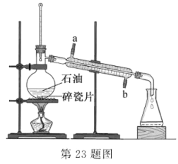
A.沸点较低的汽油比沸点较高的柴油先馏出
B.蒸馏烧瓶中放人沸石可防止蒸馏时发生暴沸
C.冷凝管中的冷凝水应该从 a 口进 b 口出
D.温度计水银球的上限和蒸馏烧瓶支管口下沿相平
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com