
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡。根据所学知识回答下列问题:
(1)下列方法中,可以使0.10 mol/L CH3COOH溶液中值增大的措施是___________。
a.加水稀释
b.加入少量CH3COONa固体
c.加入少量冰醋酸
d.通入少量HCl气体
(2)t℃时,水的离子积常数Kw=1×10-12。
①该温度下,若100体积pH=a的H2SO4溶液与1体积pH=b的NaOH溶液混合后溶液呈中性,则a+b= 。
②该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因 ;该混合溶液中:c(A-)-c(Na+)= mol/L。(填准确数值)
(3)常温下,有浓度均为0.1mol/L的三种溶液:a.NaHCO3;b.NaClO;c.CH3COONa。
①三种溶液pH由大到小的顺序为: (填序号)。
②溶液a的pH大于8,则溶液中c(H2CO3) c(CO32-) (填“>”、“<”或“=”)。
(4)已知25℃ 时,Ksp[AgCl]=1.8×10-10,现将足量氯化银分别放入:a.100mL蒸馏水中;b.100mL 0.2 mol/LAgNO3溶液中;c.100mL 0.1 mol/L氯化铝溶液中;d.100mL 0.1 mol/L盐酸溶液中。充分搅抖后,相同温度下银离子浓度由大到小的顺序是 。 (填写序号);b中氯离子的浓度为 mol/L。
【答案】(16分)(1)(1)ad;
(2)①14;②HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+,使溶液的pH=5;9.9×10-6或者10-5-10-7
(3)①b>a>c ②> (4)b>a>d>c 9×10-10
【解析】
试题分析:(1)a.加水稀释醋酸促进醋酸电离,且氢离子浓度减小,所以能使c(H+)/c(CH3COOH)值、pH均增大,故a正确;b.加CH3COONa,由于CH3COO-对CH3COOH的电离起到抑制作用,则c(H+)/c(CH3COOH)值减小,故b错误;c.加少量冰醋酸,醋酸浓度增大,弱电解质的浓度越大,电离程度越小,则c(H+)/c(CH3COOH)值减小,故c错误;d.通入HCl气体,溶液里c(H+)明显增大,平衡逆向移动,c(CH3COOH)略有增大,但c(H+)/c(CH3COOH)值增大,故d正确;故选ad;
(2)①若100体积pH=a的硫酸溶液中氢离子的物质的量浓度=10-a mol/L,1体积pH=b的NaOH溶液中氢氧根离子的物质的量浓度=10 b-12 mol/L,混合后溶液呈中性,则氢离子的物质的量等于氢氧根离子的物质的量,所以100×10-a mol/L=1×10 b-12 mol/L,所以a+b=14;
②pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,氢离子和氢氧根离子恰好反应,如果酸是强酸,则盐溶液呈中性,实际上溶液呈酸性,则HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+,使溶液的pH=5;该溶液中存在电荷守恒式为c(A-)+c(OH-)=c(Na+)+c(H+),则c(A-)-c(Na+)=c(H+)-c(OH-)=(10-5-10-7)mol/L=9.9×10-6mol/L。
(3)已知酸性的强弱顺序为:CH3COOH>H2CO3>HClO;①酸性越弱水解程度越强,浓度相等时溶液的碱性越强,三种溶液pH由大到小的顺序为b>a>c;②NaHCO3溶液的pH大于8,HCO3-的水解程度大于其电离程度,则溶液中c(H2CO3)>c(CO32-);
(4)①a.100mL 0.2molL-1AgNO3溶液中Ag+浓度为0.2mol/l抑制沉淀溶解平衡,c.100mL 0.1molL-1氯化铝溶液中氯离子浓度为0.3mol/L,银离子浓度=6×10-10mol/L;d.100mL 0.1molL-1盐酸溶液中氯离子浓度为0.1mol/L,银离子为1.8×10-9mol/L;综上所述大小顺序为b>a>d>c;b.100mL 0.2mol/L AgNO3溶液中,银离子的浓度为0.2mol/L,加如氯化银后,氯离子浓度为![]() =9×10-10mol/L。
=9×10-10mol/L。


科目:高中化学 来源: 题型:
【题目】一种离子晶体的晶胞如图其中阳离子A以![]() ,表示阴离子B以
,表示阴离子B以![]() 表示。
表示。
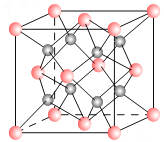
(1)若A和B的核外电子排布与Ar相同,则该离子化合物的化学式是 ___________________;
(2)阳离子周围距离最近的阴离子数为___ __,阴离子周围距离最近的阴离子数___ __。
(3)若与MgO的熔点比较,出现不同的原因是
(4)已知A的离子半径为r m,则该晶胞的体积是 ___________m3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组的研究课题是:探究测定草酸晶体(H2C2O4xH2O)中x的值。该组同学通过查阅资料查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
学习小组的同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000 mol/L的酸性KMnO4标准溶液进行滴定,达到终点时消耗了10.00mL。
请回答下列问题:
(1)配制100.00 mL待测液时,使用的玻璃仪器除烧杯、玻璃棒及胶头滴管外,还需要 。
(2)滴定时,将酸性KMnO4标准液装在如图中的 (填“甲”或“乙”)滴定管中。本实验滴定达到终点的标志是 。
![]()
(3)通过上述数据,求得x= 。
(4)讨论:
①若滴定终点时俯视滴定管,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①CO2的大量排放会加剧温室效应
②正常雨水的pH为5.6,主要是因为溶解了SO2
③利用太阳能、风能和氢能替代化石能源可以改善空气的质量
④含磷合成洗涤剂易于被细菌分解,不会导致水体污染
⑤为防止电池中的重金属离子污染土壤和水源,废电池要集中处理
A.①②③④⑤ B.②③⑤ C.①③⑤ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如右图所示。图中有机废水中有机物可用C6H10O5表示。下列有关说法正确的是
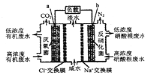
A.b电极为该电池的负极
B.b电极附近溶液的pH减小
C.a电极反应式:C6H10O5-24e-+7H2O═6CO2↑+24H+
D.中间室:Na+移向左室,Cl-移向右室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L固定体积的容器中混合,并在一定条件下发生如下反应∶2A(g)+B(g)![]() 2C(g)。若经2s后测得C的浓度为0.6 molL-1,
2C(g)。若经2s后测得C的浓度为0.6 molL-1,
求(1)A表示的反应的平均速率?
(2)2 s时物质B的浓度?
(3)2 s时物质A的转化率?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BHT是一种常用的食品抗氧化剂,从![]() 出发合成BHT的方法有如下两种。下列说法错误的是
出发合成BHT的方法有如下两种。下列说法错误的是
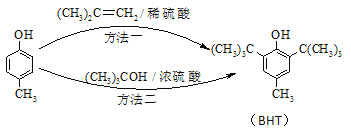
A.从绿色化学角度分析方法一优于方法二
B.BHT在水中的溶解度小于苯酚
C.两种方法的反应类型都是加成反应
D.BHT与![]() 都能使酸性KMnO4溶液褪色
都能使酸性KMnO4溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com