
【题目】(1)配平下列方程式,用双线桥法表示出电子转移的数目。 Fe2O3 + KNO3 + KOH = K2FeO4 + KNO2 + H2O ,____________,氧化剂 ________ ,氧化产物 __________
(2)用单线桥法表示下列氧化还原反应敀关系, 并标出电子转移的数目。用MnO2氧化密度为1.19 g/cm3,溶质质量分数为36.5%的HCl溶液,反应得到澄清溶液。反应的化学方程式为: MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①该反应的离子方程式为: _____________________________________________,该盐酸的物质的量浓度为___________mol/L。
②氧化剂与还原剂物质的量之比为_______________
③8.7gMnO2与足量浓盐酸反应能使________molHCl被氧化;其中,还原过程为:________→_______,__________。
④如果该反应转移1mol电子,则生成标准状况下的气体体积为___________L。
【答案】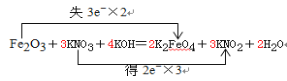 KNO3 K2FeO4
KNO3 K2FeO4 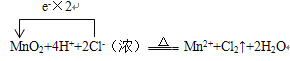 11.9 1:2 0.2
11.9 1:2 0.2 ![]() 11.2
11.2
【解析】
本题主要考查氧化还原方程的配平与计算。
(1)Fe2O3失去电子为还原剂得到K2FeO4氧化产物,KNO3得到电子为氧化剂,依据得失电子守恒和原子数守恒配平方程。
(2)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O中MnO2为氧化剂,HCl为还原剂,由得失电子守恒计算相关物质。
MnCl2+Cl2↑+2H2O中MnO2为氧化剂,HCl为还原剂,由得失电子守恒计算相关物质。
(1)Fe2O3失去电子为还原剂得到K2FeO4氧化产物,KNO3得到电子为氧化剂,依据得失电子守恒和原子数守恒配平方程: ,故答案为:
,故答案为: ;KNO3;K2FeO4;
;KNO3;K2FeO4;
(2)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O中MnO2为氧化剂,HCl为还原剂,由得失电子守恒和原子数守恒可知离子方程式为:
MnCl2+Cl2↑+2H2O中MnO2为氧化剂,HCl为还原剂,由得失电子守恒和原子数守恒可知离子方程式为: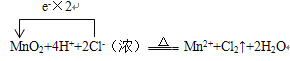 ,盐酸物质的量浓度
,盐酸物质的量浓度![]() 。氧化剂为:MnO2,还原剂为:Cl-;由得失电子可知氧化剂与还原剂物质的量之比为1:2;
。氧化剂为:MnO2,还原剂为:Cl-;由得失电子可知氧化剂与还原剂物质的量之比为1:2;
8.7gMnO2物质的量n=8.7g÷87g/mol=0.1mol,所以被氧化的HCl为0.2mol;还原过程为![]() ;转移1mol电子,则生成标准状况下的Cl2体积为0.5mol×22.4L·mol-1=11.2L。故答案为:
;转移1mol电子,则生成标准状况下的Cl2体积为0.5mol×22.4L·mol-1=11.2L。故答案为: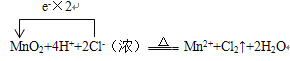 ;11.9;1:2;0.2;
;11.9;1:2;0.2;![]() ;11.2。
;11.2。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】实验室要配制480mL0.1mol·L-1Na2CO3溶液,回答下列问题。
(1)应用托盘天平称取Na2CO3·10H2O晶体___g。
(2)配制Na2CO3溶液时需用的主要玻璃仪器有烧杯、玻璃棒、___、___。
(3)若实验遇下列情况,溶液的浓度偏低的是___
A.加水时超过刻度线
B.忘记将洗涤液加入容量瓶
C.容量瓶内壁附有水珠而未进行干燥处理
D.定容后摇匀,液面低于刻度线
E.称量时砝码生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】位于短周期的四种主族元素A、B、C、D,原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。E是我国使用最早合金中的主要成分。根据你的推断完成下列问题:
(1)B、C、E的元素符号为________,________,__________。
(2)写出由上述元素形成的具有漂白作用的四种物质的化学式______、______、______、______。
(3)由A、B两种元素形成的原子个数比为1∶1的化合物的电子式______。
(4)写出D的最高价氧化物对应水化物与E反应的化学方程式,并用双线桥标出电子转移的方向和数目___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为______________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。

①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填序号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是______________________________________________________。
②让反应停止的操作方法及原因是__________________________________________。
(4)以下收集NO气体的装置,合理的是________(填序号)。
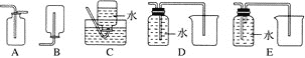
(5)将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
①NO的体积为________ L,NO2的体积为________ L。
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 向澄清石灰水中通入足量二氧化碳:2OH+CO2===![]() +H2O
+H2O
B. 氧化钠投入水中发生反应:![]() +H2O===2OH
+H2O===2OH
C. 醋酸溶液滴入到NaOH溶液中:CH3COOH+OH===CH3COO+H2O
D. 铁和稀盐酸反应制氢气:2Fe+6H+===2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测合理的是
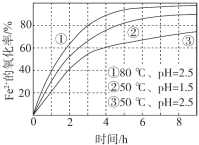
A. 由①、②可知, pH越大,+2价铁越易被氧化
B. 由②、③推测,若pH>7,+2价铁更难被氧化
C. 由①、③推测,FeCl2被O2氧化的反应为放热反应
D. 60℃、pH=2.5时, 4 h内Fe2+的平均消耗速率大于 0.15a mol/(L·h)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,地球上的碳循环,光合作用是必不可少的(如下图所示)。下列叙述正确的是

A. 石油与煤是可再生能源
B. CO2是煤、石油形成淀粉、纤维素等的催化剂
C. 光合作用将太阳能转化为化学能
D. 图中所出现的物质中淀粉与纤维素为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种短周期元素的位置如图所示(其中乙、丙、丁的位置未标出)。
![]()
已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等。
(1)甲元素在周期表中的位置为______________。
(2)丙、丁可形成AB2型化合物,其化学式为________。
(3)丙是自然界中形成化合物种类最多的元素,则丙是________(填名称),其单质与甲元素的最高价氧化物对应水化物的浓溶液共热时反应的化学方程式是______________________。
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,则丁是________(填元素符号),写出这些化合物中任意两种符合以下条件的化学式______________________
(①原子个数比为1∶2;②分子中价电子总数为偶数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种药物中间体,合成 G的部分流程如下:

请回答下列问题:
(1)G物质中的含氧官能团的名称是___________、____________。
(2)上述⑤变化过程的反应类型是_____________。
(3)反应A→B的化学方程式为________________________________________。
(4)写出满足下列条件的C的同分异构体的结构简式:_______________________。
Ⅰ. 苯环上只有两种取代基。
Ⅱ. 分子中只有4种不同化学环境的氢。
Ⅲ. 能与NaHCO3反应生成CO2。
(5)根据已有知识并结合相关信息,写出以![]() 和乙酸酐为原料制备
和乙酸酐为原料制备![]() 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH__________
CH3CH2OH__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com