
【题目】下列离子方程式正确且与对应操作和目的相符的是
选项 | 目的 | 操作 | 离子方程式 |
A | 比较Fe2+和Br还原性强弱 | 向FeBr2溶液中滴入少量氯水 | 2Br+Cl2=Br2+2Cl |
B | 比较C、Si非金属性强弱 | 向硅酸钠溶液中通入少量二氧化碳 | SiO32-+CO2+H2O=H2SiO3↓+CO32- |
C | 除去CO2中的SO2 | 将气体通入盛有饱和碳酸氢钠溶液的洗气瓶 | CO32-+SO2= SO32-+CO2 |
D | 实验室制取氯气 | 向MnO2固体中加入浓盐酸并加热 | MnO2+4HCl(浓) +2Cl +Cl2↑+2H2O |
A.AB.BC.CD.D
【答案】B
【解析】
A. 比较Fe2+和Br还原性强弱时,向FeBr2溶液中滴入少量氯水,发生的反应为2Fe2++Cl2=2Fe3++2Cl-,A错误;
B. 比较C、Si非金属性强弱,可以比较C、Si的最高价氧化物的水化物的酸性强弱,向硅酸钠溶液中通入少量二氧化碳,发生的反应为SiO32-+CO2+H2O=H2SiO3↓+CO32-,B正确;
C. 除去CO2中的SO2,将气体通入盛有饱和碳酸氢钠溶液的洗气瓶,HCO3-不能拆开写,发生的反应为2HCO3-+SO2= SO32-+CO2+H2O,C错误;
D. 实验室制取氯气,向MnO2固体中加入浓盐酸并加热,盐酸是强酸,要写成离子形式,发生的反应为MnO2+4H++2Cl-![]() 2Mn2++Cl2↑+2H2O,D错误。
2Mn2++Cl2↑+2H2O,D错误。
故选B。


科目:高中化学 来源: 题型:
【题目】将64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为22.4 L。请计算(写出计算过程):
(1)NO标况下的体积________
(2)参加反应的HNO3的物质的量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在日常生活和生产中有着重要的应用。下列说法不正确的是( )
A. 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B. 某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为溶液中的SO32—水解
C. 将饱和FeCl3溶液滴入沸水中可制备Fe(OH)3胶体,利用的是盐类水解原理
D. 纯碱溶液呈碱性的原因是CO32—+H2O![]() HCO3—+OH-
HCO3—+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“![]() ”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
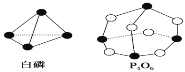
【题目】化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆 开)1mol 化学键时释放(或吸收)的能量。已知白磷和![]() 的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P—P:198,P—O:360,O=O:498,则对于反应
的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P—P:198,P—O:360,O=O:498,则对于反应![]() 表述正确的是 ( )
表述正确的是 ( )
A.放出1638 kJ 的热量B.吸收1638 kJ 的热量
C.放出126 kJ 的热量D.吸收126 kJ 的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁-次氯酸盐电池的工作原理如图,该电池反应为:![]() 。下列有关说法正确的是( )
。下列有关说法正确的是( )
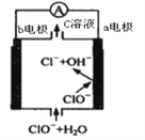
A.电池工作时,正极 a 附近的 pH 将不断增大
B.电池工作时,C溶液中的溶质是![]()
C.负极反应式:![]()
D.a 电极发生还原反应,每转移 0.2mol电子,理论上生成 0.2mol ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性KMnO4、H2O2在生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要的氧化试剂,下面是对这三种氧化剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式____________________,氧化产物与还原产物的物质的量之比为_______。
(2)取300 mL 0.2 mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是_____ mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是_________________(用文字表达),又变为棕黄色的离子方程式是_____________________。
(4)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474 g KMnO4样品溶解酸化后,用0.100 mol·L-1标准Na2S2O3溶液进行滴定,标准Na2S2O3溶液应盛装在___(填“酸式”或“碱式”)滴定管中。配平上述反应的离子方程式:___MnO4-+___S2O32-+____H+=____Mn2++_____SO42-+____H2O,实验中,滴定至终点时消耗Na2S2O3溶液12.00 mL,则该样品中KMnO4的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用不同的实验装置研究苯与液溴的反应并制取少量溴苯。试回答下列问题:


(1)若采用图甲装置进行实验,装置A中应预先需加入的试剂是____,E装置的作用是___。
(2)若采用图乙装置进行实验,C中盛放的CCl4的作用是____________。
(3)若使用图乙装置,实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,然后用___(填仪器名称)分离出溴苯(仍含有少量苯)。写出有关的离子反应方程式__________。
(4)反应完毕后,向试管D中滴加AgNO3溶液,若有_______(填现象)生成,说明这种获得溴苯的反应属于______ (填有机反应类型)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com