

| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ②HNO3 | ③NaOH ④KOH | ⑤Na2SO4 ⑥K2SO4,KNO3 | ⑦SO2 ⑧SO3 | ⑨NH3 |
分析 (1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树;
(2)酸电离出的阳离子全部是氢离子的化合物;碱电离出的阴离子全部为氢氧根离子;盐电离出得阳离子为金属离子,阴离子为酸根离子;氧化物时两种元素组成,其中一种是氧元素的化合物;氢化物是两种元素组成,其中一种是氢元素的化合物;
(3)电解质是在水溶液中或熔融状态下导电的化合物;
(4)硫酸和氢氧化钠溶液反应实质是氢离子和氢氧根离子发生反应生成水;
(5)实验室中利用氯化铵和氢氧化钙加热反应生成氨气;
(6)摩尔质量以g/mol作单位,数值上等于其相对分子质量;
根据n=$\frac{m}{M}$计算氨气的物质的量,根据N=nNA计算氨气分子数目,结合氨气分子含有的H原子数目计算氢原子物质的量;
根据n=$\frac{m}{M}$计算二氧化碳的物质的量,再根据m=nM计算氧气的质量.
解答 解:(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树,有叶、枝、杆、根,图示方法就是树状图,
故答案为:树状分类法;
(2)酸电离出的阳离子全部是氢离子的化合物,如HNO3;盐电离出得阳离子为金属离子,阴离子为酸根离子,如K2SO4,KNO3等,
故答案为:②HNO3;⑥K2SO4,KNO3等
(3)酸碱盐都是电解质,①H2SO4 属于酸式电解质,③NaOH属于碱是电解质,⑦SO2 属于非金属氧化物,本身不能电离出离子属于非电解质,⑨NH3 本身不能电离出离子属于非电解质,
故答案为;①③;
(4)①与③发生中和反应离子方程式为H++OH-=H2O,故答案为:H++OH-=H2O;
(5)实验室制备⑨NH3的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2,故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2;
(6)硝酸的摩尔质量为63g/mol;
3.4g氨气的物质的量=$\frac{3.4g}{17g/mol}$=0.2mol,含有分子数目=0.2mol×NAmol-1=0.2NA,含有H原子物质的量=0.2mol×3=0.6mol;
标况下,4.48L CO2的物质的量=$\frac{4.48L}{22.4L/mol}$=0.2mol,与其等物质的量的氧气的质量=0.2mol×32g/mol=6.4g,
故答案为:63g/mol;0.2;0.2NA;0.6;6.4.
点评 本题考查了物质分类方法,电解质概念分析判断.离子方程式和化学方程式书写,题目较简单.


科目:高中化学 来源: 题型:选择题
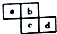
| A. | 原子半径:c>d>a>b | |
| B. | 原子序数d可能是a的3倍 | |
| C. | 最高价含氧酸的酸性c可能比d强 | |
| D. | 四种元素的氢化物可能是18电子分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由此可确定碘元素的相对原子质量为131 | |
| B. | $\stackrel{131}{53}$I是碘元素的一种同位素 | |
| C. | $\stackrel{131}{53}$I核素中含中子数为53 | |
| D. | $\stackrel{131}{53}$I2的摩尔质量为262 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某烷烃的名称为2,2,4,4-四甲基-3,3,5-三乙基己烷 | |
| B. | 今年5月18日桐庐县320国道化学品运输车侧翻造成1,1,2,2-四氯乙烷泄漏,该有机物是一种重要的有机溶剂,不溶于水且密度比水小 | |
| C. | 如图所示的有机物分子式为C14H12O2,此有机物能与NaHCO3溶液反应放出CO2气体 | |
| D. | 化合物 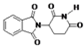 在酸性条件下水解,所得溶液加碱后加热有NH3生成 在酸性条件下水解,所得溶液加碱后加热有NH3生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
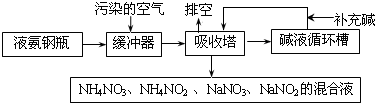
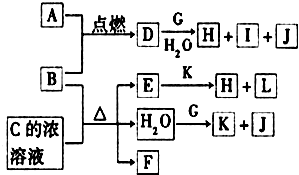 图中,A~L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见的金属单质,E的稀溶液为蓝色,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味的气体,且能使品红溶液褪色.
图中,A~L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见的金属单质,E的稀溶液为蓝色,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味的气体,且能使品红溶液褪色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,0.5molH2中含有的H原子数 | |
| B. | 22.4升HCl气体中含有的Cl原子 | |
| C. | 1L1mol/L硫酸溶液所含的H+数 | |
| D. | 0.1mol金属铝含有的电子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com