
| A、D元素处于元素周期表中第3周期第Ⅳ族 |
| B、B与D形成的化合物中,每个原子的最外层电子均为8个电子 |
| C、B、D的最高价氧化物中,D的最高价氧化物熔沸点高的根本原因在于D的最高价氧化物相对分子质量比B的最高价氧化物高 |
| D、A与D形成的化合物是一种稳定性较差的非极性分子 |


科目:高中化学 来源: 题型:
| A、1molH2含有的电子数 |
| B、通常状况下,22.4LCO2所含的分子数 |
| C、0.012kg12C所含的原子数 |
| D、1L1mol?L-1的CaCl2溶液所含的Cl-数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
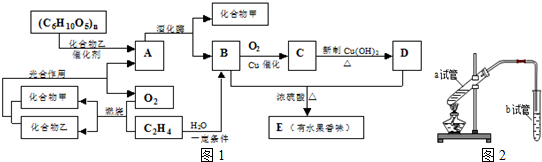
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、位于元素周期表中短周期 |
| B、原子最外层有1个电子 |
| C、属于金属元素,和Na同属于ⅠA族 |
| D、能和水反应,生成氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
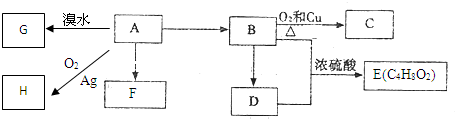
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、逸出气体若用碱石灰吸收,增重b克.则测定混合物中Na2CO3的质量分数偏小 |
| B、把所得溶液加热蒸干,并灼烧至恒重,得b克固体.蒸干过程中若未搅拌,则所测Na2CO3的质量分数可能偏大 |
| C、某NaOH标准溶液露置于空气中一段时间后,以甲基橙为指示剂,仍用此碱液滴定上述反应后的溶液,则所测Na2CO3的质量分数偏大 |
| D、产生的气体冷却至室温后,若测定其体积时忘记调平量气管和水准管内液面,则导致Na2CO3的质量分数偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
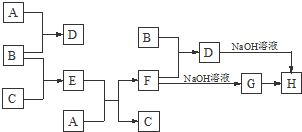
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL 1mol/LNaCl溶液 |
| B、150mL 3mol/LKCl溶液 |
| C、75mL 1mol/LMgCl2溶液 |
| D、25mL 2mol/LAlCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com